Слайд 2Важное значение имеют макростехиометрические характеристики биотехнологического процесса.
Они выражают взаимосвязь между приростом биомассы,

продукта и расходованием субстрата.
Слайд 3выход по субстрату, или экономический коэффициент (или коэффициент выхода).
определяют, сравнивая количество

выросшей за весь цикл ферментации биомассы Хк к количеству загруженного субстрата So :
Yxs=Xк/S0
Слайд 4Выход по продукту метаболизма:
Yps=Рк/S0
Различия в обозначении коэффициентов делают с помощью

индексов: по биомассе обозначают как Yxs , по продукту — как Yps.
Слайд 5
дополнения
коэффициент Yxs определен не совсем точно. В начале процесса уже

существует некоторое количество биомассы, определяемое ее концентрацией X0, так что прирост ее за время ферментации меньше, чем Хк, и равен (Хк - X0).
В то же время не весь субстрат до конца расходуется за время процесса; какая-то часть его, определяемая конечной концентрацией SK, останется, так что потребление субстрата будет не «So,
a (So - SK).
Слайд 6Экономические коэффициенты:
Yxs = (Xk – X0)/ (S0 – Sk) = ΔX/ΔS
[г.

биомассы/ г. субстрата]
Аналогичным образом для продукта метаболизма:
Yps = (Pk – P0)/ (S0 – Sk ) = ΔP/ΔS
[г.продукта/ г. субстрата]
Слайд 7Метаболические, или трофические, коэффициенты:
Ysx = 1/Yxs = (S0 – Sk)/ (Xk –

X0) = ΔS/ΔX
[г. субстрата/ г. биомассы]
Ysp = 1/Yps = (S0 – Sk)/ (Pk – P0) = ΔS/ΔP
[г. субстрата/ г. продукта]
Слайд 8 В пределе можно рассматривать промежуток ∆t сколь угодно малым — вплоть

до бесконечно малого dt, и ему будут соответствовать сколь угодно малые приросты dX, dP и dS.
Так же можно получить мгновенные текущие коэффициенты (относительные стехиометрические коэффициенты):
Yxs = dX/dS; Yps = dP/dS;
Ysx = dS/dX; Ysp = dS/dP, а также относительных - Ypx = dP/dX; Yxp = dX/dP
Слайд 9Стехиометрия процессов культивирования
микроорганизмов

Слайд 10Основные принципы
стехиометрии
Экономический, метаболический коэффициенты выхода продукта по субстрату и биомассе

— это в простейшем виде стехиометрические коэффициенты.
Они нужны для того, чтобы по одной из известных величин (например, ∆S), рассчитать и другие характеристики процесса (например, ∆Х, ∆Р).
Слайд 11
Если в результате взаимодействия реагентов А и В получаются продукты С

и D и выделяется тепло ∆Н,
с помощью стехиометрических коэффициентов ʋA, ʋB, ʋc, ʋD и ʋn получится стехиометрическое уравнение:
ʋAA + ʋBB = ʋcC + ʋD D + ʋnΔH
Слайд 12 Стехиометрические коэффициенты подбирают таким образом, чтобы выразить фундаментальный закон природы —

закон сохранения материи.
Количество атомов любого элемента, входящего в вещества А, В, С и D, не должно изменяться в процессе превращения веществ.
Слайд 13В биологии также действует закон сохранения материи.
В ходе биологических превращений

в клетке перегруппировываются атомы углерода, азота, фосфора, водорода, кислорода и других жизненно важных химических элементов.
Но общее количество каждого из этих элементов, включенное в структуры клетки, в точности равно количеству, взятому клеткой из питательной среды.
Слайд 14 Процесс ферментации можно представить как систему, в которой происходит преобразование исходных

реагентов (субстратов) в продукты (клетки и продукты метаболизма).
В аэробных процессах в число субстратов входит кислород О2, а в число продуктов — диоксид углерода СО2.
Другие субстраты и продукты в разных процессах различные, но стехиометрические соотношения между ними должны соблюдаться.
Слайд 15по аналогии со стехиометрией в микробиологическом процессе
ʋc [углеродный субстрат] +
+ʋN [азотный
![по аналогии со стехиометрией в микробиологическом процессе ʋc [углеродный субстрат] + +ʋN](/_ipx/f_webp&q_80&fit_contain&s_1440x1080/imagesDir/jpg/975173/slide-14.jpg)
субстрат] +
+ʋф [фосфорный субстрат] +
+ ʋО [О2] +.... = ʋх[биомасса] +
+ ʋр[продукт метаболизма] +
+ ʋcо2 [СО2] + ʋн2о[H2O] +... + ʋнΔН
Слайд 16ВЫВОД «ФОРМУЛЫ» БИОМАССЫ МИКРООРГАНИЗМОВ
биомасса, состоящая из множества индивидуальных веществ — белков,

нуклеиновых кислот, липидов и так далее, многие из которых даже не идентифицированы.
Все эти вещества записывают целой совокупностью, «связкой».
Слайд 17 какой-то существующей в природе истинной «формулы» биомассы нет.
нужен фиктивный, эмпирический

вид «формулы» биомассы
За основу принят элементный состав биомассы (высушенной).
Слайд 18элементный состав микроорганизмов
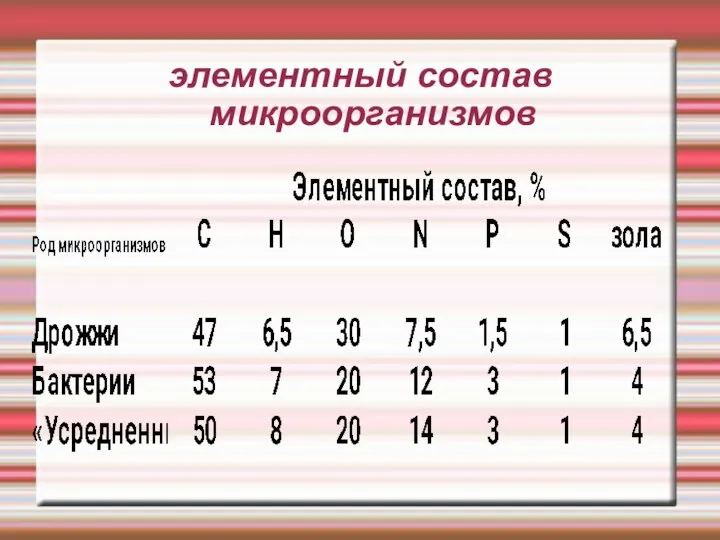
Слайд 19Как теперь из этого элементного состава получить «формулу» биомассы?
Если принять сухую

массу биомассы равной 100 г, то состав, выраженный в таблице в процентах, будет отражать массу соответствующего элемента в граммах.
Разделив эту массу на атомную массу соответствующего элемента, получаем количество грамм-атомов в 100 г сухой биомассы.
Слайд 20Расчет числа грамм-атомов элементов в 100 г сухой биомассы
тип м/о С Н
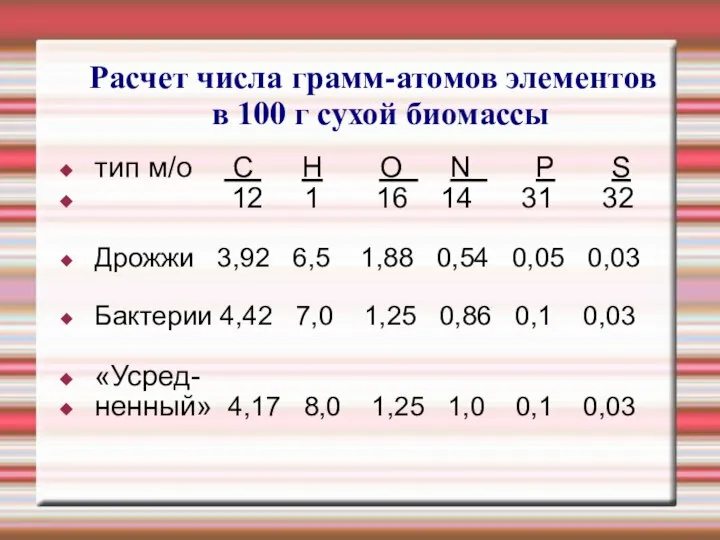
О N P S
12 1 16 14 31 32
Дрожжи 3,92 6,5 1,88 0,54 0,05 0,03
Бактерии 4,42 7,0 1,25 0,86 0,1 0,03
«Усред-
ненный» 4,17 8,0 1,25 1,0 0,1 0,03
Слайд 21 в первом приближении «формулу» дрожжей можно записать как
С3,92Н6,5О1,88N0,54P0,05S0,03
бактерий —

С4,42Н7О1,25N0,86P0,1S0,03
«усредненной» биомассы — С4,17Н8О1,25N1P0,1S0,03
Слайд 22чтобы придать видимость правдоподобия «формуле», ее умножают на какое-то очень большое число,

чтобы все коэффициенты оказались целыми числами.
Самое простое в данном случае — умножить на 100
Слайд 23 в стехиометрических расчетах обычно пренебрегают элементами, составляющими малую часть состава биомассы.

В «формуле» отбрасывают фосфор и серу, а иногда и азот.
Слайд 24 в стехиометрическом уравнении все члены можно умножить или разделить на одно

и то же число.
без ущерба для расчетов можно произвольно «принять» «молекулярную массу» для биомассы какой угодно с последующим пересчетом всех стехиометрических коэффициентов в уравнении.
Слайд 25Удобно принимать такую «молекулярную массу», чтобы в ней оказался только один атом

(грамм-атом) углерода.
Для этого в ранее вычисленных «формулах» биомассы достаточно все индексы при атомах разделить на индекс при атоме углерода.
Такой условный моль, приведенный к одному атому углерода, называют С-моль.
Слайд 26 дрожжи — CH1,66O0,48N 0,14,
бактерии — CH1,58O0,28N0,19;
«усредненная» биомасса — CH1,92O0,30N0,24;

Слайд 27для «усредненной» биомассы используется формула, предложенная Стоутхамером для С-моля:
CH1,8O0,5N0,2
Из-за простоты эту формулу

применяют в расчетах.
Слайд 28Рассчет «молекулярной массы»
С-моля:
М= 1·12 + 1,8·1 + 0,5·16 + 0,2·14 =

24,6
по брутто-формуле биомассы, проводят стехиометрические расчеты, как в химических уравнениях.
Слайд 29 РАСЧЕТ ВЫХОДА БИОМАССЫ НА УГЛЕРОДНЫЙ СУБСТРАТ
наибольший интерес с учетом

выхода составляет самый дорогой субстрат — углеродный.
в качестве углеродного субстрата могут использоваться разные вещества: глюкоза, крахмал, этанол, метанол, парафины нефти, метан и другие.
Слайд 30Эти вещества можно также пересчитать на С-моль (т.е. оставить в молекуле только

один атом углерода).
Например, для глюкозы с формулой C6H12O6 С-моль будет иметь формулу СН2О,
для крахмала с формулой (С6Н12О6) - вид С-моля не изменится.
Слайд 31разные субстраты дают различный стехиометрический выход по биомассе.
фактически измеренные данные выхода биомассы

отличаются от теоретически рассчитанных: максимальный выход — на парафинах, минимальный — на углеводах.
фактический выход «не дотягивает» до стехиометрического.
Слайд 32 Чтобы объяснить эти расхождения, ввели понятие «энергетический выход» биомассы.
- в

каждом субстрате заключена энергия, которая зависит от степени восстановленности субстрата γs, которую легко определить, если известна формула вещества.
При этом, как и в биомассе, учитывают основные элементы — углерод, водород, кислород и азот.
Обобщенная формула субстрата —
СmНnOpNq
Слайд 33 Степень восстановленности зависит от числа так называемых «доступных электронов», или «редоксонов».

Принимают, что один атом углерода имеет 4 доступных электрона, один атом водорода - 1 доступный электрон.
Кислород доступных электронов не имеет, а наоборот, как бы забирает на себя 2 электрона, т.е. имеет отрицательное число (-2) доступных электронов.
То же и с азотом, который забирает 3 (-3) доступных электрона.
Слайд 34степень восстановленности субстрата CmHnOpNq рассчитывают по формуле:
γs = 4m + n -

2р - 3q
Слайд 35Оценка биомассы по степени восстановленности (обозначение γх)
Биомасса (CHl,8O0,5N0,2):
γX =4 х 1 +

1,8 – 2 х 0,5 – 3 х 0,2 = 4,2.
для диоксида углерода СО2, воды Н2О и аммиака NH3 степень восстановленности γs = 0.
Слайд 36 В.К. Ерошиным введено понятие энергетический выход биомассы, представляющий собой отношение энергии

в субстрате к энергии, заключенной в биомассе:
η = γs/ γx
Величина η показывает, какое количество С-молей биомассы можно получить из одного С-моля субстрата исходя из соотношения энергий.
Слайд 37метан η = 8,0/4,2 = 1,9 С-моль биомассы/C-моль субстрата;
гексан η = 6,3/4,2

= 1,5
метанол η = 6,0/4,2 = 1,43;
глюкоза η = 4,0/4,2 = 0,95;
этанол η = 6,0/4,2 = 1,43;
н-алканы η = 6,0/4,2 = 1,43;
щавелевая кислота η = 1,0/4,2 = 0,24
Слайд 38 В формуле для η выход выражен в С-молях биомассы на С-моль

субстрата. От него можно перейти и к обычному массовому выходу:
YXS = η Mx/Ms
где Мх и Ms — молекулярные массы С-молей биомассы и субстрата соответственно.
Слайд 39
метан YXS = 1,9 х 24,6/16 = 2,92 г биомассы/ г субстрата;

гексан YXS = 1,5 х 24,6/14,3 = 1,72
метанол YXS = 1,43 х 24,6/32 = 1,1
глюкоза YXS = 0,95 х 24,6/30 = 0,78
этанол YXS = 1,43 х 24,6/23 = 1,53 г
н-алканы YXS = 1,43 х 24,6/14 = 2,51
Слайд 40для глюкозы энергетический выход биомассы дает значения чуть ниже стехиометрического (0,78 против

0,82), но при этом отличие от фактического (0,5) все еще велико.
Получается, что биомассы может быть даже больше, чем по стехио-метрическим расчетам, а это противоречит здравому смыслу.
Ведь из одного атома углерода не может получиться два, как это предсказывает, например, энергетический выход по метану.
Слайд 41ОПРЕДЕЛЕНИЕ СТЕХИОМЕТРИЧЕСКИХ СООТНОШЕНИЙ В РЕАЛЬНЫХ ПРОЦЕССАХ ФЕРМЕНТАЦИИ
исходные предпосылки «энергетической» теории материального

баланса неверны.
Они не учитывают того, что в клетке одновременно протекают как бы два процесса.
1. Катаболизм.
2. Анаболизм.
Слайд 42общее стехиометрическое соотношение для объединенного процесса:
ʋs S + ʋo2 [02] + ʋN
![общее стехиометрическое соотношение для объединенного процесса: ʋs S + ʋo2 [02] +](/_ipx/f_webp&q_80&fit_contain&s_1440x1080/imagesDir/jpg/975173/slide-41.jpg)
[NH3] → X + ʋp [P] + + ʋco2 [CO2] + ʋH2O[H2O]
биомасса выражена в С-молях, а субстрат — в обычных молях.
Слайд 43
Необходимо знать, количество израсходованного субстрата (в реальных мерах — граммы, килограммы и

т. д.) и количество образовавшейся биомассы микроорганизмов или продукта метаболизма — соответственно Gs, Gx и GP (в пересчете на весь аппарат) или для периодического процесса приращения их концентраций — соответственно ∆S, ∆Х и ∆Р.
Слайд 44 Разделив эти величины на молекулярные массы соответственно субстрата, биомассы или продукта,

получаем для этих веществ количества г молей (или кг • молей), которые и являются основой для последующих стехиометрических расчетов.
Слайд 45 Первый из этих расчетов — приведение всех количеств к одному С-молю

биомассы.
обычно находят такие стехиометрические коэффициенты, которые дают стехиометрический коэффициент при биомассе, выраженной в С-молях, равным 1,
ʋs S + ʋo2 [02] + ʋN [NH3] → X + ʋp [P] + + ʋco2 [CO2] + ʋH2O[H2O]
Слайд 46Таким образом сразу находим ʋs и ʋР.
Для определения коэффициентов по другим

веществам (О2, СО2, NH3 и Н2О) необходимо составить и решить систему уравнений элементного баланса
каждое вещество (субстрат, биомасса, продукт, вода, кислород, диоксид углерода) может быть описано общей элементной формулой CmHnOpNq.
Слайд 47 При этом индексы в формуле субстрата обозначим как ms, ns, ps,

qs,
в формуле продукта — соответственно тР, nР, рР, qР.
Для биомассы соответствующие индексы тх= 1, nх= 1,8, Рх= 0,5, qx= 0,2.
Слайд 48 уравнение баланса по углероду:
ʋSmS = 1 + ʋpmp + ʋCO2
То же

для водорода:
ʋSnS + ʋNH3 · 3 = 1,8 + ʋpnp + ʋH2O · 2
Слайд 49Уравнение баланса по кислороду:
ʋSpS + ʋO2 · 2 = 0,5 + ʋpPp

+ ʋCO2 · 2 + ʋH2O · 1
Уравнение баланса по азоту:
ʋsqs + ʋNH3 = 0,2 + ʋpqp
Слайд 50 Решение системы уравнений позволит найти все стехиометрические коэффициенты для данного процесса

ферментации.
Для примера рассмотрим конкретный процесс производства лимонной кислоты.
Известно, что в процессе ферментации на 1 кг потребленной сахарозы получается 0,6 кг лимонной кислоты и 0,3 кг сухой биомассы. Рассчитайте стехиометрические коэффициенты уравнения
Слайд 51Переведем все величины в г моли соответствующих веществ
Молекулярная масса (г/моль): сахарозы

(С12Н22О11) равна 342, лимонной кислоты (СбН8О7) — 192, С-моль биомассы — 24,6.
Отсюда в молях:
1000/342 [CI2H22O11] → 300 /24,6 [X] +
+ 600 /192 [C6H8O7]
2,92[CI2H22O11] →12,20 [X] + 3,13 [C6H8O7].
Слайд 52 Пересчитаем все стехиометрические коэффициенты на С-моль биомассы, т.е. разделим обе части

равенства на 12,2.
0,24 [С12Н22О11] → [X] + 0,26 [С6Н8О7].
для полного уравнения есть:
ʋs = 0,24 и ʋP= 0,26.
Слайд 53Для нахождения оставшихся коэффи-циентов записываем систему уравнений элементного баланса для данного процесса
При

этом для субстрата (сахарозы) значения индексов:
ms =12, ns= 22, ps= 11, qs = 0
Для продукта (лимонной кислоты):
mР = 6, nР= 8, рР = 7, qP = 0.
Баланс по углероду: ʋSmS = 1 + ʋpmp + ʋCO2
0,24 · 12 = 1+ 0,26 · 6 + ʋCO2,
ʋCO2=0,32.
Слайд 54Баланс по водороду: ʋSnS + ʋNH3 · 3 = 1,8 + ʋpnp

+ ʋH2O · 2
0,24 · 22 + ʋNH3 · 3 = 1,8 + 0,26 · 8 + 2 · ʋH2O,
или
2ʋH2O - 3ʋNH3 = l,4.
Слайд 55Баланс по кислороду: ʋSpS + ʋO2 · 2 = 0,5 + ʋpPp

+ ʋCO2 · 2 + ʋH2O
0,24 · 11 + 2 ʋO2 = 0,5 + 7 · 0,26 + 2 · 0,32 + ʋH2O,
или
2 ʋO2 – ʋH2O = 0,32
Слайд 56 Баланс по азоту: ʋsqs + ʋNH3 = 0,2 + ʋpqp
0 +

ʋNH3 = 0,2 + 0
откуда ʋNH3 = 0,2
из 2 ʋH2O – 3 ʋNH3 = l,4,
ʋH2O = 1,0
из 2 ʋO2 – ʋH2O = 0,32;
ʋO2 = 0,66













![по аналогии со стехиометрией в микробиологическом процессе ʋc [углеродный субстрат] + +ʋN](/_ipx/f_webp&q_80&fit_contain&s_1440x1080/imagesDir/jpg/975173/slide-14.jpg)


























![общее стехиометрическое соотношение для объединенного процесса: ʋs S + ʋo2 [02] +](/_ipx/f_webp&q_80&fit_contain&s_1440x1080/imagesDir/jpg/975173/slide-41.jpg)














 Кровеносная система дождевого червя
Кровеносная система дождевого червя Птицы
Птицы Практикум по гистологии
Практикум по гистологии Белки, состав, структура, функции
Белки, состав, структура, функции Группы животных
Группы животных Редуценты. Истинные редуценты и детритофаги
Редуценты. Истинные редуценты и детритофаги Основы фитопатологии
Основы фитопатологии Критические факторы, влияющие на развитие плода
Критические факторы, влияющие на развитие плода Физиология сердца и сосудов
Физиология сердца и сосудов Конвергенция. Дивергенция
Конвергенция. Дивергенция Отряд двукрылые (Diptera)
Отряд двукрылые (Diptera) Мышцы головы и шеи
Мышцы головы и шеи Морфология бактерий
Морфология бактерий Презентация на тему "Удивительные олигохеты Австралийский гигантский дождевой червь" - презентации по Биологии
Презентация на тему "Удивительные олигохеты Австралийский гигантский дождевой червь" - презентации по Биологии Хрящевые рыбы
Хрящевые рыбы Зоогеографическое районирование Мирового океана
Зоогеографическое районирование Мирового океана Трахея. Поперечный срез трахеи
Трахея. Поперечный срез трахеи Виды РНК. тРНК
Виды РНК. тРНК Биосинтез белка
Биосинтез белка Спячка у птиц
Спячка у птиц Екологічні групи і життєві форми рослин
Екологічні групи і життєві форми рослин Өсімдіктерді сауықтыру
Өсімдіктерді сауықтыру Предмет и история биомеханики
Предмет и история биомеханики Углеводы. Образование углеводов (реакция фотосинтеза)
Углеводы. Образование углеводов (реакция фотосинтеза) Черепные нервы (V,VI,VII,VIII). Нормальная анатомия и некоторые клинические аспекты
Черепные нервы (V,VI,VII,VIII). Нормальная анатомия и некоторые клинические аспекты Сложное простым языком. Оптическая система глаза
Сложное простым языком. Оптическая система глаза 7. Строение кл
7. Строение кл Презентация на тему Звери запасаются жиром
Презентация на тему Звери запасаются жиром