Содержание
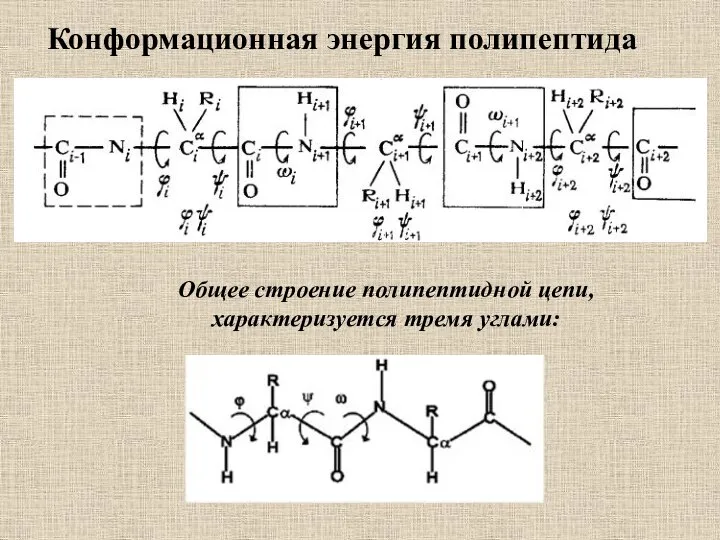
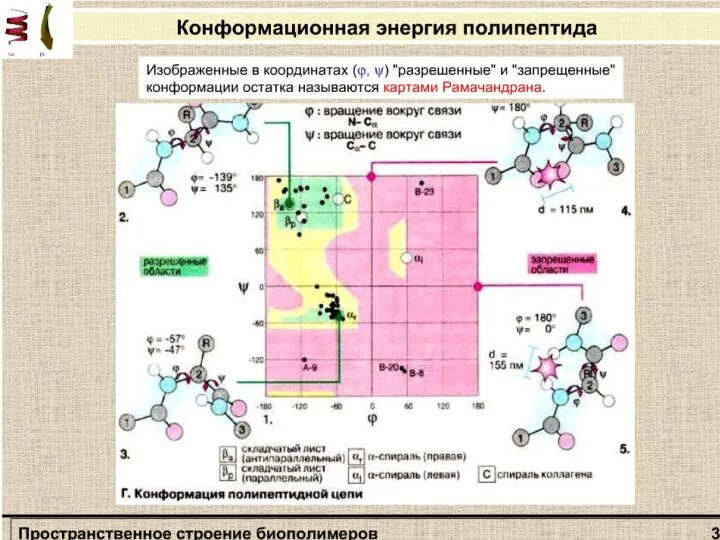
- 2. Конформационная энергия полипептида Общее строение полипептидной цепи, характеризуется тремя углами:
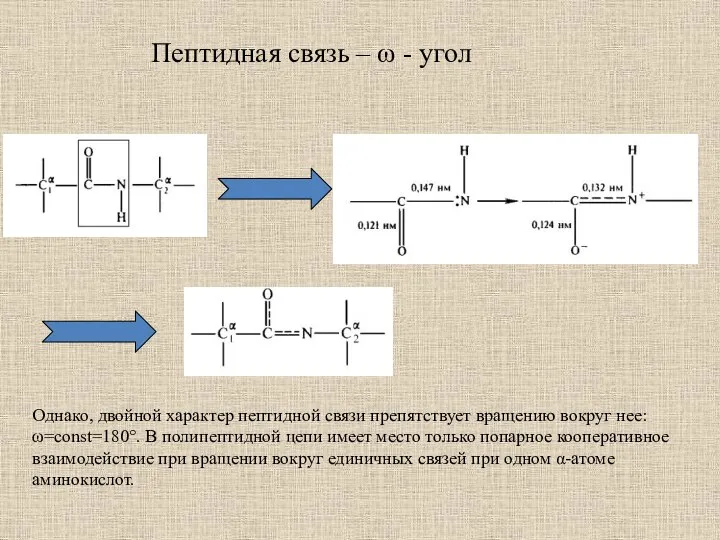
- 3. Пептидная связь – ω - угол Однако, двойной характер пептидной связи препятствует вращению вокруг нее: ω=const=180°.
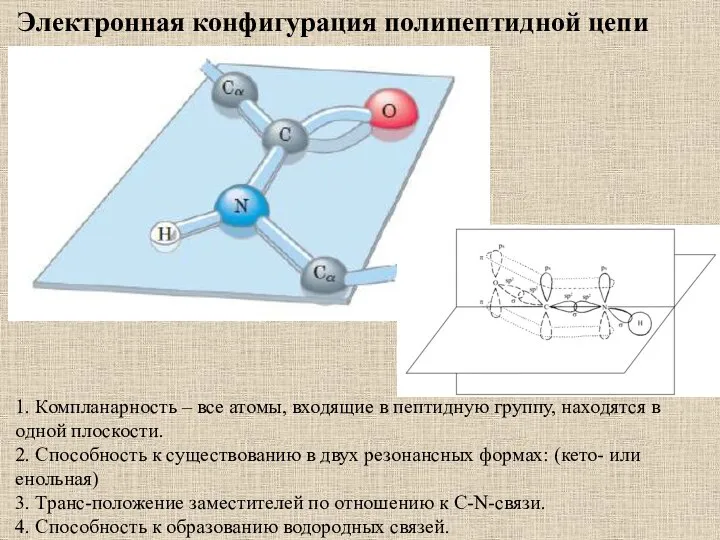
- 4. 1. Компланарность – все атомы, входящие в пептидную группу, находятся в одной плоскости. 2. Способность к
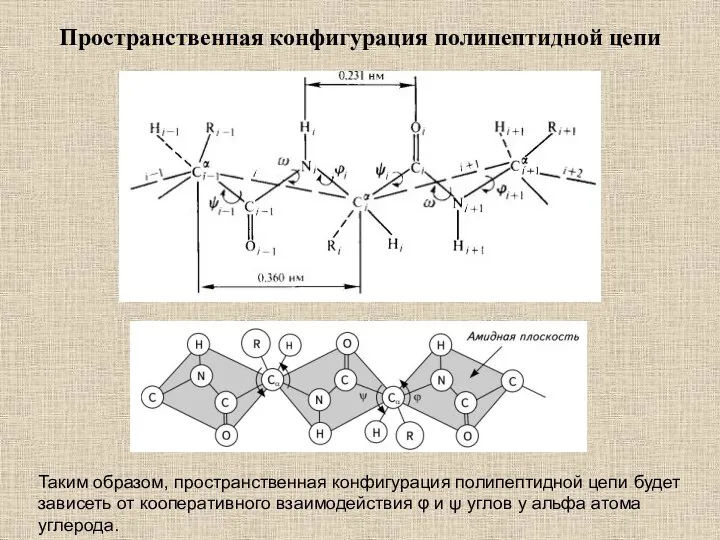
- 5. Пространственная конфигурация полипептидной цепи Таким образом, пространственная конфигурация полипептидной цепи будет зависеть от кооперативного взаимодействия φ
- 6. Не все значения углов ψ и φ допустимы вследствие возможного стерического несоответствия двух соседних аминокислотных остатков.
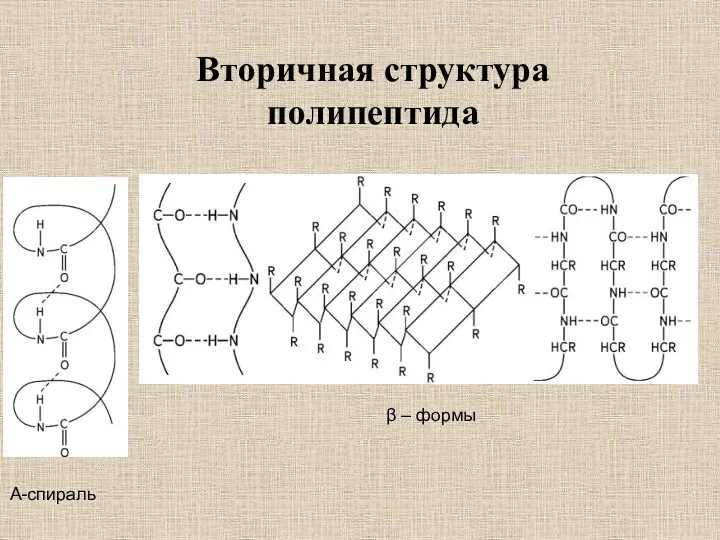
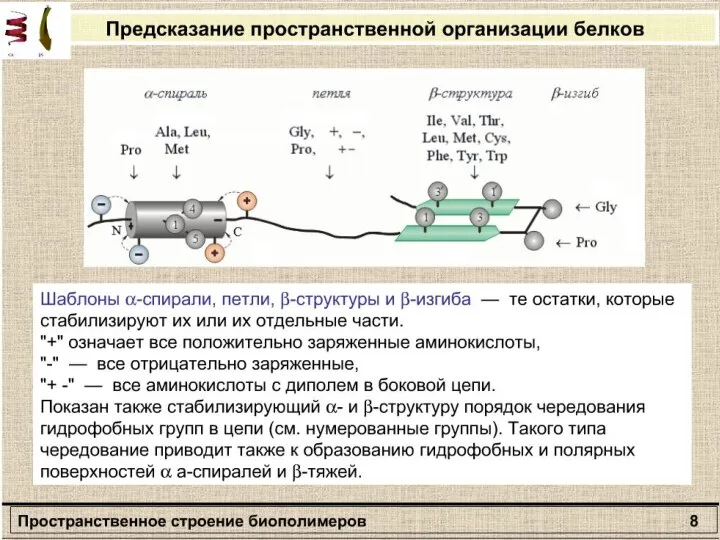
- 12. Вторичная структура полипептида Α-спираль β – формы
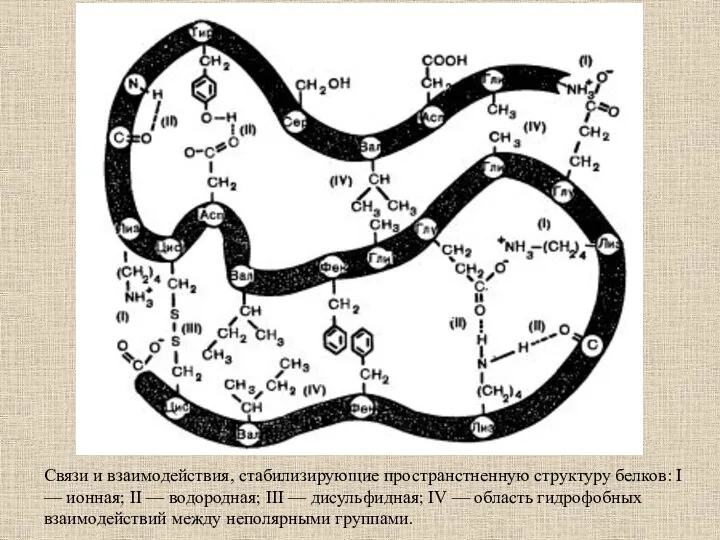
- 13. Связи и взаимодействия, стабилизирующие пространстненную структуру белков: I — ионная; II — водородная; III — дисульфидная;
- 27. Раздел: Молекулярная биофизика Тема: Динамика биополимеров
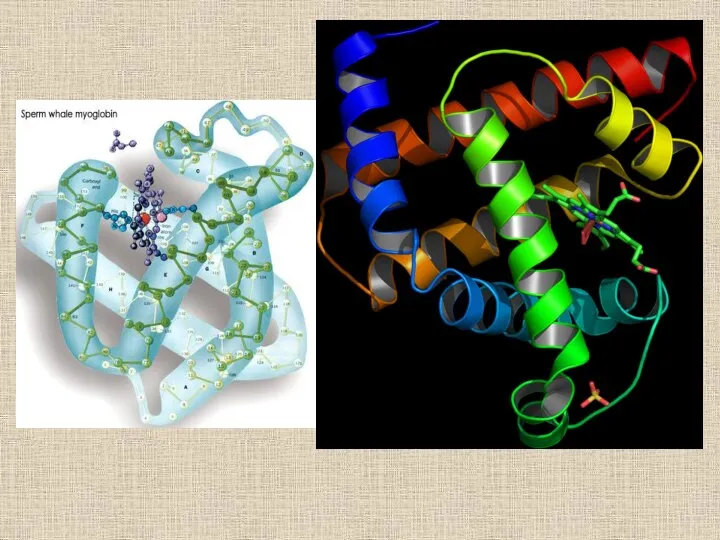
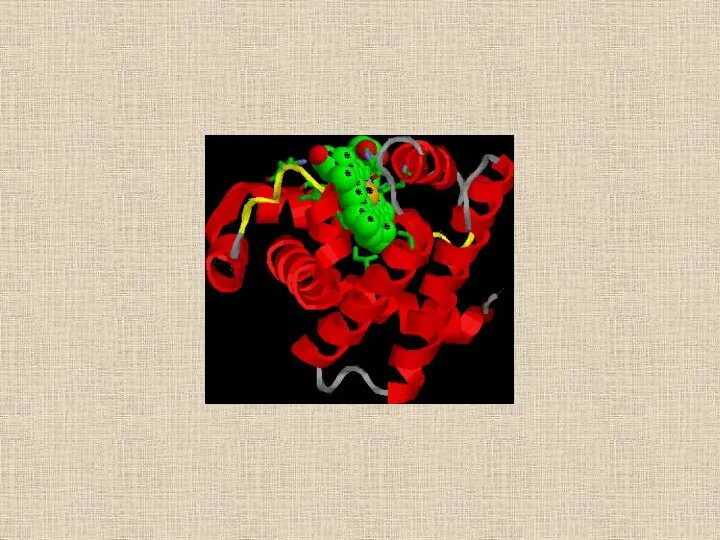
- 28. Пространственная структура миоглобина (кашалота) в проекции ху Миоглобин (переносчик кислорода в мышцах) содержит один гем и
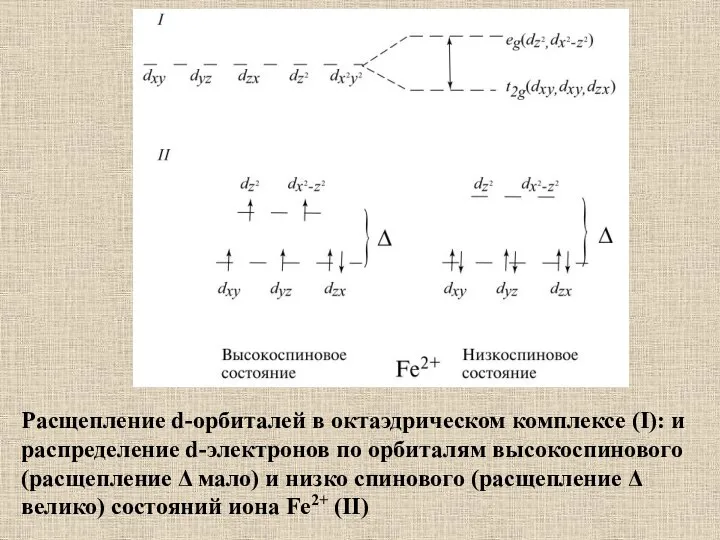
- 29. Расщепление d-орбиталей в октаэдрическом комплексе (I): и распределение d-электронов по орбиталям высокоспинового (расщепление Δ мало) и
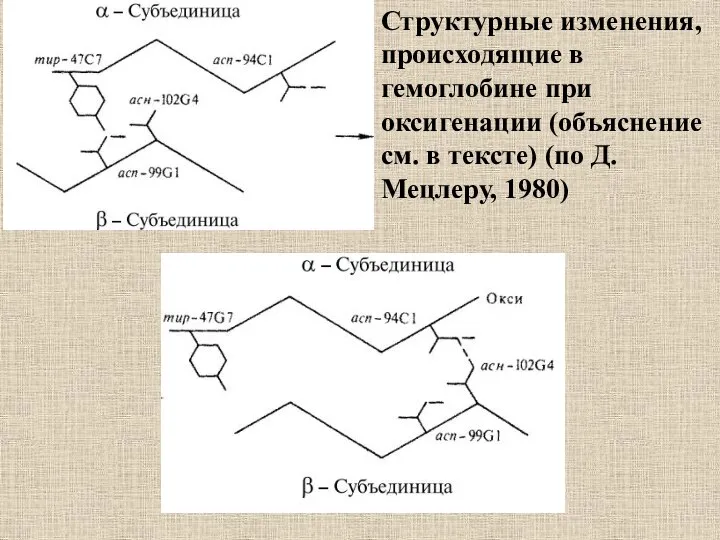
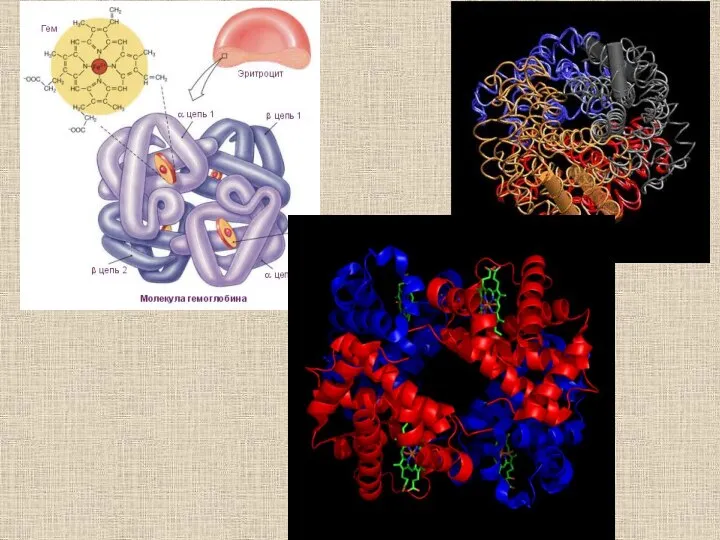
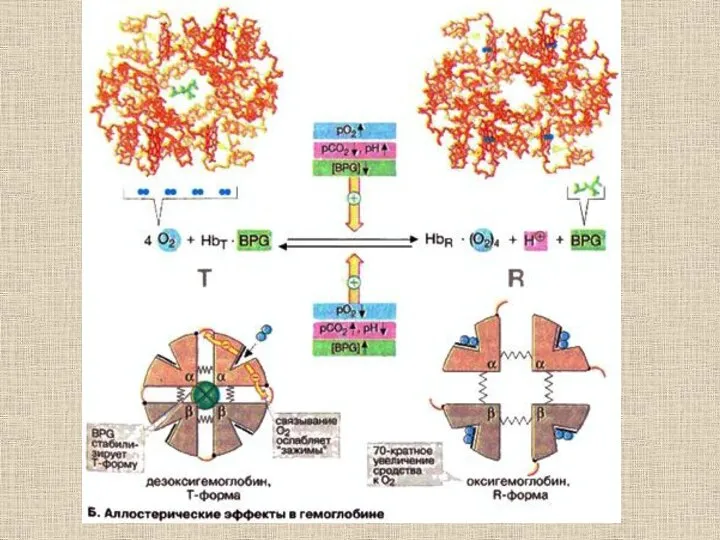
- 30. Структурные изменения, происходящие в гемоглобине при оксигенации (объяснение см. в тексте) (по Д. Мецлеру, 1980)
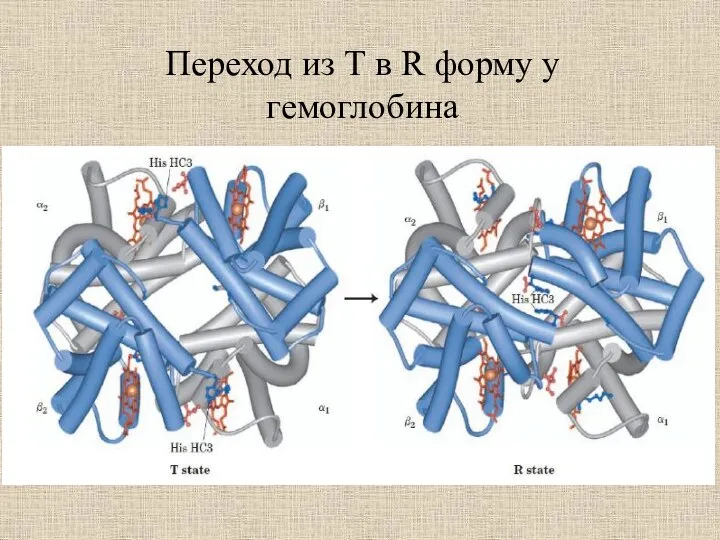
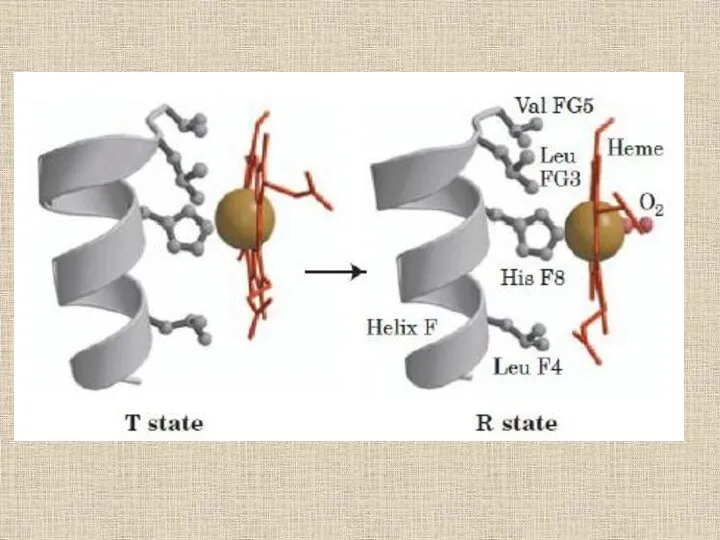
- 31. Переход из T в R форму у гемоглобина
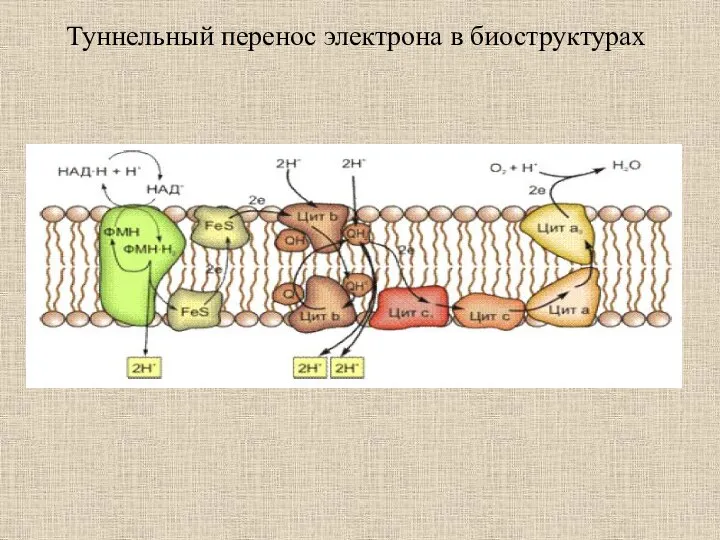
- 33. Туннельный перенос электрона в биоструктурах
- 34. Методы изучения подвижности белков Люминесцентные методы ЭПР ЯМР ЯГР спектроскопия Метод изотопного обмена
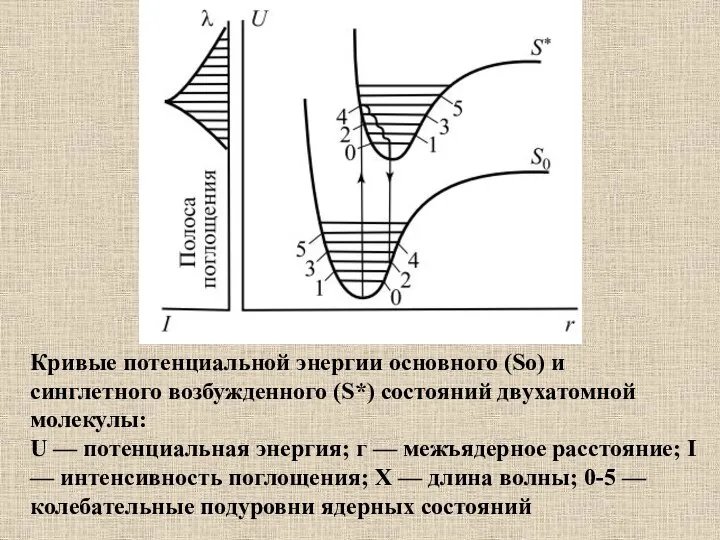
- 35. Кривые потенциальной энергии основного (So) и синглетного возбужденного (S*) состояний двухатомной молекулы: U — потенциальная энергия;
- 36. Электронные уровни органической молекулы и переходы между ними (схема Яблонского): р — вероятность переходов в единицу
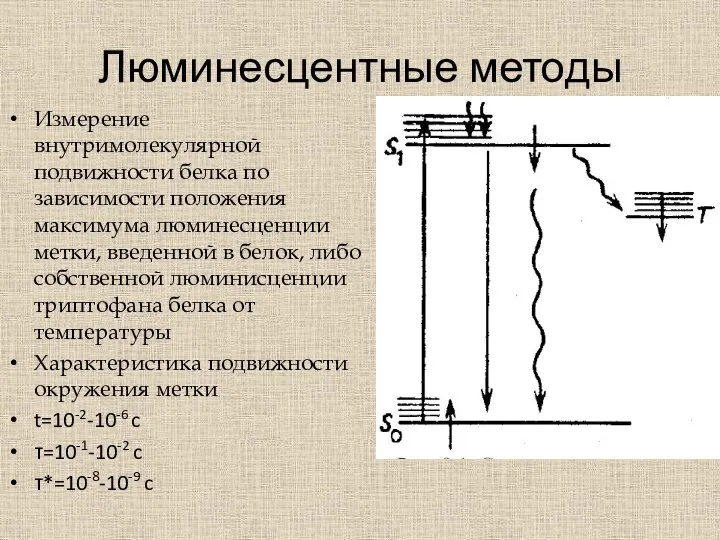
- 37. Люминесцентные методы Измерение внутримолекулярной подвижности белка по зависимости положения максимума люминесценции метки, введенной в белок, либо
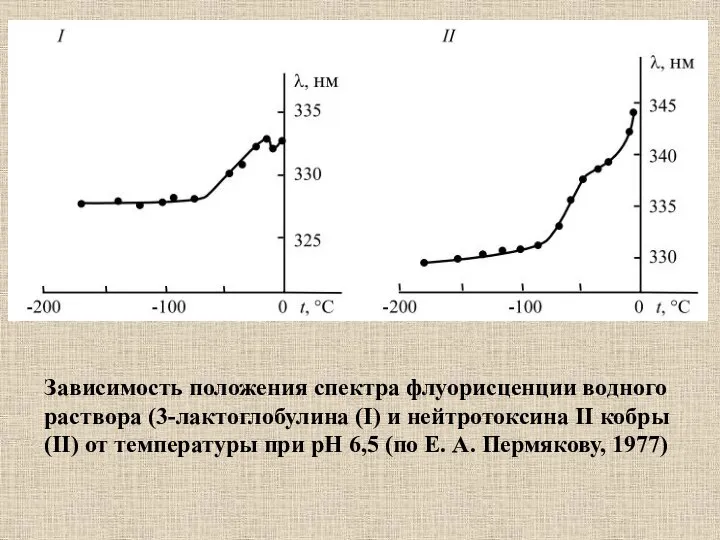
- 38. Зависимость положения спектра флуорисценции водного раствора (3-лактоглобулина (I) и нейтротоксина II кобры (II) от температуры при
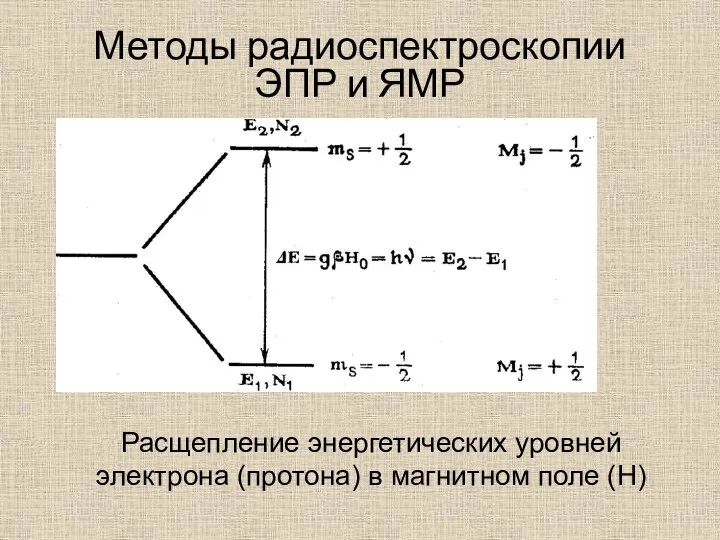
- 39. Методы радиоспектроскопии ЭПР и ЯМР Расщепление энергетических уровней электрона (протона) в магнитном поле (Н)
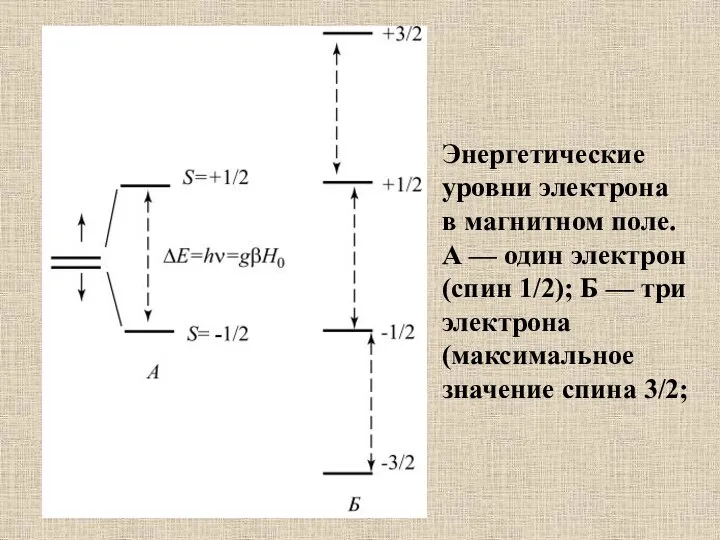
- 40. Энергетические уровни электрона в магнитном поле. А — один электрон (спин 1/2); Б — три электрона
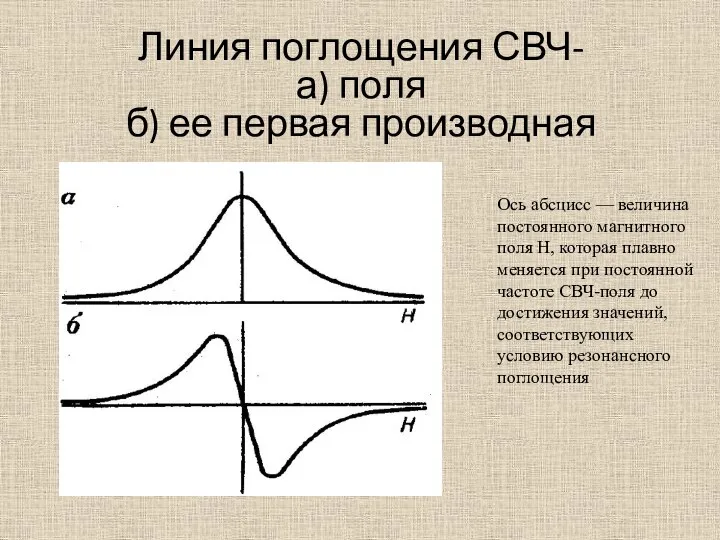
- 41. Линия поглощения СВЧ- а) поля б) ее первая производная Ось абсцисс — величина постоянного магнитного поля
- 42. Линия резонанса ЭПР Ширина: Т1 – время передачи энергии окружающей среде Т2 – время спин-спинового взаимодействия
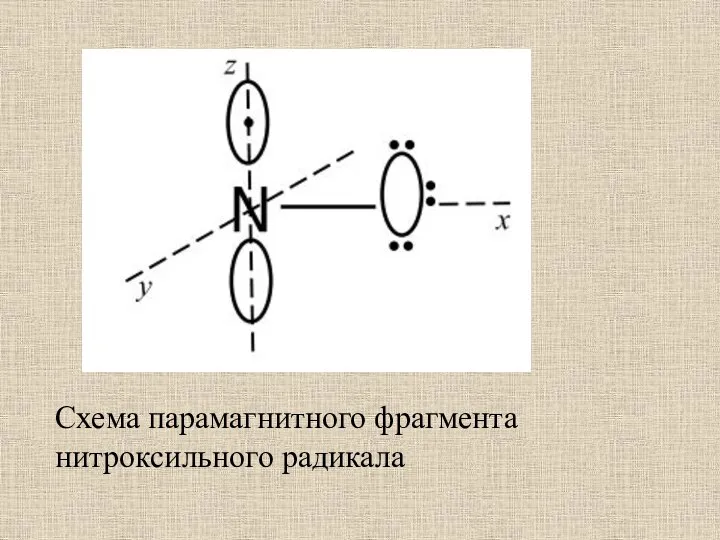
- 43. Схема парамагнитного фрагмента нитроксильного радикала
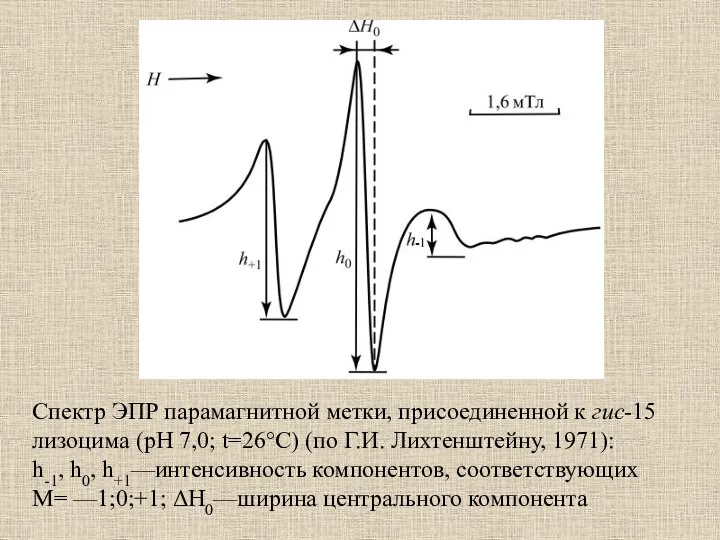
- 44. Спектр ЭПР парамагнитной метки, присоединенной к гис-15 лизоцима (рН 7,0; t=26°C) (по Г.И. Лихтенштейну, 1971): h-1,
- 45. ЯМР-спектроскопия Измерение времени релаксации Т1 и Т2 по ширине линии резонанса. Определение времени вращения метки, на
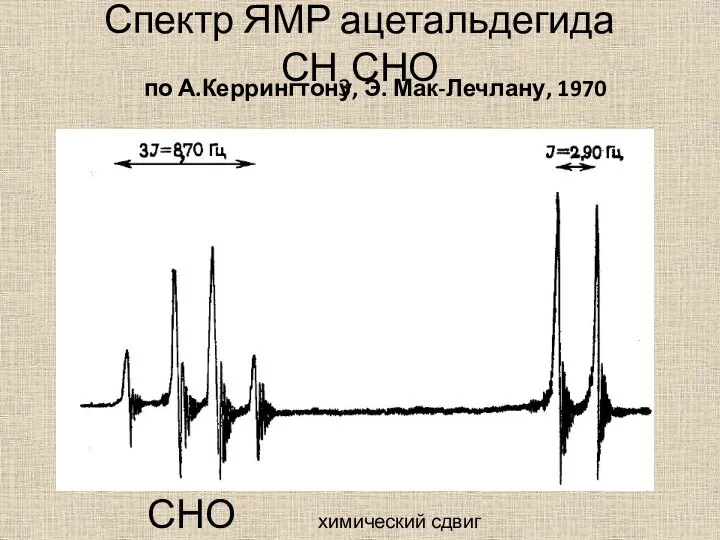
- 46. Спектр ЯМР ацетальдегида СН3СНО СНО химический сдвиг СН3 по А.Керрингтону, Э. Мак-Лечлану, 1970
- 47. ЯГР спектроскопия Дает информацию не только о временных, а также амплитудных характеристиках движений в белке (средние
- 48. Эффект Мёссбауэра Уширение спектра обусловлено диффузией молекул белка. Изменение частоты уширения пропорционально скорости источника (v)
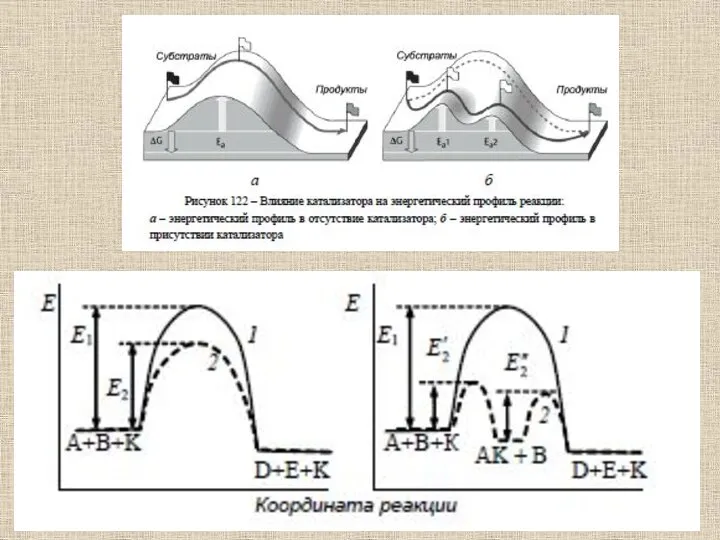
- 51. Ферментативный катализ
- 52. Ферменты (от латинского fermentum – закваска), энзимы (от греческого en – "в" и zyme – "закваска")
- 53. Ферменты отличаются от других катализаторов тремя уникальными свойствами: - высокой эффективностью действия, - специфичностью действия, -
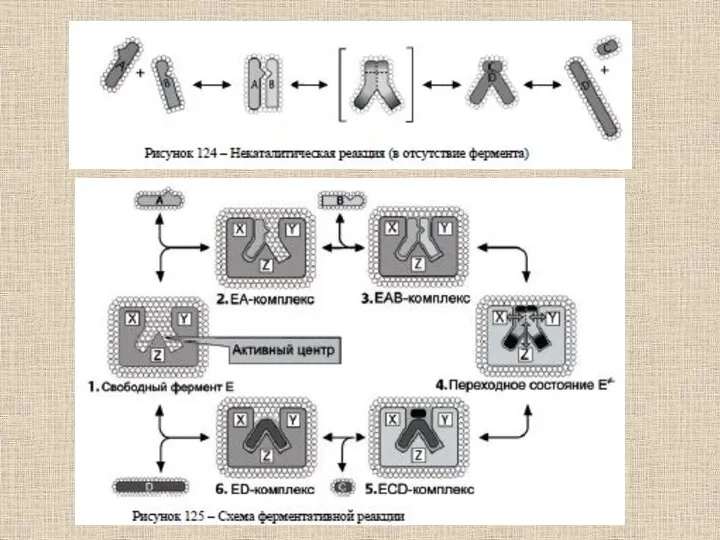
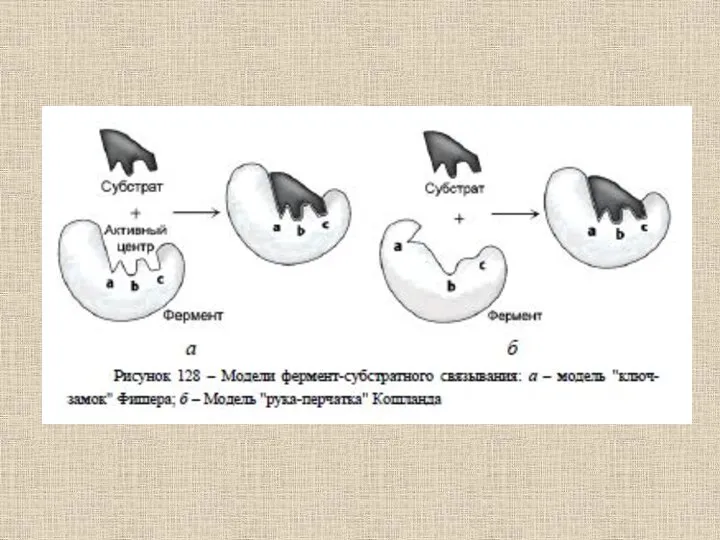
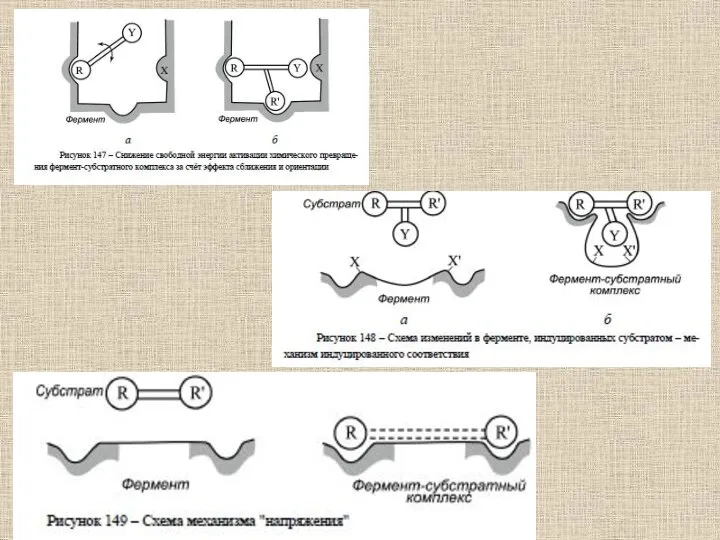
- 59. Взаимодействия, которые играют главную роль при связывании субстрата в активном центре фермента и образовании комплекса фермент-субстрат
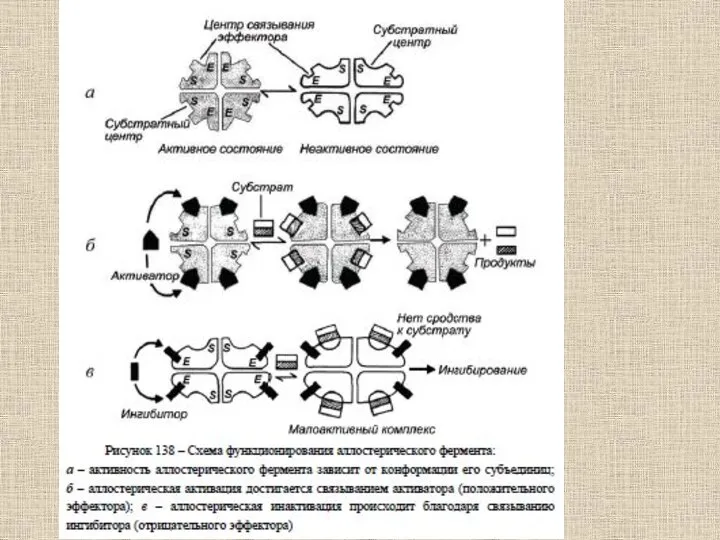
- 61. Основные механизмы управления каталитической активностью фермента связаны со следующими явлениями и процессами: 1) аллостерия; 2) кооперативность;
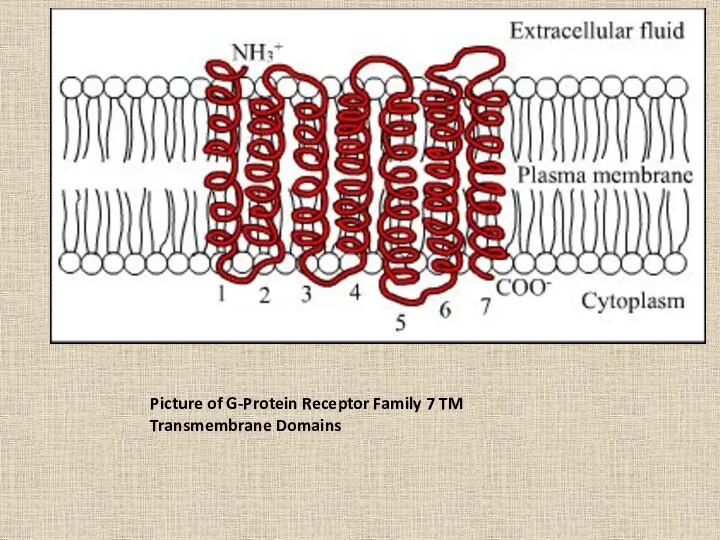
- 65. Picture of G-Protein Receptor Family 7 TM Transmembrane Domains
- 71. Скачать презентацию
























 Немецкая овчарка
Немецкая овчарка Презентация на тему РАЗНООБРАЗИЕ РАСТЕНИЙ
Презентация на тему РАЗНООБРАЗИЕ РАСТЕНИЙ 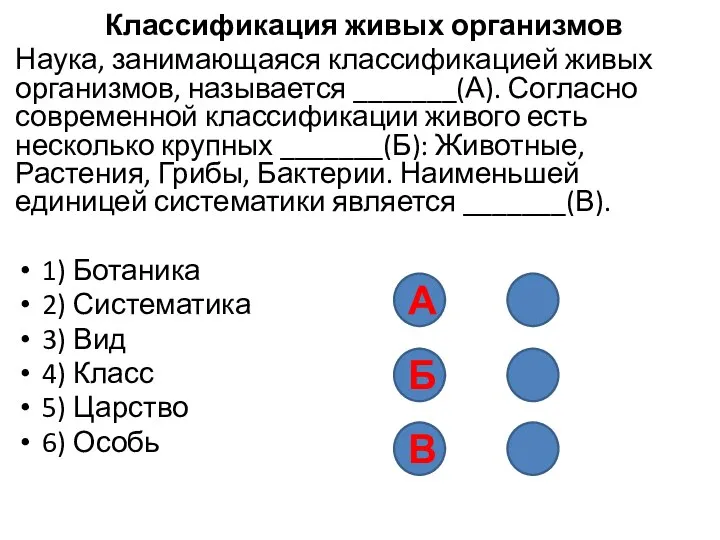 Классификация живых организмов
Классификация живых организмов Презентация на тему ГИГИЕНА ПИТАНИЯ
Презентация на тему ГИГИЕНА ПИТАНИЯ  Презентация на тему Царства живой природы
Презентация на тему Царства живой природы  Выполнила Ученица 9 а класса Школы № 953 Васильева Маргарита Научный руководитель: Гусева Наталья Геннадьевна
Выполнила Ученица 9 а класса Школы № 953 Васильева Маргарита Научный руководитель: Гусева Наталья Геннадьевна Презентация на тему Признаки живых организмов
Презентация на тему Признаки живых организмов  Познавательная игра Эти удивительные растения
Познавательная игра Эти удивительные растения Викторина Планета рыб (4)
Викторина Планета рыб (4) Внешнее строение дождевого червя. Лабораторная работа
Внешнее строение дождевого червя. Лабораторная работа Электронный плакат, птица Гаичка
Электронный плакат, птица Гаичка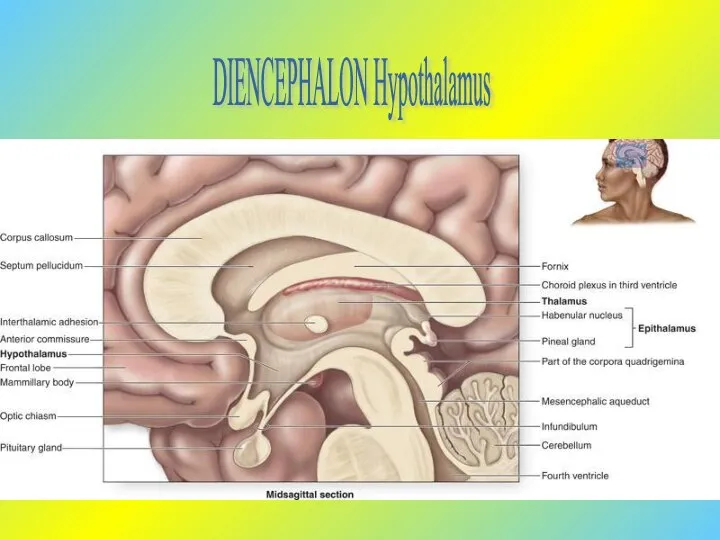 Паравентрикулярное ядро. Дорсальный гипоталамус
Паравентрикулярное ядро. Дорсальный гипоталамус Тип Членистоногие
Тип Членистоногие ЛРС. Малина
ЛРС. Малина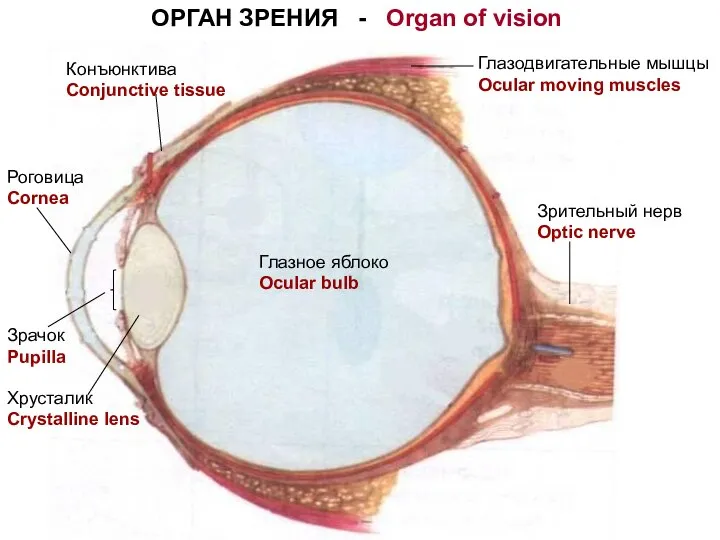 Орган зрения
Орган зрения Деревья и плоды
Деревья и плоды Сущность жизни и свойства живого. Уровни организации живой материи
Сущность жизни и свойства живого. Уровни организации живой материи Инструменты для груминга
Инструменты для груминга Обычная презентация
Обычная презентация Клеточный уровень. Клеточная теория. 10 класс
Клеточный уровень. Клеточная теория. 10 класс Полезные комнатные растения
Полезные комнатные растения Виды соцветий
Виды соцветий Просмотр и определение вида животной ткани
Просмотр и определение вида животной ткани Метофазный метод учета хромосомных аберраций
Метофазный метод учета хромосомных аберраций Технологии животноводства. Заболевания животных и их предупреждение
Технологии животноводства. Заболевания животных и их предупреждение Živočíchy - vylučovanie
Živočíchy - vylučovanie Kosterní svalovina
Kosterní svalovina Дезоксирибонуклеиновая кислота (ДНК) и Рибонуклеиновая кислота (РНК)
Дезоксирибонуклеиновая кислота (ДНК) и Рибонуклеиновая кислота (РНК)