Содержание
- 2. Цель урока Формирование представлений о единой научной картине мира через модель атома Резерфорда
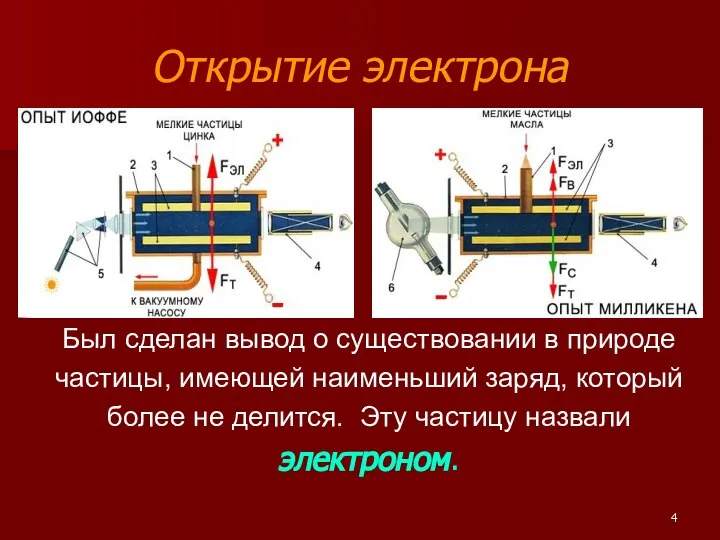
- 3. Дискретность электрического заряда Существование мельчайших частиц, имеющих наименьший электрический заряд, было доказано опытами А.Ф.Иоффе и Р.Милликена
- 4. Открытие электрона Был сделан вывод о существовании в природе частицы, имеющей наименьший заряд, который более не
- 5. Электрон Обозначают знаком ē Электрон очень мал. Масса электрона составляет 9,1* 10 -31 кг. За единицу
- 6. Заряд электрона Значение элементарного электрического заряда Заряд электрона – предел делимости электрического заряда, поэтому его называют
- 7. Модель атома Томсона Атом представляет собой равномерно положительно заряженный шар, внутри которого плавают отрицательные электроны. Дж.
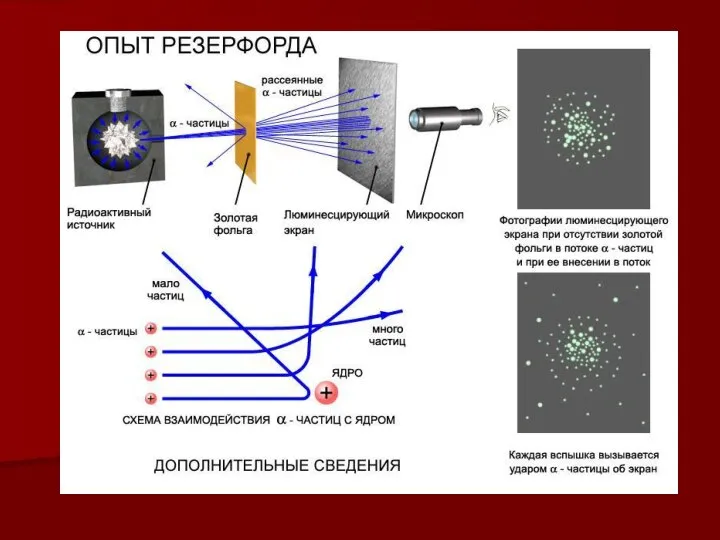
- 9. Строение атома Опыт Э.Резерфорда по рассеянию альфа-частиц привёл к открытию новой – планетарной модели атома. Э.
- 10. Модель атома Резерфорда В центре атома находится положительно заряженное ядро, состоящее из протонов и нейтронов. Вокруг
- 11. Ядро атома Занимает очень малый объём атома В нём сосредоточена почти вся масса атома Заряд ядра
- 12. Протоны Положительно заряженные элементарные частицы. Обозначают протоны знаком p+ Масса протона в 1840 раз больше массы
- 13. Нейтроны Нейтральные (не имеющие заряда) частицы ядра. Нейтроны обозначают знаком n0. Масса нейтрона приблизительно равна массе
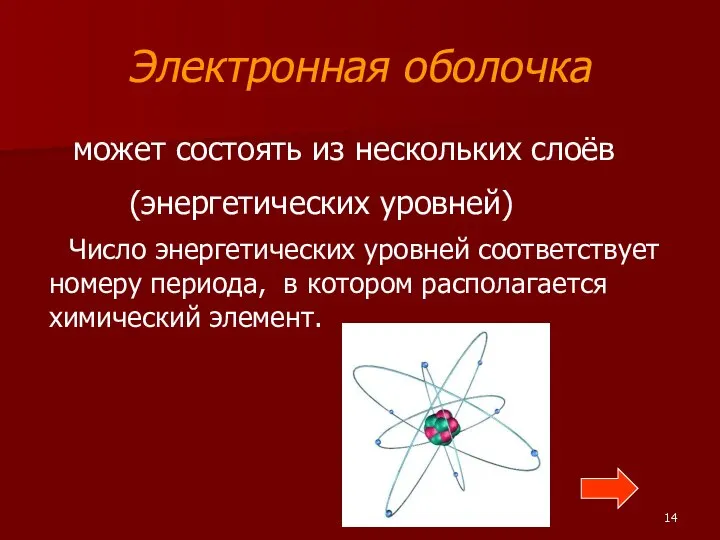
- 14. Электронная оболочка может состоять из нескольких слоёв (энергетических уровней) Число энергетических уровней соответствует номеру периода, в
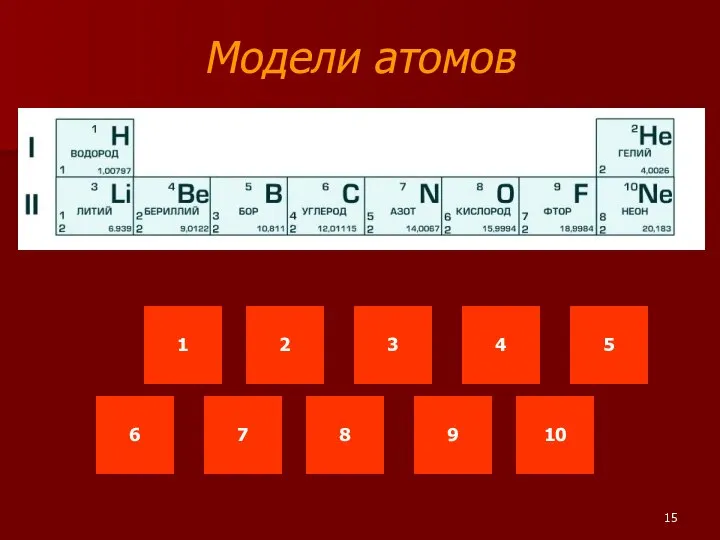
- 15. Модели атомов 1 3 4 5 10 6 7 8 9 2
- 16. Модель атома водорода 1p+ 1ē
- 17. Модель атома гелия 2p+ 2n0 2ē
- 18. Модель атома лития 3p+ 4n0 3ē
- 19. Модель атома бериллия 4p+ 5n0 4ē
- 20. Модель атома бора 5p+ 6n0 5ē
- 21. Модель атома углерода 6p+ 6n0 6ē
- 22. Модель атома азота 7p+ 7n0 7ē
- 23. Модель атома кислорода 8p+ 8n0 8ē
- 24. Модель атома фтора 9p+ 10n0 9ē
- 25. Модель атома неона 10p+ 10n0 10ē
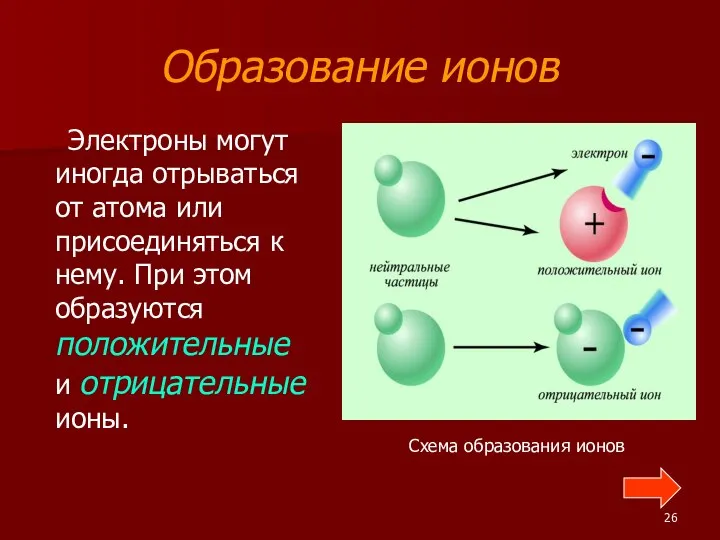
- 26. Образование ионов Электроны могут иногда отрываться от атома или присоединяться к нему. При этом образуются положительные
- 27. Схема образования иона если атом азота потерял два электрона, то он превращается в положительный ион с
- 28. Схема образования иона если атом азота приобрёл три электрона, то он превращается в отрицательный ион с
- 29. Вопросы на закрепление Как на опыте показать, что электрический заряд делится на части? Как назвали частицу
- 30. Делимость электрического заряда
- 31. Нуклоны Протон – положительно заряженная элементарная частица. Обозначение p+ Масса протона в 1840 раз больше массы
- 33. Скачать презентацию

























 Колебания и плавность хода автомобиля
Колебания и плавность хода автомобиля Презентация на тему Масса. Вес и невесомость
Презентация на тему Масса. Вес и невесомость  Колебания. Общие понятия
Колебания. Общие понятия Механическое движение
Механическое движение Бензиновые двигатели
Бензиновые двигатели Физические свойства веществ при низких температурах. Свойства криогенных жидкостей
Физические свойства веществ при низких температурах. Свойства криогенных жидкостей Поверхностное натяжение
Поверхностное натяжение ИК-спектроскопия (часть 1)
ИК-спектроскопия (часть 1) Направление и пределы самопроизвольного протекания физико-химических процессов
Направление и пределы самопроизвольного протекания физико-химических процессов Применение ядерной энергии в различных отраслях. Доза радиоактивного излучения. Атомная энергетика
Применение ядерной энергии в различных отраслях. Доза радиоактивного излучения. Атомная энергетика Количество теплоты. Удельная теплоёмкость
Количество теплоты. Удельная теплоёмкость Презентация на тему Импульс тела
Презентация на тему Импульс тела  Презентация на тему Солнце (11 класс)
Презентация на тему Солнце (11 класс)  Наглядные примеры проведения демонстрационных экспериментов на уроках физики с использованием школьного осциллографа
Наглядные примеры проведения демонстрационных экспериментов на уроках физики с использованием школьного осциллографа Уравнение газа состояния идеального
Уравнение газа состояния идеального Испарение и конденсация
Испарение и конденсация Посадки. Основы построения и расчет предельных отклонений
Посадки. Основы построения и расчет предельных отклонений Движение тел
Движение тел Поиск материалов с заданными свойствами. Практическая работа
Поиск материалов с заданными свойствами. Практическая работа Объединенный газовый закон
Объединенный газовый закон Построение зубчатого зацепления вручную карандашом
Построение зубчатого зацепления вручную карандашом Волны. Интерференция и дифракция
Волны. Интерференция и дифракция Стационарное электрическое поле
Стационарное электрическое поле Презентация на тему Реактивное движение
Презентация на тему Реактивное движение  3 slides
3 slides Механические колебания и волны. Решение задач
Механические колебания и волны. Решение задач Möbius band
Möbius band Давление. Урок физики
Давление. Урок физики