Слайд 3Гибридизация атомных орбиталей – изменение формы и энергии орбиталей атома при образовании ковалентной

связи для достижения более эффективного перекрывания орбиталей.
Слайд 4Различные орбитали, несильно отличающиеся энергиями, образуют соответствующее число гибридных орбиталей. Число гибридных

орбиталей равно числу атомных орбиталей, участвующих в гибридизации. Гибридные орбитали одинаковы по форме электронного облака и по энергии.
Слайд 5В гибридизации участвуют не только связывающие электроны, но и неподеленные электронные пары.

Слайд 6По сравнению с атомными орбиталями гибридные более вытянуты в направлении образования химических

связей и поэтому обуславливают лучшее перекрывание электронных облаков.
Слайд 7Гибридная орбиталь больше вытянута по одну сторону ядра,
чем по другую.

Слайд 9sp-гибридизация - это гибридизация, в которой участвуют атомные орбитали одного s- и одного p-электронов
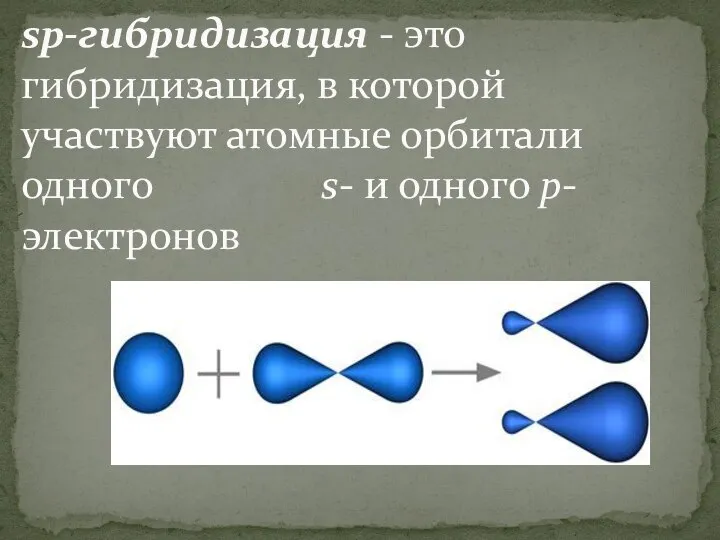
Слайд 10
В процессе гибридизации образуются 2 гибридные орбитали, которые ориентируются друг к другу под

углом 180°
Слайд 11
Представление о sp-гибридизации орбиталей можно применить для объяснения линейной формы молекулы BeH2, в

которой атом бериллия образован гибридными
sp-орбиталями.
Слайд 12Образование молекулы фторида бериллия .
Каждый атом фтора, входящий в состав этой молекулы,

обладает одним неспаренным электроном,
который и участвует в образовании ковалентной связи.
Слайд 13
Атом бериллия в невозбужденном состоянии неспаренных электронов не имеет:
Поэтому для участия в образовании
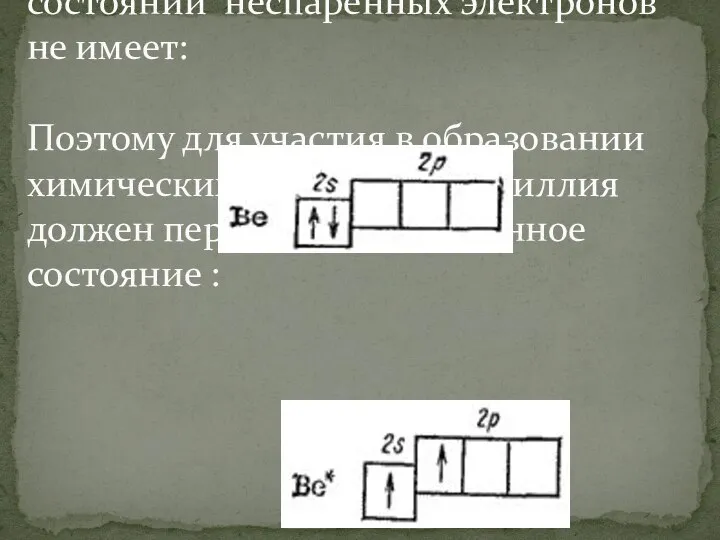
химических связей атом бериллия должен перейти в возбужденное состояние :
Слайд 14при затрате некоторой энергии вместо исходных s- и р-орбиталей атома бериллия могут

образоваться две равноценные гибридные орбитали
(sp-орбитали).
Слайд 15Примеры химических соединений, для которых характерна
sp-гибридизация: BeCl2, BeH2,CO, CO2, HCN, карбин, ацетиленовые углеводороды (алкины).

Слайд 16sp2-гибридизация – гибридизация, в которой участвуют атомные орбитали одного s- и двух p-электронов

Слайд 17В результате гибридизации образуются три гибридные sp2 орбитали, расположенные в одной плоскости под углом

120° друг к другу
Слайд 18Этот тип гибридизации наблюдается в молекуле BCl3.

Слайд 19sp2-гибридизация атома бора в молекуле фторида бора .
Здесь вместо исходных одной s-
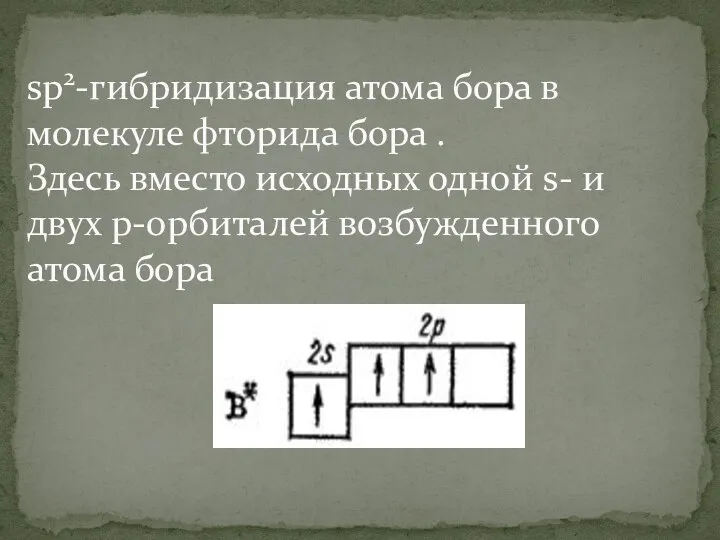
и двух р-орбиталей возбужденного атома бора
Слайд 20образуются три равноценные
sp2-орбитали. Поэтому молекула построена в форме правильного треугольника, в центре которого

расположен атом бора, а в вершинах—атомы фтора.
Слайд 21Примеры соединений, в которых наблюдается sp2-гибридизация: SO3, BCl3, BF3, AlCl3, CO32-, NO3-, графит,

этиленовые углеводороды (алкены), карбоновые кислоты и ароматические углеводороды (арены).
Слайд 22sp3-гибридизация – гибридизация, в которой участвуют атомные орбитали одного s- и трех
p-электронов

Слайд 23Четыре sp3-гибридные орбитали симметрично ориентированны в пространстве под углом 109°28'

Слайд 24
не всегда пространственная конфигурация молекулы соответствует тетраэдру, это зависит от числа атомов

в молекуле.
Примером тому служат молекул воды и аммиакаNH3.
Слайд 25Валентность атома азота – III, его пять электронов внешнего уровня занимают четыре

орбитали, значит, тип гибридизации – sp3, но только три орбитали принимают участие в образовании химической связи. Тетраэдр без одной вершины превращается в пирамиду. Поэтому у молекулы аммиака форма молекулы пирамидальная, угол связи искажается до 107°30′.
Слайд 26кислород в молекуле воды находится в sp3 гибридном состоянии, а форма молекулы - угловая,

угол связи составляет 104°27′.
























 Принципиальные электро-схема (6 класс)
Принципиальные электро-схема (6 класс) Физика ЕГЭ. Разбор диагностического тестирования (Занятие 1)
Физика ЕГЭ. Разбор диагностического тестирования (Занятие 1) Силовая электроника
Силовая электроника Что такое кипение
Что такое кипение Разработка машины для корчевания пней
Разработка машины для корчевания пней Презентация по физике "Давление и сила давления" -
Презентация по физике "Давление и сила давления" -  Тематический состав ВсОШ по физике для 11ого класса
Тематический состав ВсОШ по физике для 11ого класса Резьбовые соединения. Контроль крепежа
Резьбовые соединения. Контроль крепежа Экспериментальные методы регистрации заряженных частиц
Экспериментальные методы регистрации заряженных частиц Источники электрического тока
Источники электрического тока Презентация на тему Закон Архимеда
Презентация на тему Закон Архимеда  Атомы каждого химического элемента
Атомы каждого химического элемента Методы расчетов резисторных схем постоянного тока.11 класс
Методы расчетов резисторных схем постоянного тока.11 класс Электротехника и электроника. Анализ и расчет переходных процессов в электрических цепях
Электротехника и электроника. Анализ и расчет переходных процессов в электрических цепях Источники света. Прямолинейное распространение света
Источники света. Прямолинейное распространение света Внутренняя энергия и работа
Внутренняя энергия и работа Магнитное поле
Магнитное поле Физика космоса кружок
Физика космоса кружок Построение эвольвентного профиля зуба
Построение эвольвентного профиля зуба Физика и познание мира
Физика и познание мира Розв'язування задач на тему Закони вiдбивання свiтла
Розв'язування задач на тему Закони вiдбивання свiтла Задача: расчет процесса водяного пара
Задача: расчет процесса водяного пара Потенциальная энергия заряженного тела в однородном электростатическом поле
Потенциальная энергия заряженного тела в однородном электростатическом поле Технологические характеристики грунтов. Определение трудности процессов разработки горных пород
Технологические характеристики грунтов. Определение трудности процессов разработки горных пород Радиальное биение
Радиальное биение Полное внутреннее отражение
Полное внутреннее отражение Презентация на тему Ультрафиолетовые лучи
Презентация на тему Ультрафиолетовые лучи  Между двумя точечными заряженными телами сила электрического взаимодействия
Между двумя точечными заряженными телами сила электрического взаимодействия