Содержание
- 2. У гомогенному випадку фазовий перехід - це перехід від однофазного стану, в якому взагалі не існує
- 3. Слід пам'ятати, що паралельно з процесом фазового переходу - плавлення-кристалізації йде незалежний процес затвердіння-розрідження, який не
- 4. Повторення основ фізичної хімії
- 5. Рівноважна температура переходу при постійному тиску з твердого в рідкий стан T∞ в рівноважній термодинамічній системі
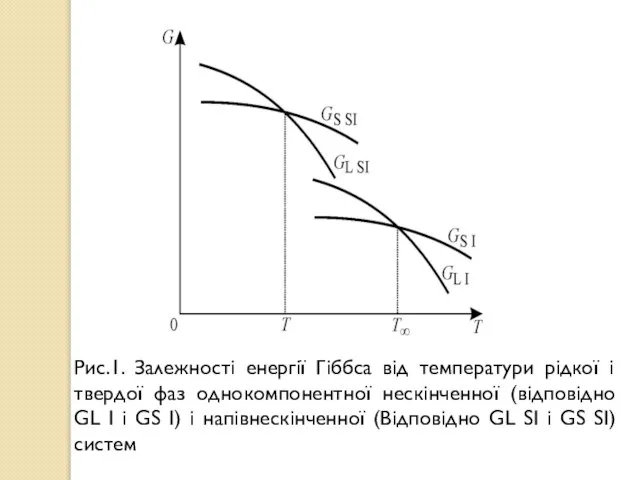
- 6. Рис.1. Залежності енергії Гіббса від температури рідкої і твердої фаз однокомпонентної нескінченної (відповідно GL I і
- 7. (4) Поява додаткових доданків в рівності (4) у порівнянні з (2) приводить до збільшення значення потенціалу
- 8. (7) Приймається допущення, що теплота плавлення також не залежить від температури, при якій відбувається фазовий перехід.
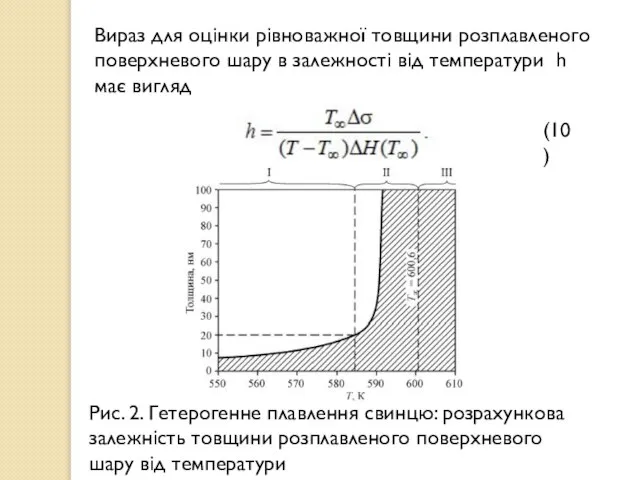
- 9. Вираз для оцінки рівноважної товщини розплавленого поверхневого шару в залежності від температури h має вигляд (10)
- 10. Висновки 1) наявність поверхні в напівнескінченній системі, і, як наслідок, виникнення явища плавлення, викликаного цією поверхнею,
- 11. 2. Залежність температури плавлення нанорозмірних систем від їх розмірів Для систем розмірами (діаметром нанокристалів, товщиною тонкої
- 12. Нанорозмірні системи можна умовно розділити на дві групи: 1) Системи, в яких немає можливості для зміни
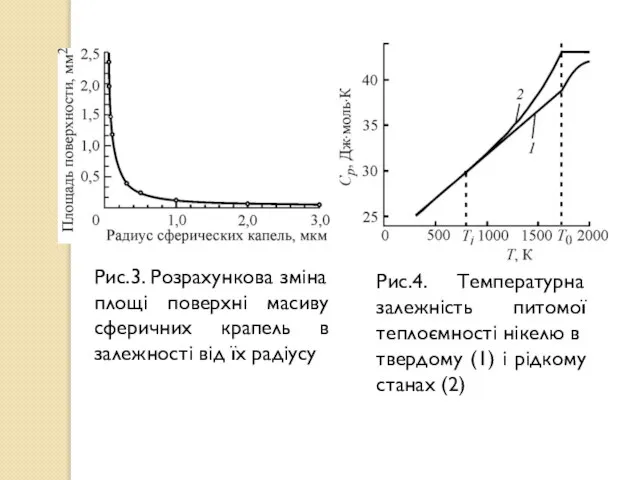
- 13. Рис.3. Розрахункова зміна площі поверхні масиву сферичних крапель в залежності від їх радіусу Рис.4. Температурна залежність
- 14. 3. Залежність температури плавлення нанорозмірних систем від їх розмірів без зміни форми 3.1. Нанокристали, нанокластери у
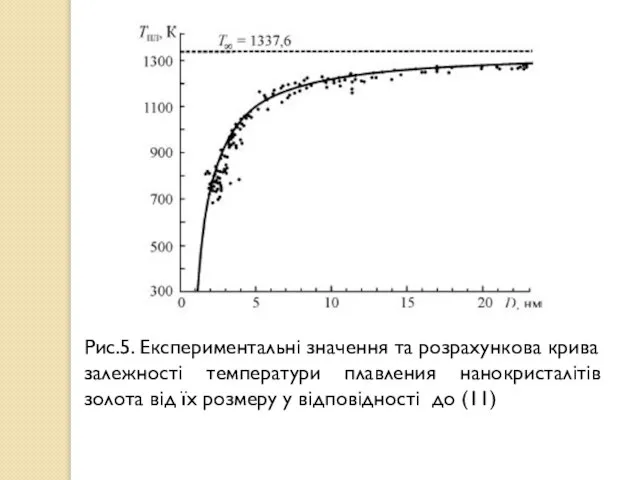
- 15. Рис.5. Експериментальні значення та розрахункова крива залежності температури плавления нанокристалітів золота від їх розмеру у відповідності
- 16. 3.2 Нитьовидні нанокристали, оточені іншим твердим розчином Рис. 6. Нитьовидні нанокристали індію у матриці пористого анодного
- 18. Скачать презентацию











 Задачи на динамику
Задачи на динамику Проводники и диэлектрики в электрическом поле
Проводники и диэлектрики в электрическом поле В мире звуков
В мире звуков Переменный ток
Переменный ток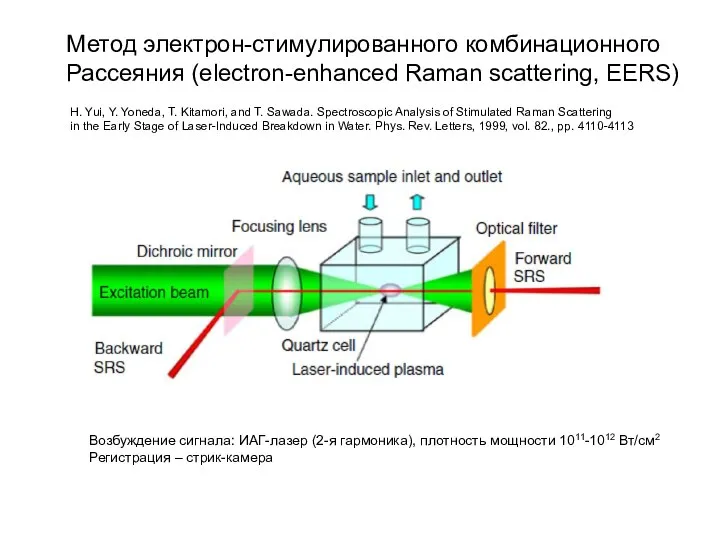 Метод электрон-стимулированного комбинационного Рассеяния (electron-enhanced Raman scattering, EERS)
Метод электрон-стимулированного комбинационного Рассеяния (electron-enhanced Raman scattering, EERS) Презентация на тему Испарение и конденсация
Презентация на тему Испарение и конденсация  ԱՎԱՐՏԱԿԱՆ ԱՇԽԱՏԱՆՔ ՄԱՍՆԱԳԻՏՈՒԹՅՈՒՆ` ՀԱՄԱԿԱՐԳՉԱՅԻՆ ԳԵՂԱՐՎԵՍՏԱԿԱՆ ՆԱԽԱԳԾՈՒՄ
ԱՎԱՐՏԱԿԱՆ ԱՇԽԱՏԱՆՔ ՄԱՍՆԱԳԻՏՈՒԹՅՈՒՆ` ՀԱՄԱԿԱՐԳՉԱՅԻՆ ԳԵՂԱՐՎԵՍՏԱԿԱՆ ՆԱԽԱԳԾՈՒՄ Радуга
Радуга Приспособления малой механизации
Приспособления малой механизации Устройство ракет Циолковского
Устройство ракет Циолковского Откуда приходит электричество?
Откуда приходит электричество? Теоретические основы электротехники. Трехфазные электрические цепи
Теоретические основы электротехники. Трехфазные электрические цепи Плоское движение капсулы в атмосфере
Плоское движение капсулы в атмосфере Металлоискатель по принципу прием-передача
Металлоискатель по принципу прием-передача Точка росы
Точка росы Понятия о машине и механизме
Понятия о машине и механизме Производство, передача и использование электрической энергии
Производство, передача и использование электрической энергии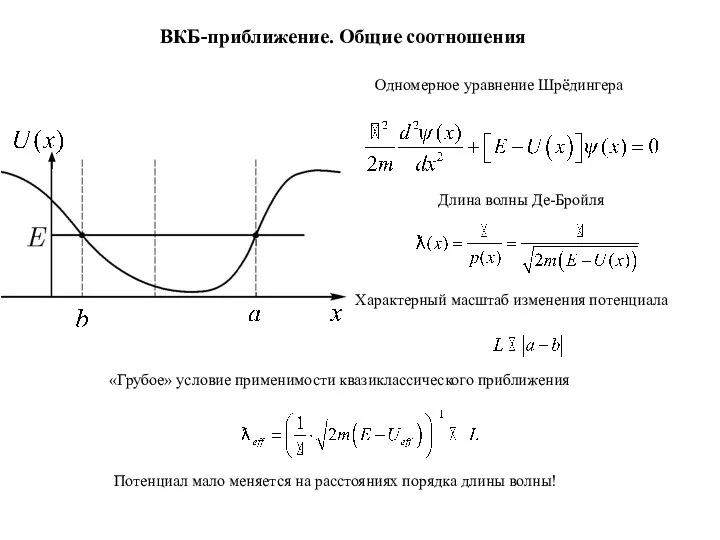 ВКБ-приближение. Общие соотношения
ВКБ-приближение. Общие соотношения Диффузия в газах, жидкостях и твердых телах
Диффузия в газах, жидкостях и твердых телах АЭС с реакторами на быстрых нейтронах с натриевым теплоносителем. Белоярская АЭС с реактором БН-600
АЭС с реакторами на быстрых нейтронах с натриевым теплоносителем. Белоярская АЭС с реактором БН-600 Колебания. Колебательные системы
Колебания. Колебательные системы Электрическое сопротивление
Электрическое сопротивление Алгоритмизация информации на уроках физики
Алгоритмизация информации на уроках физики Уход за швейной машиной. Создание изделий из текстильных материалов
Уход за швейной машиной. Создание изделий из текстильных материалов Графическое представление прямолинейного равномерного движения
Графическое представление прямолинейного равномерного движения Презентация на тему КПД тепловых двигателей (8 класс)
Презентация на тему КПД тепловых двигателей (8 класс)  Разработка инструментария для решения задачи вычислительной гидродинамики при моделировании воздушных потоков
Разработка инструментария для решения задачи вычислительной гидродинамики при моделировании воздушных потоков Динер Никита Физика Инерция
Динер Никита Физика Инерция