Слайд 2Лекция №5
КЛАССИФИКАЦИИ РАСТВОРОВ.
СПОСОБЫ ВЫРАЖЕНИЯ
КОНЦЕНТРАЦИИ
Дисциплина: «Физико- химические методы исследований и техника

лабораторных работ»
1 курс 2 семестр
Слайд 31. Классификации растворов
РАСТВОРЫ- гомогенные системы, содержащие не менее двух веществ.
Виды растворов:
-

растворы твердых, жидких и газообразных веществ в жидких растворителях
- однородные смеси твердых, жидких и газообразных веществ.
Растворитель- это вещество, взятое в избытке и в том же агрегатном состоянии, что и сам раствор,
Растворенное вещество- компонент раствора, взятый в недостатке.
Слайд 4В зависимости от агрегатного состояния растворителя:
- газообразные- воздух и другие смеси газов
-

жидкие- гомогенные смеси газов, жидкостей и твердых тел с жидкостями.
- твердые растворы- сплавы, например, металлов друг с другом, стёкла.
Наибольшее значение имеют жидкие смеси, в кото-рых растворитель- жидкость.
Часто применяемые растворители:
- из неорганических веществ- вода,
- из органических веществ- метанол, этанол, ацетон и др.
Слайд 5Способность к образованию растворов у разных веществ выражена в различной степени.
Одни

вещества способны смешиваться друг с другом в любых количествах (например, вода и спирт), другие - в ограниченных (например, хлорид натрия и вода).
Слайд 6Принцип процесса образования раствора.
При внесении в растворитель твердого вещества (например, поваренной соли),

частицы ионов (Na+ и Cl), находящиеся на поверхности, в результате колебательного движения, отрываются и переходят в растворитель.
Этот процесс распространяется на следующие слои частиц, которые обнажаются в кристалле после удаления поверхностного слоя.
Так, постепенно, частицы, образующие кристалл (ионы или молекулы), переходят в раствор.
Слайд 7Частицы, перешедшие в раствор, вследствие диффузии распределяются по всему объему растворителя.
По

мере увеличения концентрации частицы, находящиеся в непрерывном движении, при столкновении с твердой поверхностью еще не растворившегося вещества могут задерживаться на ней, т.е. растворение всегда сопровождается обратным явлением- кристаллизацией.
Может наступить такой момент, когда одновременно выделяется из раствора столько же частиц (ионов, молекул), сколько их переходит в раствор- наступает равновесие.
Слайд 8По соотношению преобладания числа частиц, переходящих в раствор или удаляющихся из раствора,

различают:
- насыщенные растворы- находящийся в равновесии с растворяемым веществом, т.е. данное вещество при данной температуре в них больше не растворяется и раствор содержит максимально возможное (для данных условий) количество растворенного вещества;
- ненасыщенные растворы- в которых еще можно растворить добавочное количество данного вещества
Слайд 9- пересыщенные растворы, содержат растворенного вещества больше, чем его должно быть в

данных условиях в насыщенном растворе.
Это неустойчивые, неравновесные системы, в которых наблюдается самопроизвольный переход в равновесное состояние (выделяется избыток растворенного вещества, и раствор становится насыщенным)
Слайд 10В зависимости от того, электронейтральными или заряженными частицами являются компоненты раствора, их

подразделяют на:
- молекулярные- растворы неэлектролитов
- ионные- растворы электролитов, проводящие электрический ток.
Слайд 113. Способы выражения концентрации растворов
Каждый раствор характеризуется концентрацией, т.е. количеством (или массой)

вещества, содержащегося в определенном объеме раствора.
Растворы с большой концентрацией растворенного вещества называют концентрированными, с малой– разбавленными.
Слайд 12Содержание растворенного вещества в растворе может быть выражено:
1. Процентная концентрация- количество граммов

вещества, находящегося в 100 г раствора.
Например:
5% раствор содержит 5 г вещества в 100 г раствора (берут 5 г вещества и 100- 5= 95 г растворителя)
Слайд 132. Молярная концентрация показывает число молей растворенного вещества, содержащихся в 1л раствора:
-

двумолярный раствор (2М) содержит 2 моль/л,
- одномолярный (1 М)- 1 моль/л;
- децимолярный (0,1 М)- 0,1моль/л,
- сантимолярный (0,01 М)- 0,01 моль/л и т.д.
Слайд 143. Нормальная (эквивалентная) концентрация- нормальность- показывает число эквивалентов растворенного вещества в 1

л раствора.
Эквивалент- количество элемента, которое соединяется с одним атомом водорода и замещает его в химических реакциях.
Так, эквивалент хлора в соединении HCI равен 1 (1моль), в соединении H2S эквивалент серы будет равен ½ моль
Эквивалент цинка для реакции:
Zn+ 2HCI= ZnCI2+H2↑, равен ½ моль
Слайд 15Эквивалент сложного соединения- такое его количество, которое в данной реакции соответствует (эквивалентно)

одному атому водорода.
Так для реакции Zn+ H2SО4 = ZnSО4+H2↑, 1 моль H2SО4 соответствует 2 атомам водорода, следовательно её эквивалент равен ½ моль.
Масса одного эквивалента элемента или соединения называется его эквивалентной массой.














 Научное открытие России: Гравитационные волны
Научное открытие России: Гравитационные волны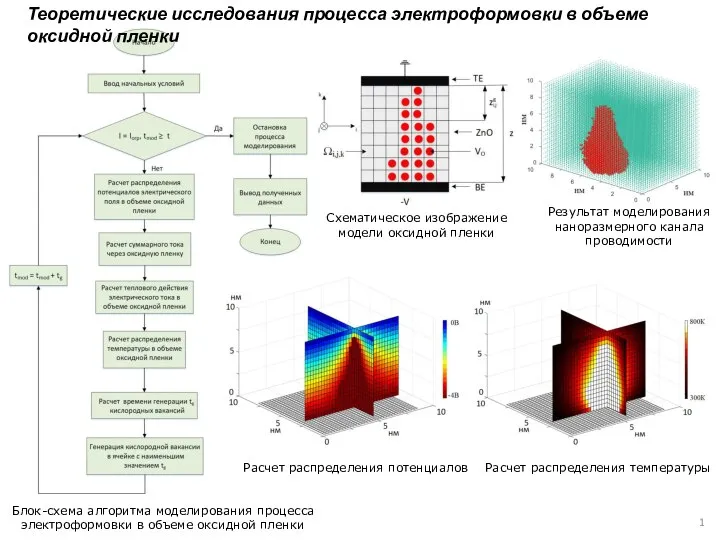 Модель исследования процесса электроформовки в объеме оксидной пленки
Модель исследования процесса электроформовки в объеме оксидной пленки Фотометрия Бугера, Ламберта, Бера
Фотометрия Бугера, Ламберта, Бера Деформированное состояние в точке. Обобщенный закон Гука. Лекция 10
Деформированное состояние в точке. Обобщенный закон Гука. Лекция 10 Презентация на тему Паровые машины
Презентация на тему Паровые машины  Электромагнитные колебания
Электромагнитные колебания Принципы действия различных типов двигателей. Двигатели внешнего сгорания
Принципы действия различных типов двигателей. Двигатели внешнего сгорания Техническое состояние трансмиссии автомобилей
Техническое состояние трансмиссии автомобилей Чувствительность взрывчатых систем к внешним воздействиям
Чувствительность взрывчатых систем к внешним воздействиям Закон сохранения механической энергии
Закон сохранения механической энергии Нефтегазовая и рудная геофизика. Сейсмические методы при изучении строения земной коры
Нефтегазовая и рудная геофизика. Сейсмические методы при изучении строения земной коры Реологиялық әдістер. Кернеу және пішін өзгерісі
Реологиялық әдістер. Кернеу және пішін өзгерісі Радиоволны. История открытия
Радиоволны. История открытия Выдающиеся физики
Выдающиеся физики Ядерная геофизика
Ядерная геофизика Визуальный и измерительный метод неразрушающего контроля. Электронный учебный курс
Визуальный и измерительный метод неразрушающего контроля. Электронный учебный курс Кинематика твердого тела/ Простейшие движения твердого тела
Кинематика твердого тела/ Простейшие движения твердого тела Сила трения. Сила упругости
Сила трения. Сила упругости Становление физиологии. Ятрофизика, ятромеханика
Становление физиологии. Ятрофизика, ятромеханика 840842
840842 Ангармонизм, упругость
Ангармонизм, упругость Взаимные превращения жидкостей и газов
Взаимные превращения жидкостей и газов Диадинамические токи
Диадинамические токи Презентация на тему Взаимодействие частиц вещества
Презентация на тему Взаимодействие частиц вещества  Выпускная бакалаврская работа Повышение безопасности труда при ремонте сельскохозяйственной техники
Выпускная бакалаврская работа Повышение безопасности труда при ремонте сельскохозяйственной техники Особенности эксплуатации оборудования для ТО и ТР колес и шин (урок 20-23)
Особенности эксплуатации оборудования для ТО и ТР колес и шин (урок 20-23) Блоки. Простые механизмы
Блоки. Простые механизмы Определение толщины зуба на любом радиусе
Определение толщины зуба на любом радиусе