Содержание
- 2. Основные понятия Термодинамика – это раздел физики, изучающий общие закономерности обмена тепловой энергии между системами, системой
- 3. Основные параметры состояния вещества Температура тел - определяет направление возможного самопроизвольного перехода тепла между телами. Температура,
- 4. Давление - представляет собой силу, действующею по нормали к поверхности тела и отнесенную к единице площади
- 5. Плотность – отношение массы вещества к объему занимаемому этим веществом. Удельный объем - величина обратная плотности
- 6. Изопроцессы Уравнение Менделеева – Клапейрона Процессом называется ряд последовательных изменений состояния системы. V = сonst изохорический
- 7. Внутренняя энергия термодинамической системы - кинетическая энергия теплового движения ее молекул и потенциальная энергия их взаимодействия.
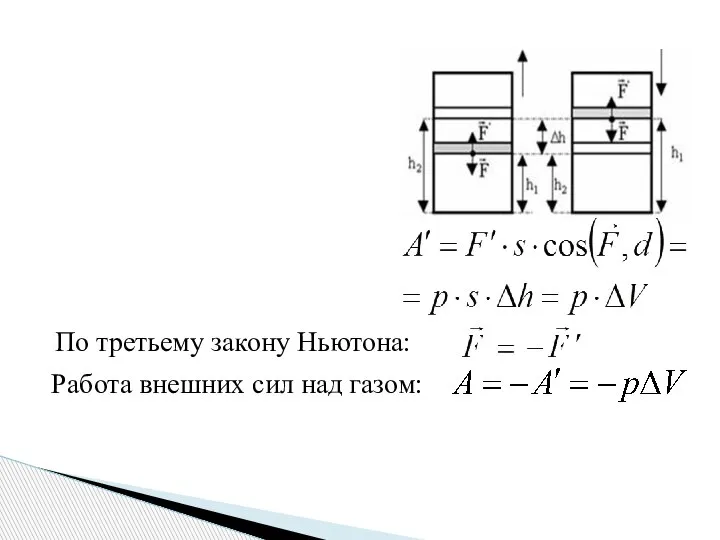
- 8. РАБОТА В ТЕРМОДИНАМИКЕ Если газ расширяется при постоянном давлении р, то сила, действующая со стороны газа
- 9. По третьему закону Ньютона: Работа внешних сил над газом:
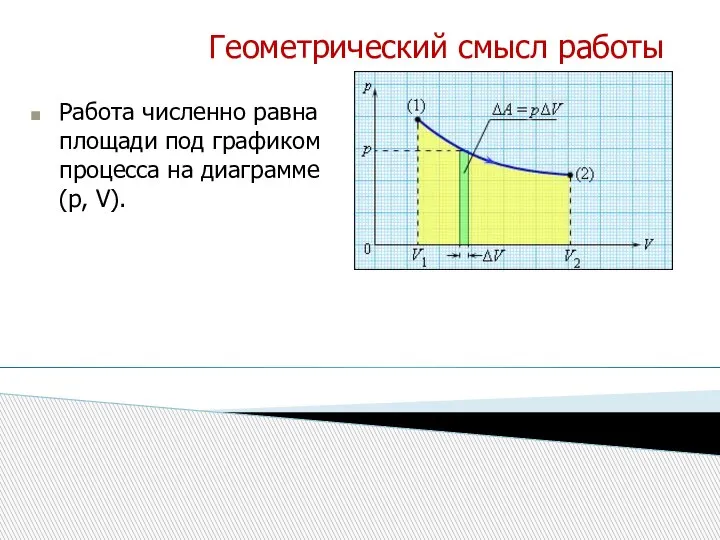
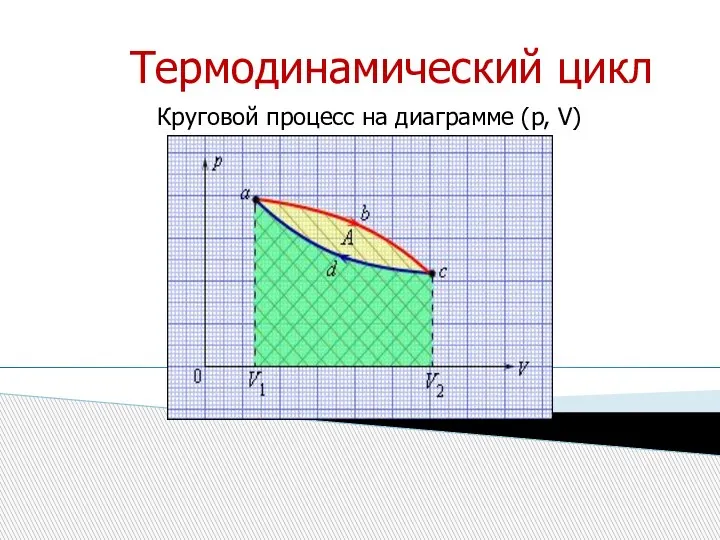
- 10. Геометрический смысл работы Работа численно равна площади под графиком процесса на диаграмме (p, V).
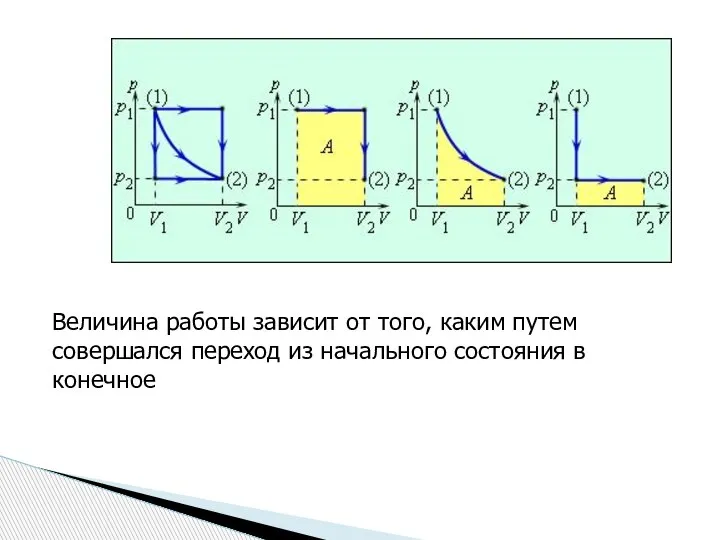
- 11. Величина работы зависит от того, каким путем совершался переход из начального состояния в конечное
- 12. Количество теплоты Q = cm(t02-t01) – нагревание (охлаждение) Q=±λm - плавление (отвердевание) Q = ±Lm -
- 13. Первый закон термодинамики Изменение внутренней энергии системы при переходе ее из одного состояния в другое равно
- 14. Вечный двигатель первого рода - устройство, способное совершать неограниченное количество работы без подведения энергии извне. Из
- 15. Применение первого закона термодинамики к процессам в одноатомных идеальных газах Изотермический процесс (Т = const): Изобарический
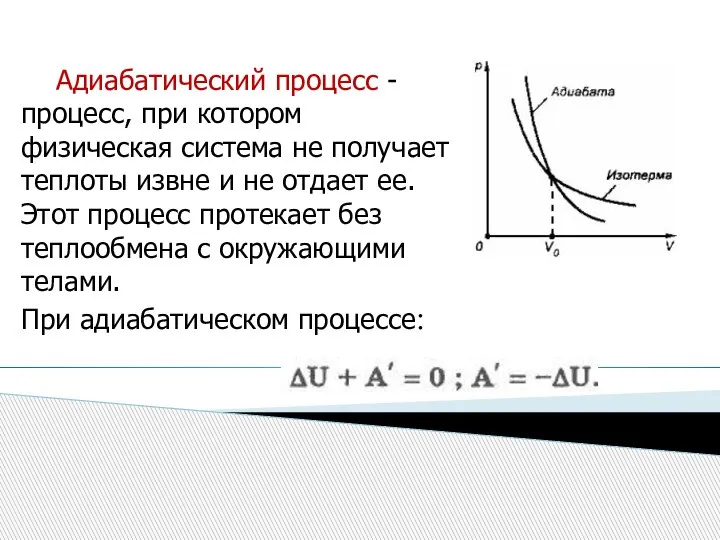
- 16. Адиабатический процесс - процесс, при котором физическая система не получает теплоты извне и не отдает ее.
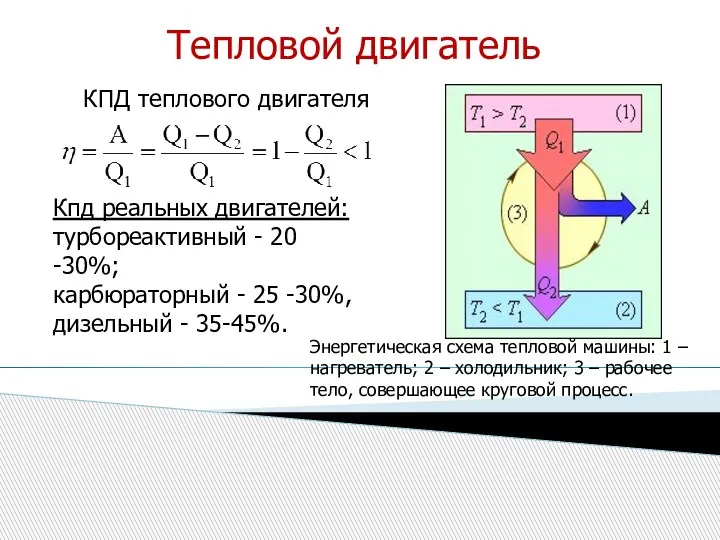
- 17. ТЕПЛОВЫЕ ДВИГАТЕЛИ Тепловые двигатели - устройства, превращающие внутреннюю энергию топлива в механическую энергию. Любой тепловой двигатель
- 18. Термодинамический цикл Круговой процесс на диаграмме (p, V)
- 19. Тепловой двигатель Энергетическая схема тепловой машины: 1 – нагреватель; 2 – холодильник; 3 – рабочее тело,
- 20. Идеальная тепловая машина Машина работает на идеальном газе. 1 - 2 - при тепловом контакте с
- 21. Теорема Карно: кпд реальной тепловой машины не может быть больше кпд идеальной машины, работающей в том
- 22. Второй закон термодинамики Второй з-н термодинамики указывает направление возможных энергетических превращений и тем самым выражает необратимость
- 23. Формулировка У. Кельвина: невозможно осуществить такой периодический процесс, единственным результатом которого было бы получение работы за
- 25. Скачать презентацию
















 Презентация на тему Трансформаторы (11 класс)
Презентация на тему Трансформаторы (11 класс)  Механическая работа. Единицы работы
Механическая работа. Единицы работы Расчёт режимов разомкнутых сетей
Расчёт режимов разомкнутых сетей Теплотехнология. Приемники энергии
Теплотехнология. Приемники энергии Презентация на тему Физика в картинках
Презентация на тему Физика в картинках  Электрическая емкость
Электрическая емкость Физические явления и интересные факты
Физические явления и интересные факты Презентация на тему Закон Паскаля
Презентация на тему Закон Паскаля 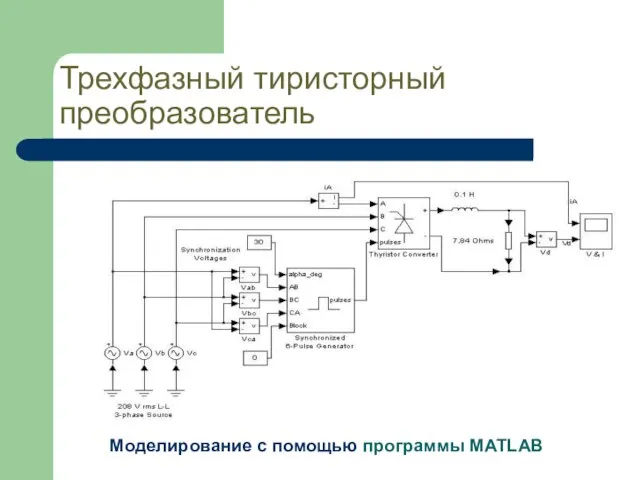 Презентация на тему Трехфазный тиристорный преобразователь
Презентация на тему Трехфазный тиристорный преобразователь  Электромагнитные колебания
Электромагнитные колебания Интенсивность звука в идеальной жидкости
Интенсивность звука в идеальной жидкости Закон Ома для участка цепи
Закон Ома для участка цепи Презентация на тему Люминесцентный анализ
Презентация на тему Люминесцентный анализ  Теплоносители и их свойства. Местная вентиляция и кондиционирование воздуха. (Тема 14)
Теплоносители и их свойства. Местная вентиляция и кондиционирование воздуха. (Тема 14) Основные положения теплопроводности
Основные положения теплопроводности Расчет силы тока и напряжения в электрических цепях
Расчет силы тока и напряжения в электрических цепях Физическая оптика: интерференция и дифракция. Лекция 2
Физическая оптика: интерференция и дифракция. Лекция 2 Окружающие нас тела называются физическими телами. Строение вещества. Молекула
Окружающие нас тела называются физическими телами. Строение вещества. Молекула Материалы, применяемые в машиностроении. II часть
Материалы, применяемые в машиностроении. II часть Гидродинамика. Движение жидкости
Гидродинамика. Движение жидкости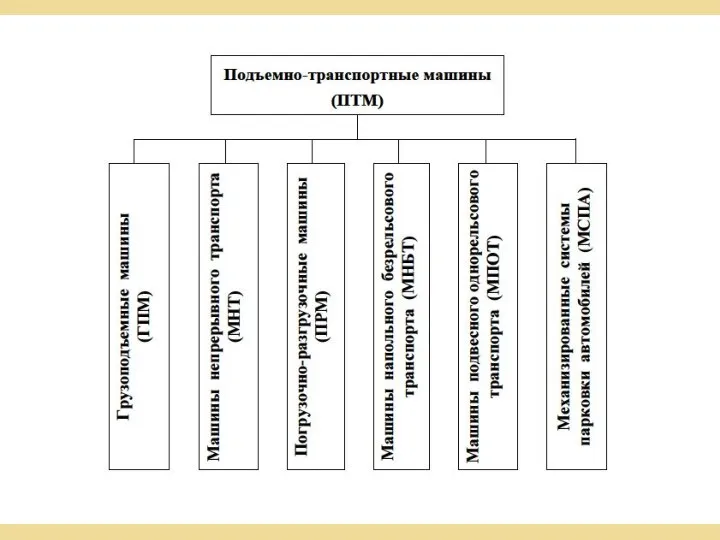 Классификация подъемно-транспортных машин
Классификация подъемно-транспортных машин Инструкция по сборке стальной рамы Prusa i3 Steel Pro для модификации 3d принтера Anet A6
Инструкция по сборке стальной рамы Prusa i3 Steel Pro для модификации 3d принтера Anet A6 Что такое мощность
Что такое мощность Электрическое напряжение. Вольтметр. Измерение напряжения
Электрическое напряжение. Вольтметр. Измерение напряжения Физические задачи с литературным содержанием
Физические задачи с литературным содержанием Разбор выполнения заданий
Разбор выполнения заданий Идеальный газ
Идеальный газ Теплопроводность через плоскую и цилиндрическую стенки при граничных условиях третьего рода (теплопередача)
Теплопроводность через плоскую и цилиндрическую стенки при граничных условиях третьего рода (теплопередача)