Содержание
- 2. 1. внутренняя энергия зависит от температуры. 2. газ может совершать работу при любых процессах. 3.при изотермическом
- 3. Uk = U0 +A +Q Внутренняя энергия U = 3/2 v*R*T Работа в термодинамике А =
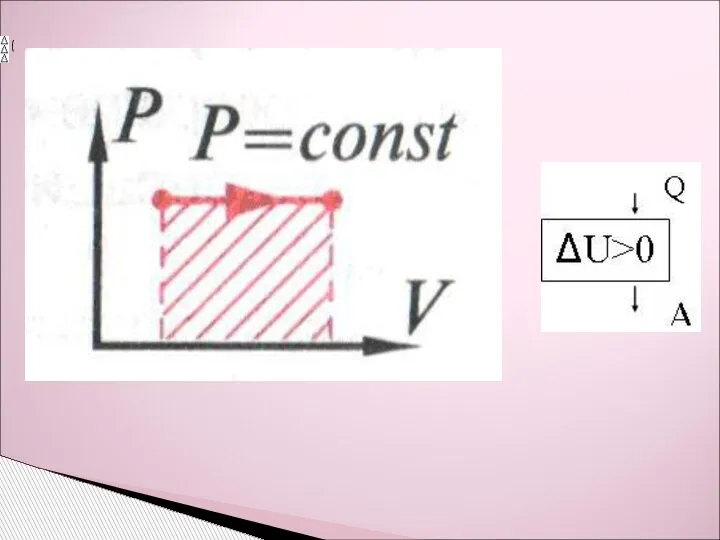
- 4. Изотермический Q = A . Изохорный Q = U2 –U1 изобарический ? изопроцессы
- 5. 1. как изменяется внутренняя энергия системы? 2. какую работу она совершает? 3. получает или отдает система
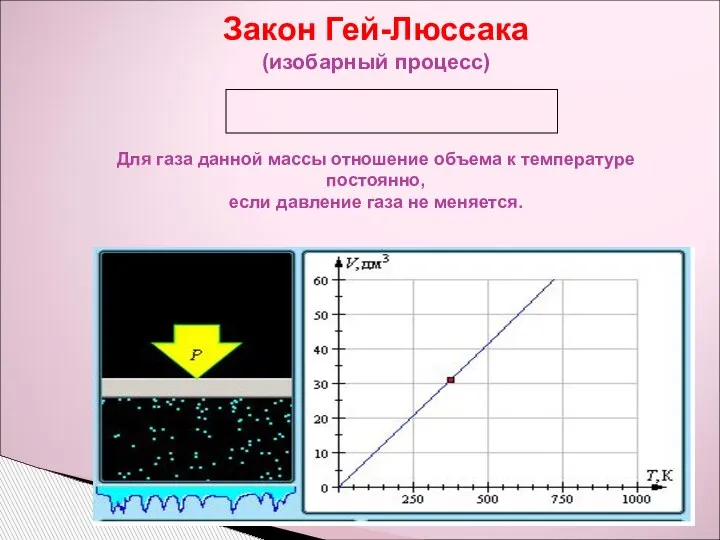
- 6. Закон Гей-Люссака (изобарный процесс) Для газа данной массы отношение объема к температуре постоянно, если давление газа
- 7. (
- 9. Скачать презентацию




 Испарение и конденсация. Насыщенный и ненасыщенный пар
Испарение и конденсация. Насыщенный и ненасыщенный пар Обледенение летательных аппаратов
Обледенение летательных аппаратов Кең ауқымды вибратор
Кең ауқымды вибратор 840842
840842 Презентация на тему Архимед
Презентация на тему Архимед  Бипризма Френеля
Бипризма Френеля ШВЕЙНАЯ МАШИНА
ШВЕЙНАЯ МАШИНА Давление в физике
Давление в физике Переменный электрический ток
Переменный электрический ток Виды подшипников
Виды подшипников Тайны мыльных пузырей
Тайны мыльных пузырей Изучение закона сохранения энергии. Лабораторная работа
Изучение закона сохранения энергии. Лабораторная работа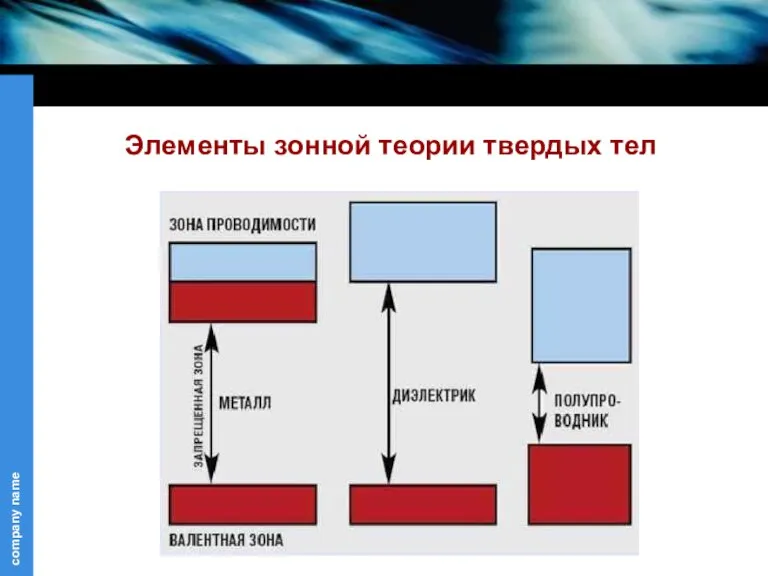 Элементы зонной теории твердых тел. Лекция 12
Элементы зонной теории твердых тел. Лекция 12 Электродинамика. Электрическое поле. Магнитное поле
Электродинамика. Электрическое поле. Магнитное поле Трение несмазанных поверхностей. Силовое взаимодействие
Трение несмазанных поверхностей. Силовое взаимодействие Бизнес идея: Практичный домкрат для автомобилей
Бизнес идея: Практичный домкрат для автомобилей Тормоза грузовых и пассажирских вагонов
Тормоза грузовых и пассажирских вагонов lektsia
lektsia Естествознание как источник развития техники
Естествознание как источник развития техники Лабораторная работа Определение положения центра тяжести плоской фигуры
Лабораторная работа Определение положения центра тяжести плоской фигуры Первый в мире паровой поезд когда и кем был изобретен
Первый в мире паровой поезд когда и кем был изобретен Макромир
Макромир Криволинейное движение тела.Тест
Криволинейное движение тела.Тест Электроэнергия. Гидроэлектростанция. Линия электропередач. Электролампа
Электроэнергия. Гидроэлектростанция. Линия электропередач. Электролампа Давление. Свойства и сила давления
Давление. Свойства и сила давления Практические занятия
Практические занятия Дефекты машинной строчки (технология, 7 класс)
Дефекты машинной строчки (технология, 7 класс) Кинематика
Кинематика