Содержание
- 2. Радиоактивность 1896 г. – Анри Беккерель 1899 г. – Эрнест Резерфорд А.Беккерель Э.Резерфорд
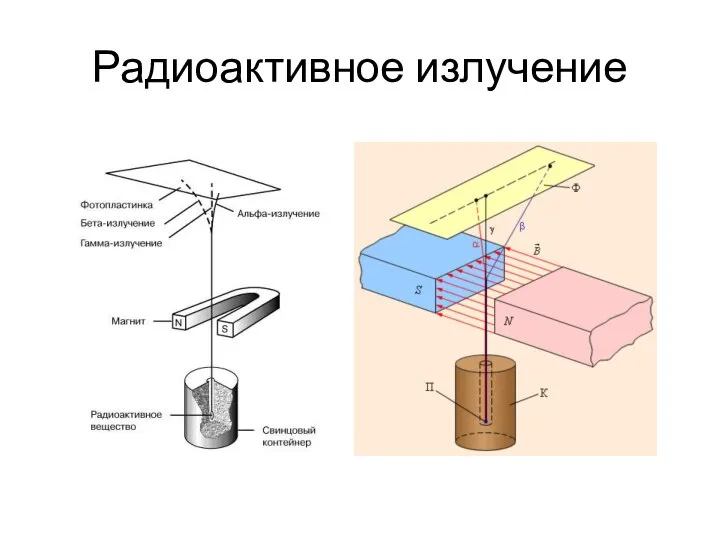
- 3. Радиоактивное излучение
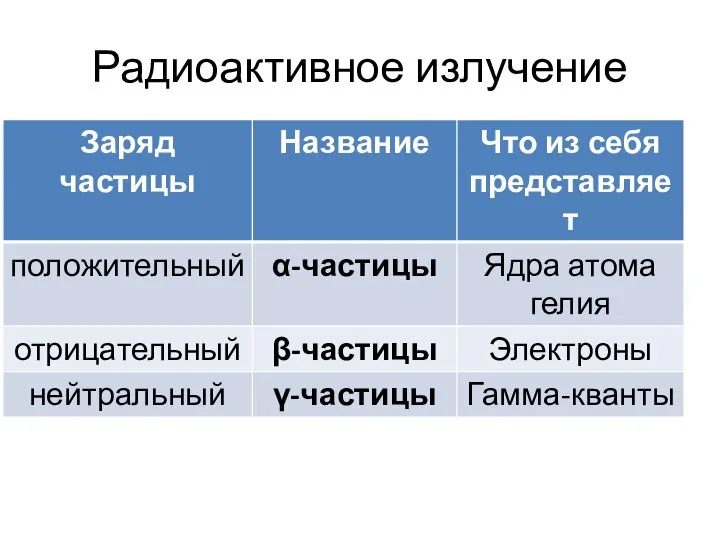
- 4. Радиоактивное излучение
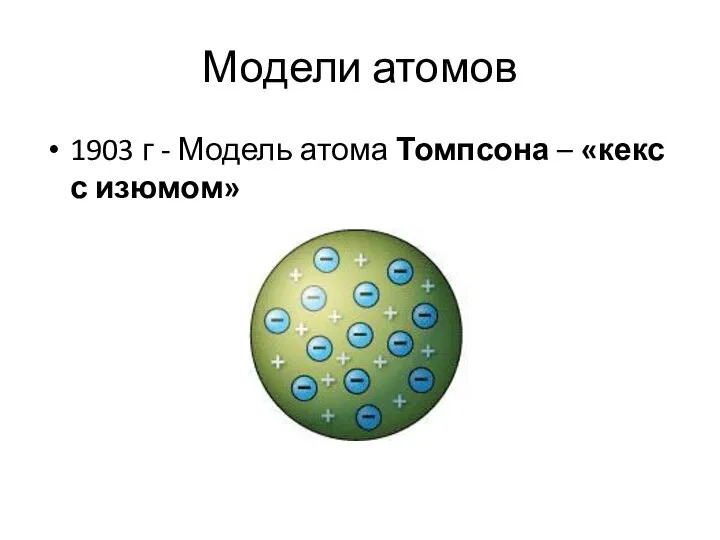
- 5. Модели атомов 1903 г - Модель атома Томпсона – «кекс с изюмом»
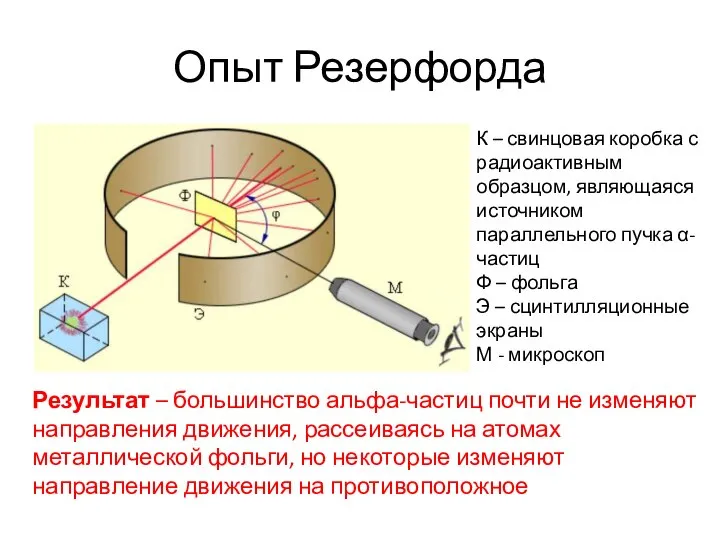
- 6. Опыт Резерфорда К – свинцовая коробка с радиоактивным образцом, являющаяся источником параллельного пучка α-частиц Ф –
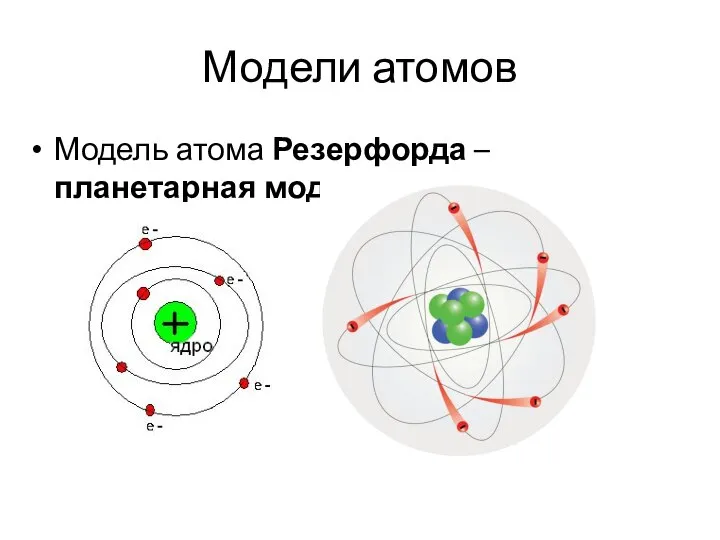
- 7. Модели атомов Модель атома Резерфорда – планетарная модель
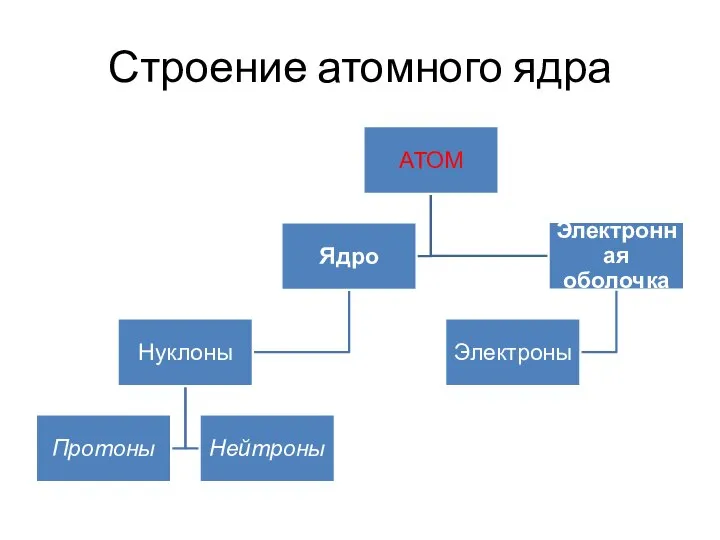
- 8. Строение атомного ядра
- 9. Изотопы Атомы одного и того же химического элемента, отличающиеся друг от друга массовым числом, т.е. числом
- 11. Скачать презентацию


 Работа при повороте тела. Кинетическая энергия вращающегося твердого тела
Работа при повороте тела. Кинетическая энергия вращающегося твердого тела Опыт Эрнеста Резерфорда 1871 - 1937
Опыт Эрнеста Резерфорда 1871 - 1937 Работа газа и пара при расширении. Тепловые двигатели
Работа газа и пара при расширении. Тепловые двигатели Детали машин и основы конструирования. Конструкционные материалы. (Лекция 3)
Детали машин и основы конструирования. Конструкционные материалы. (Лекция 3)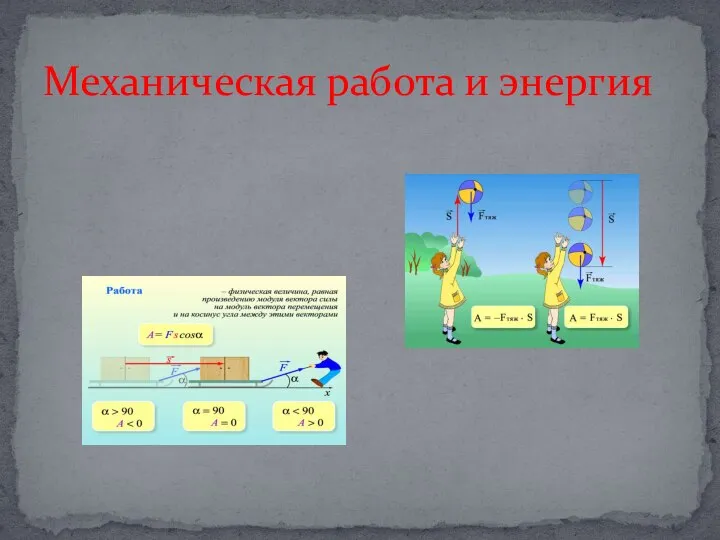 Механическая работа и энергия
Механическая работа и энергия Энергия связи. Дефект масс
Энергия связи. Дефект масс Методы измерения потерь в оптических волокнах
Методы измерения потерь в оптических волокнах Архимед көче
Архимед көче Физика и техника
Физика и техника Электризация тел
Электризация тел Изгиб. Основные понятия. Классификация видов изгибов
Изгиб. Основные понятия. Классификация видов изгибов Электропроводность полупроводников
Электропроводность полупроводников Электрическое сопротивление
Электрическое сопротивление Гальваномагнитные эффекты
Гальваномагнитные эффекты Эксплуатация РЛС и НРЗ
Эксплуатация РЛС и НРЗ Большой адронный коллайдер
Большой адронный коллайдер Ускорение свободного падения на Земле и других небесных телах
Ускорение свободного падения на Земле и других небесных телах Бесконтактный нейтрализатор статических электрических зарядов
Бесконтактный нейтрализатор статических электрических зарядов Мощность. Единицы мощности
Мощность. Единицы мощности Квантовая радиофизика
Квантовая радиофизика Плотность
Плотность Методическая разработка по применению первого закона термодинамики к решению графических задач
Методическая разработка по применению первого закона термодинамики к решению графических задач Использование видеоматериалов на уроках физики как способ повышения самоэффективности личности школьника
Использование видеоматериалов на уроках физики как способ повышения самоэффективности личности школьника Взаимодействие тел
Взаимодействие тел Условия, при которых тело плавает и при которых тонет
Условия, при которых тело плавает и при которых тонет Электромагнитная индукция. Закон электромагнитной индукции. Индуктивность. Энергия магнитного поля катушки с током
Электромагнитная индукция. Закон электромагнитной индукции. Индуктивность. Энергия магнитного поля катушки с током Усилитель звуковой частоты
Усилитель звуковой частоты Измерение давления
Измерение давления