Содержание
- 2. Ян Баптист ван Гельмонт 12 января 1580, Брюссель, Брюссель — 30 декабря 1644, Вилворде, Вилворде, Бельгия)
- 3. Дмитрий Иванович Менделеев (27 января (8 февраля) 1834, Тобольск — 20 января (2 февраля) 1907, Санкт-Петербург)
- 4. Бенуа́ Поль Эми́ль Клапейро́н (26 февраля 1799, Париж — 28 января 1864 Париж) — французский физик
- 5. Уравнение Менделеева-Клапейрона . .
- 6. Нормальные условия Давление р=760мм.рт.ст.=1атм=105Па Температура t=00С (Т=273,150К) 1 моль=22,4 л 1мм.рт.ст.=133 Па
- 7. Задача 1. Рассчитайте массу и объем сернистого газа SO2 количеством вещества 0,8 моль.
- 8. Дано: n(SO2)=0,8 моль Найти: m-?,V-? Решение: M(SO2)=32+2*16=64г/моль; m=n*M ; m=0.8 моль*64г/моль = 51,2г V=n*Vm; V= 0.8
- 9. Задача 2. При температуре 170С и давлении 780 мм.рт.ст. масса газа равна 1,56 г занимает объем
- 10. Дано: t = 170C +273 = 2900K P=780 мм.рт.ст.* 133,3 = 1,03* 105Па m = 1,56г
- 11. Задача 3. Какой объем дихлорэтана ClCH2CH2Cl получится при смешивании 5л хлора Cl2 и 5л этилена CH2=CH2
- 12. Дано: V(Cl2) =5л; V(CH2=CH2) =5л р = 105Па; Т=2730К Найти: V (ClCH2CH2Cl)-? Решение: Cl2 + CH2=СН2
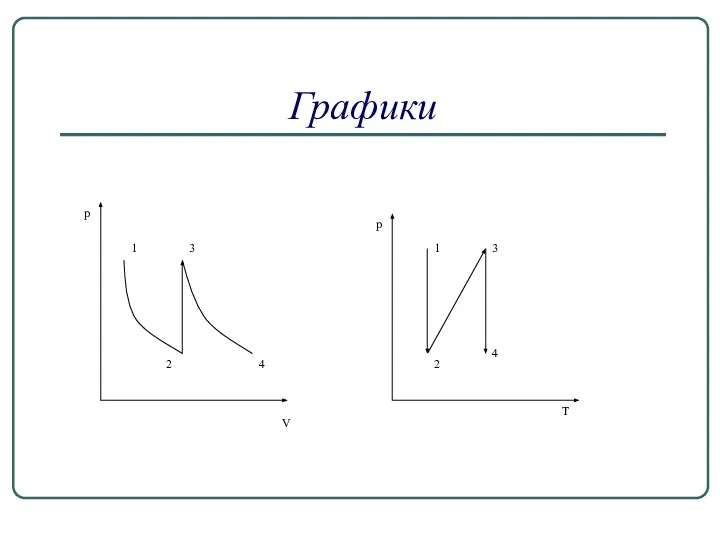
- 13. Задача 4. На рисунке изображены процессы, происходящие с определенной массой идеального газа. Изобразить эти процессы в
- 14. Процесс1-2: T=const, pV=const, при уменьшении p, V увеличивается. Процесс 2-3:V=const, , при увеличении Т, р увеличивается
- 15. Графики
- 16. Домашнее задание
- 18. Скачать презентацию













 Коэффициент полезного действия механизма. Дома: §61 Повторить «золотое правило» механики. Познакомиться с понятием коэффициента полезного действия как основной характеристики рабочего механизма.
Коэффициент полезного действия механизма. Дома: §61 Повторить «золотое правило» механики. Познакомиться с понятием коэффициента полезного действия как основной характеристики рабочего механизма. К решению задач на зарядку конденсатора
К решению задач на зарядку конденсатора Переменный электрический ток
Переменный электрический ток Презентация на тему Момент силы. Применение закона равновесия рычага к блоку
Презентация на тему Момент силы. Применение закона равновесия рычага к блоку  Определение коэффициента поверхностного натяжения синтетических моющих средств
Определение коэффициента поверхностного натяжения синтетических моющих средств Гидротрансформатор
Гидротрансформатор Трехфазный переменный ток. Мощность трехфазной цепи
Трехфазный переменный ток. Мощность трехфазной цепи Поступательное движение
Поступательное движение Телескопны ничек ясарга
Телескопны ничек ясарга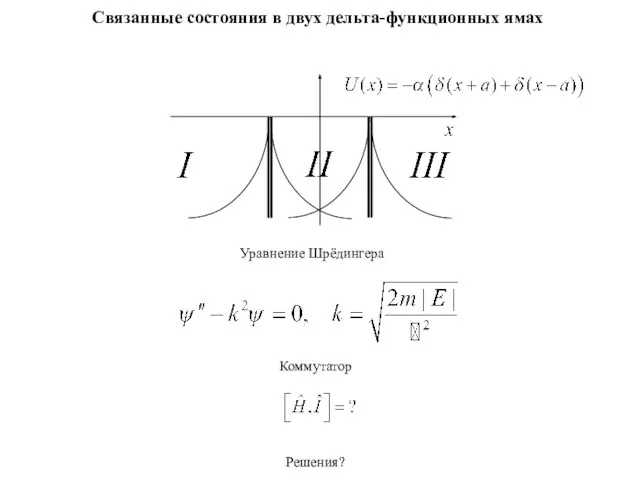 Связанные состояния в двух дельта - функционных ямах
Связанные состояния в двух дельта - функционных ямах Изменение изотопного состава. Выгорание топлива
Изменение изотопного состава. Выгорание топлива Неисправности транспортного средства
Неисправности транспортного средства Газовые законы. Решение тестовых задач. 10 класс
Газовые законы. Решение тестовых задач. 10 класс Действие магнитного поля на проводник с током
Действие магнитного поля на проводник с током Открытия Эйнштейна
Открытия Эйнштейна Safarov_Krasnov
Safarov_Krasnov Переменный ток
Переменный ток Презентация на тему Потенциальная энергия
Презентация на тему Потенциальная энергия  Живой свет свечи
Живой свет свечи Домашнее задание1
Домашнее задание1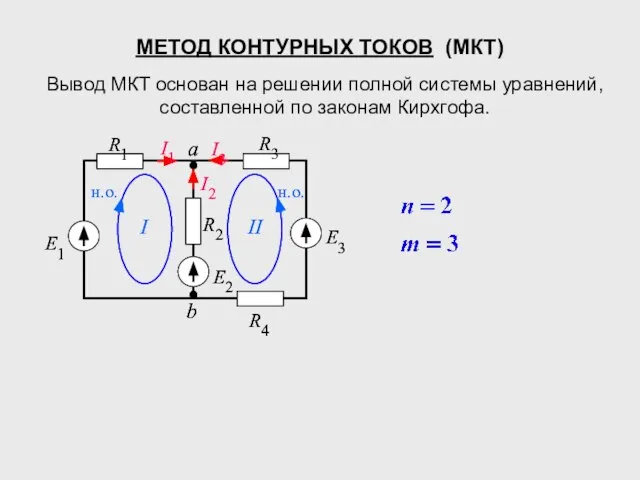 Метод контурных токов (МКТ)
Метод контурных токов (МКТ) Неполадки в швейной машине
Неполадки в швейной машине Движение по окружности. Физика
Движение по окружности. Физика Принципы работы с микроскопом
Принципы работы с микроскопом Рентгеновские лучи
Рентгеновские лучи Презентация на тему Производство и передача электроэнергии
Презентация на тему Производство и передача электроэнергии  Повторение систем карта. Электронный тест
Повторение систем карта. Электронный тест Закон Ома для участка цепи
Закон Ома для участка цепи