Содержание
- 2. Цель: расширить знания учащихся по теме, доказать ядерную модель атома с помощью опытов Резерфорда.
- 3. Актуализация знаний Что вам известно о строении вещества? Как мы узнаем о строении вещества? Каково строение
- 4. Гипотеза о том, что вещества состоят из большого числа атомов, зародилась свыше двух тысячелетий назад. Позиция
- 5. Конкретные представления о строении атома развивались по мере накопления физикой фактов о свойствах вещества. 1897 г
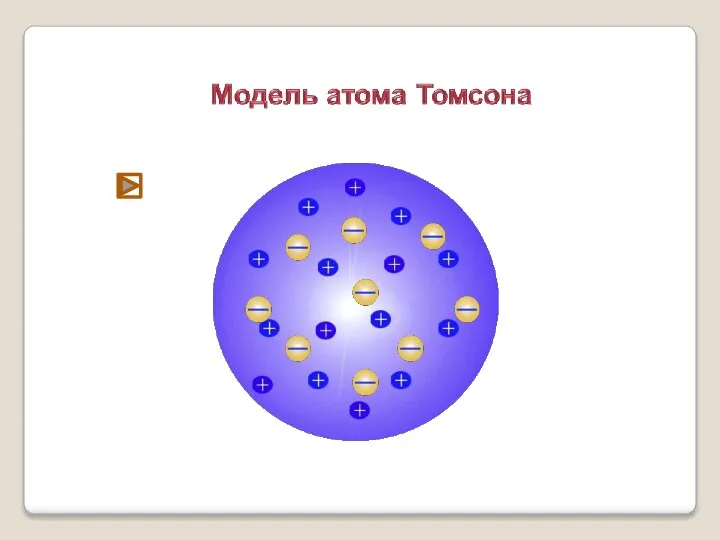
- 6. Модель строения атома Томсона Атом – шар, по всему объёму которого равномерно распределён положительный заряд. Внутри
- 8. Модель Томсона нуждалась в экспериментальной проверке. Важно было убедиться, действительно ли положительный заряд распределён по всему
- 9. В 1899 г. открыл альфа - и бета-лучи. Вместе с Ф. Содди в 1903 г. разработал
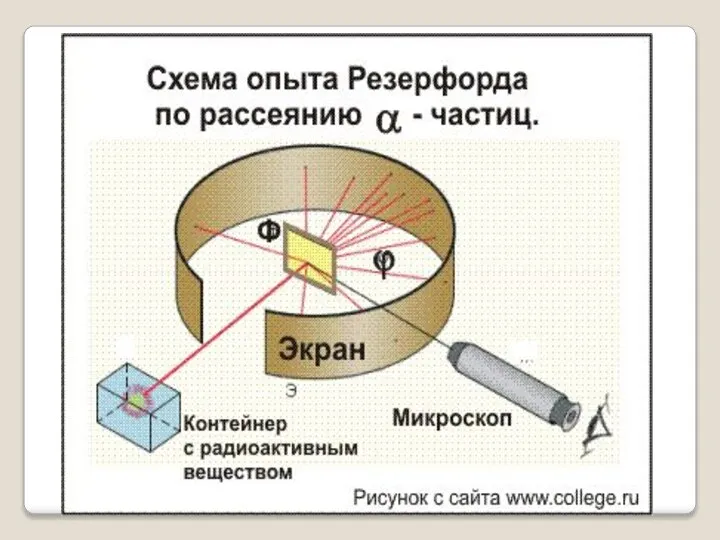
- 10. Идея опыта Резерфорда: Зондировать атом альфа–частицами. Альфа-частицы возникают при распаде радия. Масса альфа-частицы в 8000 раз
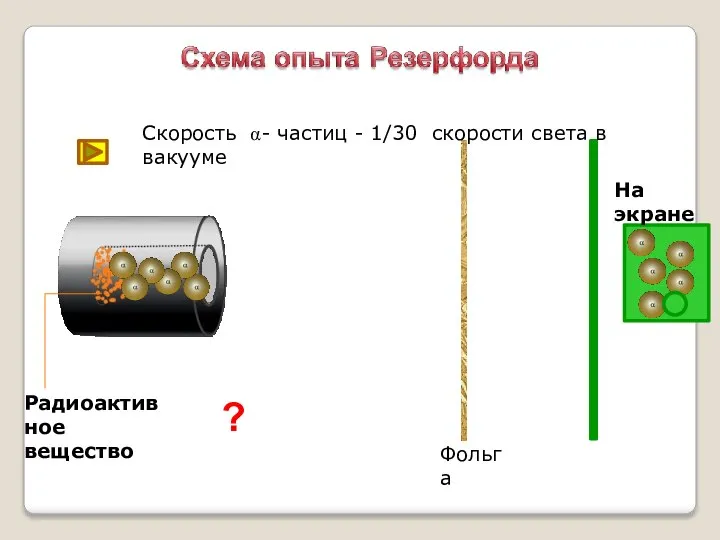
- 12. ? Фольга Радиоактивное вещество Скорость α- частиц - 1/30 скорости света в вакууме На экране
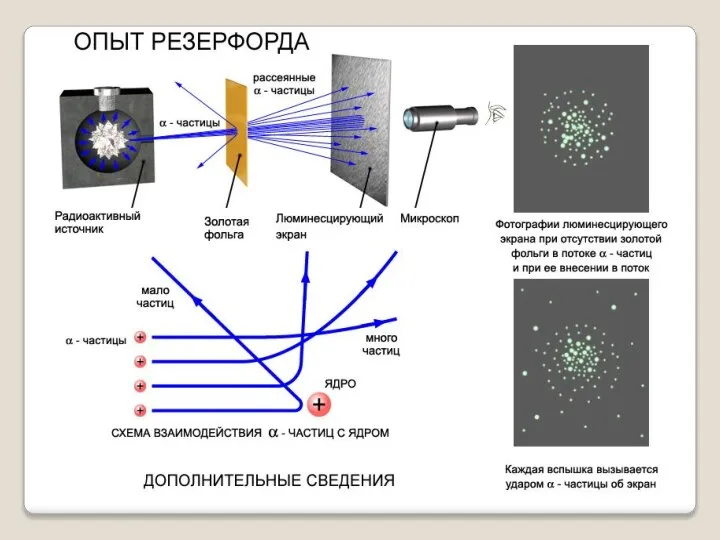
- 14. Опыты показали: Подавляющая часть альфа-частиц проходит сквозь фольгу практически без отклонения или с отклонением на малые
- 15. Обнаружилось, что некоторые α-частицы отклонялись на большие углы, до 180º. Резерфорд понял, что такое отклонение возможно
- 16. Выводы из опытов: Положительный заряд сосредоточен в малой части атома – ядре; Практически вся масса атома
- 17. Конец ХIХ - начало ХХ века На основе выводов из опытов Резерфордом была предложена планетарная модель
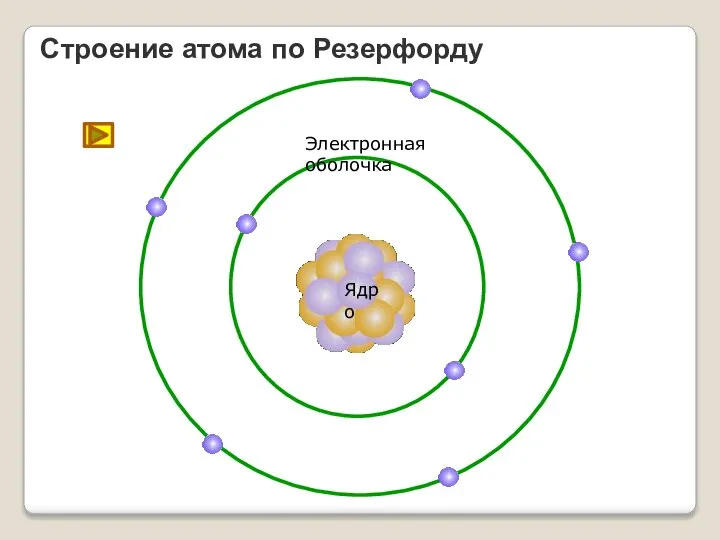
- 18. Строение атома по Резерфорду Ядро Электронная оболочка
- 19. Недостатки атома Резерфорда Эта модель не согласуется с наблюдаемой стабильностью атомов. По законам классической электродинамики вращающийся
- 20. Попыткой спасения планетарной модели атома стали постулаты Нильса Бора
- 21. Вопросы на закрепление: 1. В чём заключается сущность модели Томсона? 2. В чём заключалась идея опыта
- 23. Скачать презентацию















 Презентация на тему Простые механизмы. Рычаг
Презентация на тему Простые механизмы. Рычаг  Весы циферблатные
Весы циферблатные Магнитное поле и его характеристики
Магнитное поле и его характеристики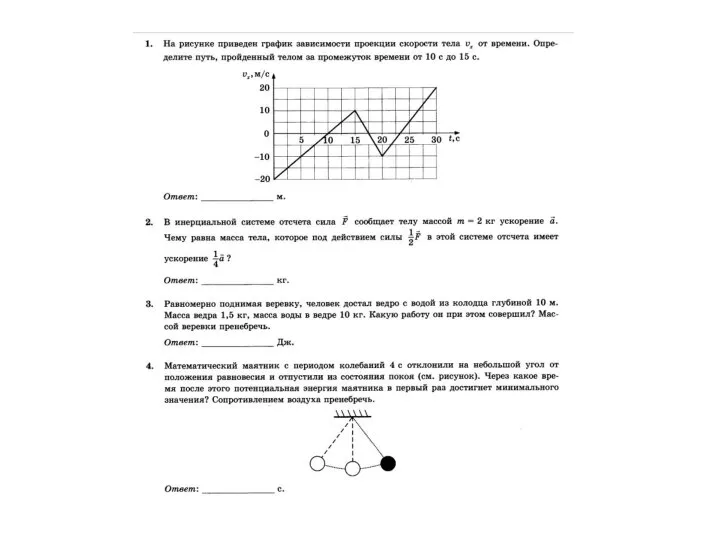 График зависимости скорости проекции тела от времени
График зависимости скорости проекции тела от времени Трубчатый ферментёр
Трубчатый ферментёр Equations of mathematical physics
Equations of mathematical physics Волшебный магнит
Волшебный магнит Компрессия двигателя
Компрессия двигателя Реактивное движение
Реактивное движение Стенд для лабораторных работ Зубчатые передачи
Стенд для лабораторных работ Зубчатые передачи Расчет влияния на человека электрического поля контактной сети электрифицированных железных дорог. Задача 4
Расчет влияния на человека электрического поля контактной сети электрифицированных железных дорог. Задача 4 Вакуумметры. Характеристики вакуумметров
Вакуумметры. Характеристики вакуумметров Постоянные магниты. Магнитное поле Земли
Постоянные магниты. Магнитное поле Земли Закон всемирного тяготения
Закон всемирного тяготения Магнитные материалы и компоненты. (Лекция 5)
Магнитные материалы и компоненты. (Лекция 5) Курс физики. Введение
Курс физики. Введение Переходные процессы в линейных электрических цепях
Переходные процессы в линейных электрических цепях Маса. інертність
Маса. інертність Закон сохранения импульса
Закон сохранения импульса Изготовление и изучение дифракционных оптических элементов
Изготовление и изучение дифракционных оптических элементов Механизм кинематикасының графикалық әдістері
Механизм кинематикасының графикалық әдістері Первый закон термодинамики
Первый закон термодинамики Сравнение идей классической и квантовой физики в объяснении строения атома
Сравнение идей классической и квантовой физики в объяснении строения атома Описание линейных дискретных систем в Zобласти. Тема № 8
Описание линейных дискретных систем в Zобласти. Тема № 8 Метод Акбаева
Метод Акбаева Разработка технологии формирования SiV-центров в поликристаллических алмазных пленках
Разработка технологии формирования SiV-центров в поликристаллических алмазных пленках Теоретическая механика. Дифференциальные уравнения движения. Криволинейное движение (задачи)
Теоретическая механика. Дифференциальные уравнения движения. Криволинейное движение (задачи) Решение задач по теме Закон Кулона. 10 класс
Решение задач по теме Закон Кулона. 10 класс