Содержание
- 2. Молекулы вещества в жидком состоянии расположены почти вплотную друг к другу. Могут совершать тепловые колебания около
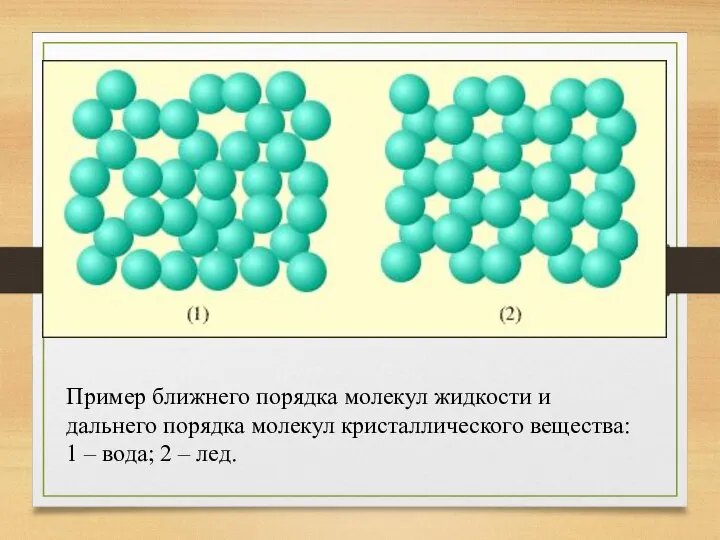
- 3. Пример ближнего порядка молекул жидкости и дальнего порядка молекул кристаллического вещества: 1 – вода; 2 –
- 4. Молекула воды H2O состоит из одного атома кислорода и двух атомов водорода, расположенных под углом 104°.
- 5. Молекулярный механизм поверхностного натяжения. Внутри жидкости результирующая сила притяжения, действующая на молекулу со стороны соседних молекул,
- 6. Капля масла в водном растворе спирта. Молекулы, находящиеся на поверхности под действием резуль- тирующей силы притяжения
- 7. В космическом корабле шарообразную форму принимает и достаточно большая масса жидкости.
- 8. Поверхностное натяжение – явление молекулярного давления на жидкость, вызванное притяжением молекул поверхностного слоя к молекулам внутри
- 9. Сила поверхностного натяжения – сила, направленная по касательной к поверхности жидкости, перпен- дикулярно участку контура, ограничивающего
- 10. Поверхностное натяжение жидкости зависит: 1) от природы жидкости, т. е. от сил притяжения между молекулами данной
- 11. Действие сил поверхностного натяжения Поверхностное натяжение жидкостей, находящихся в контакте с воздухом, мН/м.
- 12. Из-за действия сил поверхностного натяжения в каплях жидкости и внутри мыльных пузырей возникает избыточное давление Δp.
- 13. Избыточное давление внутри мыльного пузыря в два раза больше, так как пленка имеет две поверхности: Отсюда
- 15. Смачивание – искривление поверхности жидкости у поверхности твердого тела в результате взаимодействия молекул жидкости с молекулами
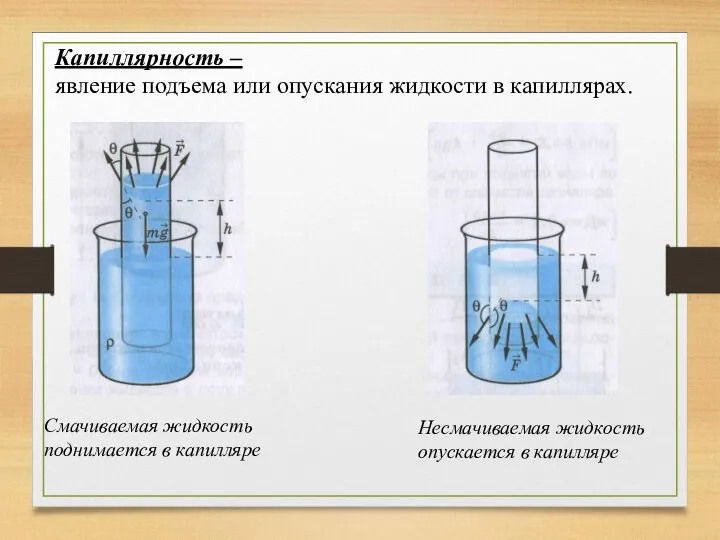
- 18. Капиллярность – явление подъема или опускания жидкости в капиллярах. Смачиваемая жидкость поднимается в капилляре Несмачиваемая жидкость
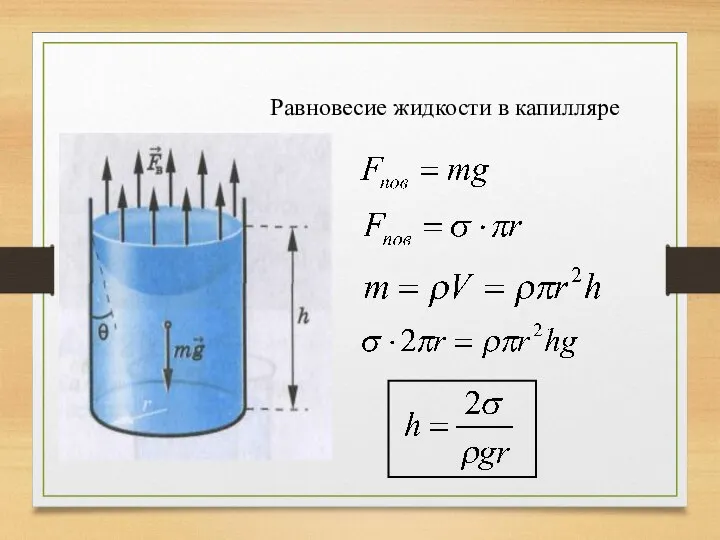
- 19. Равновесие жидкости в капилляре
- 21. Скачать презентацию















 Движение тела по окружности под действием силы тяжести
Движение тела по окружности под действием силы тяжести Суперпроводники. История открытия
Суперпроводники. История открытия Газовые законы
Газовые законы Проводники с током в магнитном поле. Лекция 7
Проводники с током в магнитном поле. Лекция 7 Тормозные системы
Тормозные системы Кинематика
Кинематика Электромагнитные волны. Лекция 11
Электромагнитные волны. Лекция 11 Презентация на тему Выталкивающая сила
Презентация на тему Выталкивающая сила  Определение проекции силы на координатную ось
Определение проекции силы на координатную ось Инновационные технологии в машиностроении. Лекция 1, 2. Общая характеристика машиностроительного производства
Инновационные технологии в машиностроении. Лекция 1, 2. Общая характеристика машиностроительного производства Разработка инструментария для решения задачи вычислительной гидродинамики при моделировании воздушных потоков
Разработка инструментария для решения задачи вычислительной гидродинамики при моделировании воздушных потоков Радиоактивные превращения атомных ядер
Радиоактивные превращения атомных ядер Общие сведения о системах радиосвязи. Электропитание средств связи
Общие сведения о системах радиосвязи. Электропитание средств связи Общий осмотр автомобиля Toyota Mark II
Общий осмотр автомобиля Toyota Mark II Презентация на тему Интерференция. Дифракция
Презентация на тему Интерференция. Дифракция  Неразъемные соединения
Неразъемные соединения Слесарные инструменты
Слесарные инструменты Урок 12 Електродвигуни. Електровимірювальні прилади
Урок 12 Електродвигуни. Електровимірювальні прилади Моделирование процессов преобразования сигналов и помех линейными и нелинейными звеньями
Моделирование процессов преобразования сигналов и помех линейными и нелинейными звеньями Международная система единиц СИ
Международная система единиц СИ Презентация на тему Источники электрического тока
Презентация на тему Источники электрического тока  Фильтры с бесконечной импульсной характеристикой. Синтез БИХ-фильтров методом билинейного Z-преобразования''
Фильтры с бесконечной импульсной характеристикой. Синтез БИХ-фильтров методом билинейного Z-преобразования'' Однородные уравнения. Уравнения, приводящиеся к однородным
Однородные уравнения. Уравнения, приводящиеся к однородным Построение изображений, полученных с помощью линз
Построение изображений, полученных с помощью линз Определение коэффициента поверхностного натяжения синтетических моющих средств
Определение коэффициента поверхностного натяжения синтетических моющих средств Электроэнергия Ксенон (Светодиоды)
Электроэнергия Ксенон (Светодиоды) Графическое представление результатов измерений
Графическое представление результатов измерений Блоки цилиндров и цилиндровые втулки
Блоки цилиндров и цилиндровые втулки