Содержание
- 2. СОДЕРЖАНИЕ Цель Первые понятия о железе Значение Физические свойства Химические свойства(с простыми веществами) Химические свойства(со сложными
- 3. ЦЕЛИ Содержание Формирование понятий о железе: Изучение химических и физических свойств; Решение практических задач и уравнений
- 4. Ковкий, вязкий металл серебристо-белого цвета. Гидротермальный источник с железистой водой. Оксиды железа окрашивают воду в бурый
- 5. ЗНАЧЕНИЕ Железо — один из самых используемых металлов, на него приходится до 95 % мирового металлургического
- 6. Физические свойства Цвет : серебристо-белый Блеск : блестящий Пластичность : очень пластичный, легко куется, прокатывается, штампуется
- 7. Химические свойства Взаимодействие с простыми веществами-неметаллами 2) С кислородом 3Fe + 2O2 —>Fe3O4 Содержание 1) С
- 8. Химические свойства Взаимодействие со сложными веществами Содержание 1) С водой 2) С солями 3) С кислотами
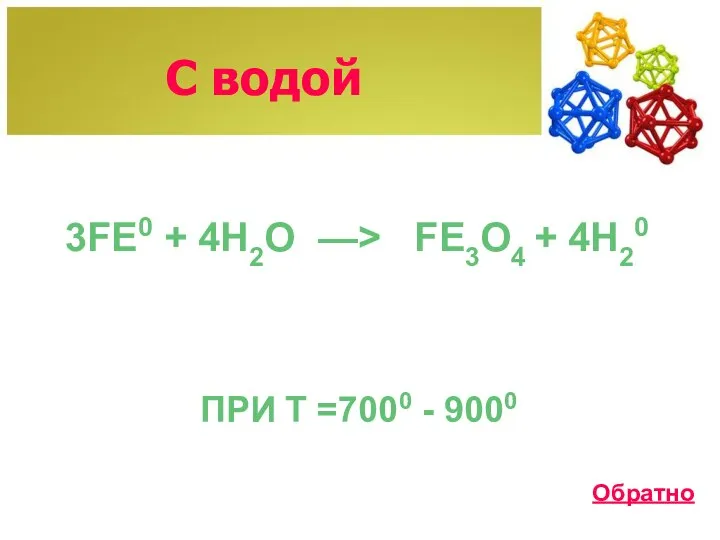
- 9. С водой 3FE0 + 4H2O ПРИ T =7000 - 9000 —> FE3O4 + 4H20 Обратно
- 10. С солями ОПЫТ: осуществите реакцию между порошком железа и раствором хлорида меди (II). Fe + CuCl2
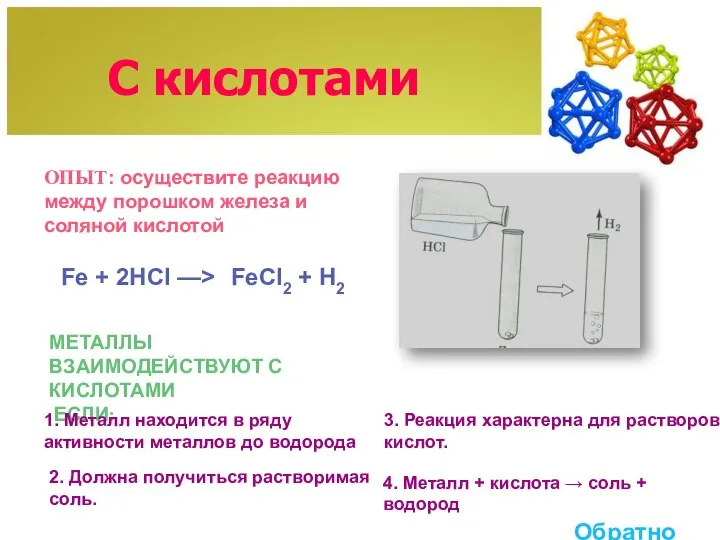
- 11. С кислотами ОПЫТ: осуществите реакцию между порошком железа и соляной кислотой Fe + 2HCl —> МЕТАЛЛЫ
- 12. Интересные факты А количество железа, равное всему добытому человечеством золоту, извлекается из недр земного шара примерно
- 13. Нахождение в природе Железо является также одним из наиболее распространенных элементов в природных водах, где среднее
- 14. Важнейшие источники Содержание
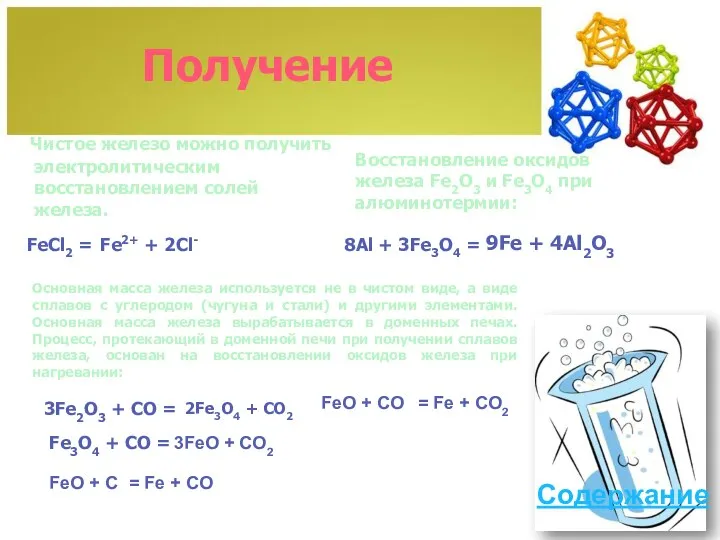
- 15. Получение Чистое железо можно получить электролитическим восстановлением солей железа. Содержание FeCl2 = Fe2+ + 2Cl- Восстановление
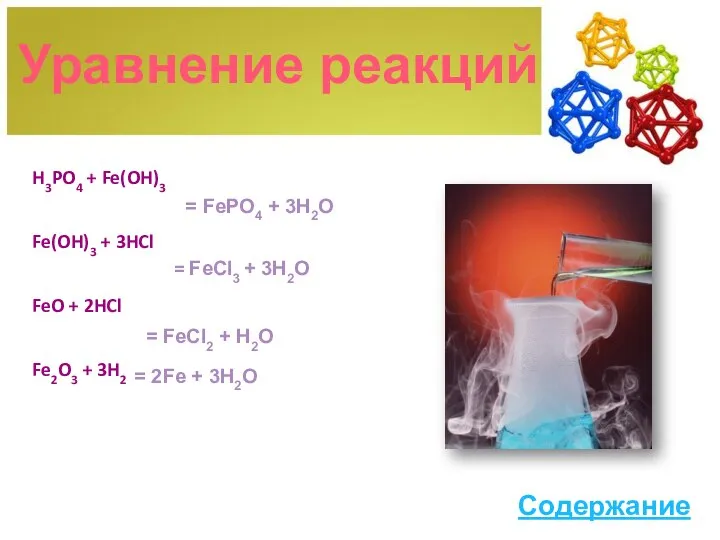
- 16. H3PO4 + Fe(OH)3 Fe(OH)3 + 3HCl FeO + 2HCl Fe2O3 + 3H2 Уравнение реакций = FePO4
- 17. Вывод Железо один из самых значимых и известных металлов. Он играет важную роль как и в
- 19. Скачать презентацию












 Техническая механика. Раздел: Теоретическая механика. Лекция 1
Техническая механика. Раздел: Теоретическая механика. Лекция 1 Сплавы. Свойства сплавов
Сплавы. Свойства сплавов Парообразование
Парообразование Электричество и магнетизм. Электрическое поле в диэлектриках (Лекция 5)
Электричество и магнетизм. Электрическое поле в диэлектриках (Лекция 5) Теорема Гаусса и её применение к расчету электрических полей. Лекция 14
Теорема Гаусса и её применение к расчету электрических полей. Лекция 14 Применение ядерной энергии в различных отраслях. Доза радиоактивного излучения. Применение ядерного оружия
Применение ядерной энергии в различных отраслях. Доза радиоактивного излучения. Применение ядерного оружия Физико-химические параметры самораспространяющегося высокотемпературного синтеза
Физико-химические параметры самораспространяющегося высокотемпературного синтеза Тайны мыльных пузырей
Тайны мыльных пузырей Презентация на тему Мощность. Единицы мощности
Презентация на тему Мощность. Единицы мощности  Краткие сведения из физической оптики. Явления дифракции, дисперсии, интерференции. Лазерные источники излучения. Лекция №3
Краткие сведения из физической оптики. Явления дифракции, дисперсии, интерференции. Лазерные источники излучения. Лекция №3 Физика- это наука понимать природу. Архимедова сила
Физика- это наука понимать природу. Архимедова сила Световое давление Урок для 11 класса.
Световое давление Урок для 11 класса. Теоретические основы контроля и анализа функционирования систем автоматического управления
Теоретические основы контроля и анализа функционирования систем автоматического управления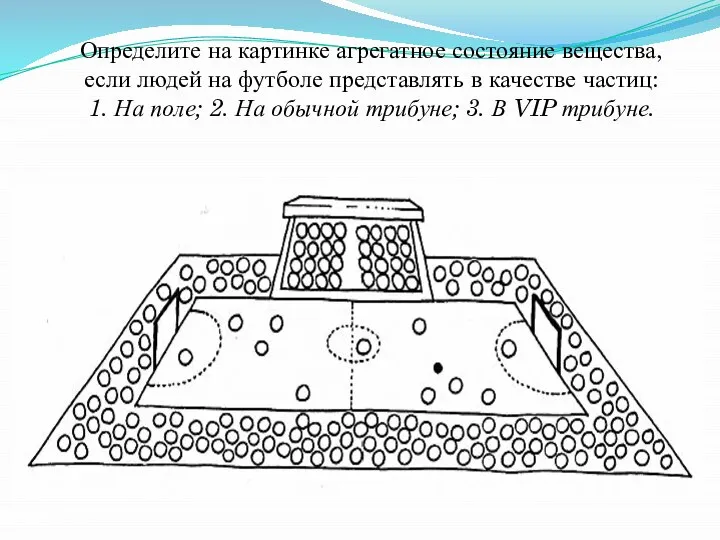 Физические свойства вещества: текучесть, плотность, тепло и электропроводность, ковкость и пластичность
Физические свойства вещества: текучесть, плотность, тепло и электропроводность, ковкость и пластичность Плазма и ионизирующие излучения в атомной и космической промышленности. Тема 1
Плазма и ионизирующие излучения в атомной и космической промышленности. Тема 1 Закон Ома. Светодиоды. Кнопки
Закон Ома. Светодиоды. Кнопки Электр тогы
Электр тогы Фейерверки. Скорость звука
Фейерверки. Скорость звука Разработка проекта устройства снижающего тяжесть последствий при потере устойчивости дорожных катков и компакторов
Разработка проекта устройства снижающего тяжесть последствий при потере устойчивости дорожных катков и компакторов Открытая лаборатория. Физика - наука о природе
Открытая лаборатория. Физика - наука о природе Механическое движение. Урок физики в 7 классе
Механическое движение. Урок физики в 7 классе 11кл. Электромагн индукция (3)
11кл. Электромагн индукция (3) Рисунки к методичке по теплообменнику
Рисунки к методичке по теплообменнику Термодинамика и молекулярная физика. Лекция 6
Термодинамика и молекулярная физика. Лекция 6 Магнитный поток. Вектор магнитной индукции
Магнитный поток. Вектор магнитной индукции Fizika_Lektsii_po_Optike_geometricheskaya_volnovaya_izluchenie_kvantovye_yavlenia (1)
Fizika_Lektsii_po_Optike_geometricheskaya_volnovaya_izluchenie_kvantovye_yavlenia (1) Технологические характеристики грунтов. Определение трудности процессов разработки горных пород
Технологические характеристики грунтов. Определение трудности процессов разработки горных пород Резонанс. Учет и использование резонанса в быту и промышленности
Резонанс. Учет и использование резонанса в быту и промышленности