Содержание
- 2. Сванте Август Аррениус (1859 – 1927) - основатель теории электролитической диссоциации
- 3. 2.Электролитическая диссоциация процесс распада молекул электролита на ионы в растворе или расплаве. Электролитическая диссоциация -
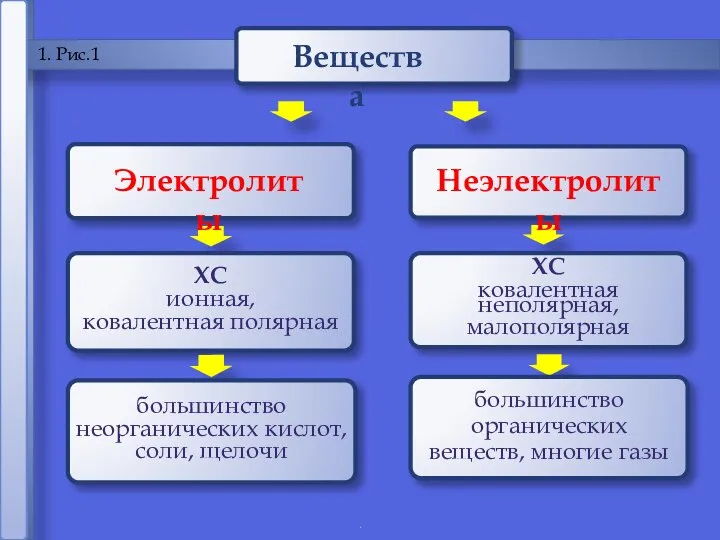
- 4. . 1 1. Рис.1 Электролиты Неэлектролиты
- 5. 1. Электролиты и неэлектролиты это вещества, растворы и расплавы которых проводят электрический ток. Электролиты -
- 6. 1. Электролиты и неэлектролиты это вещества, растворы или расплавы которых не проводят электрический ток. Неэлектролиты -
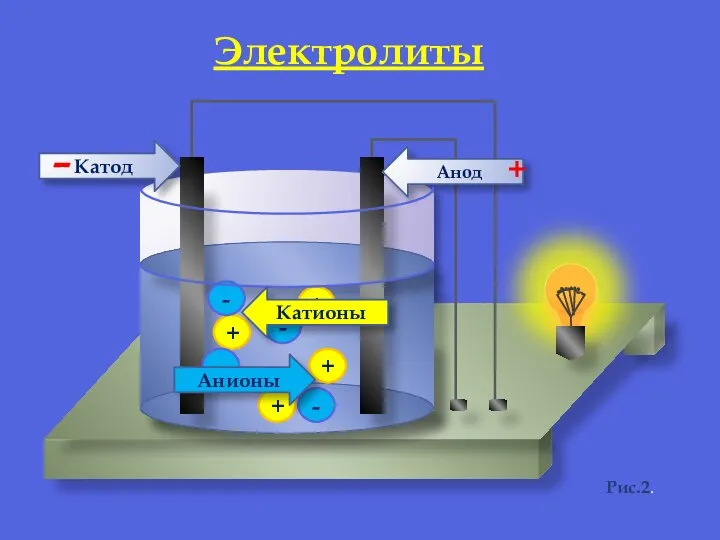
- 7. + + + + - - - - Анионы Катионы Анод Катод - + Электролиты Рис.2.
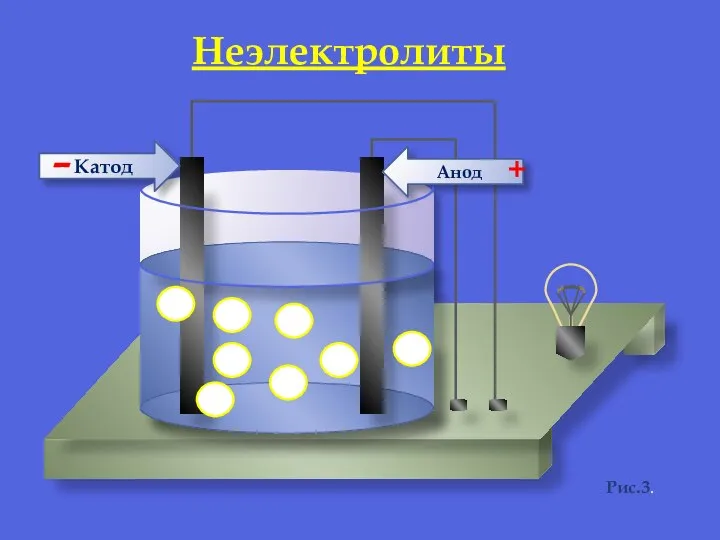
- 8. Анод Катод - + Рис.3. Неэлектролиты
- 9. 1. Электролиты и неэлектролиты Вода – хороший растворитель, т.к. молекулы воды полярны. слабый амфотерный электролит. ион
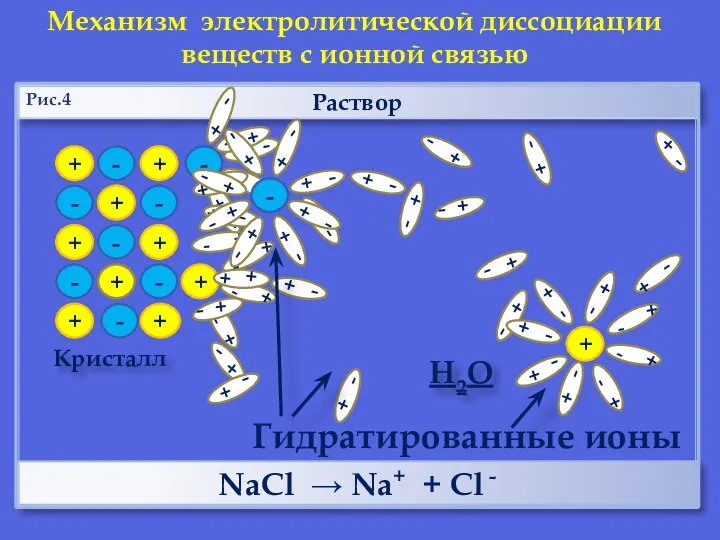
- 10. + + - - + + - - Раствор Кристалл - + + + - -
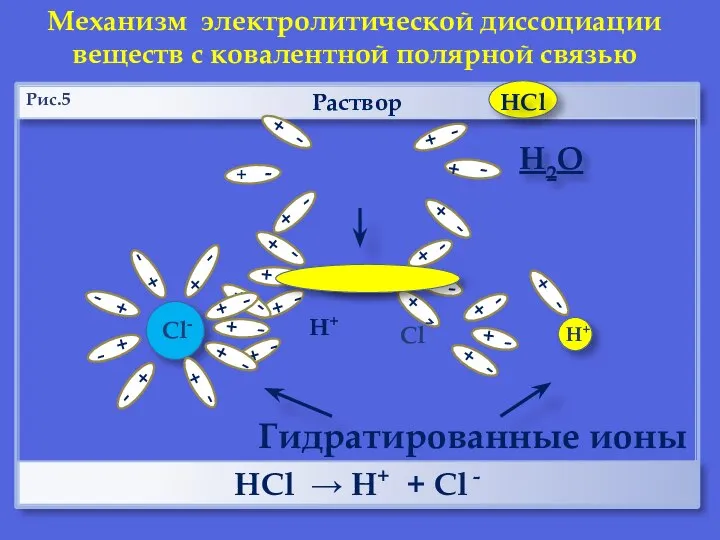
- 11. Раствор НCl → Н+ + Cl - Механизм электролитической диссоциации веществ с ковалентной полярной связью Н2О
- 12. 2.Сильные и слабые электролиты HCl + + + Сильные и слабые Рис.6.
- 13. отношение числа диссоциированных молекул к общему числу молекул, находящихся в растворе. Степень электролитической диссоциации (α) -
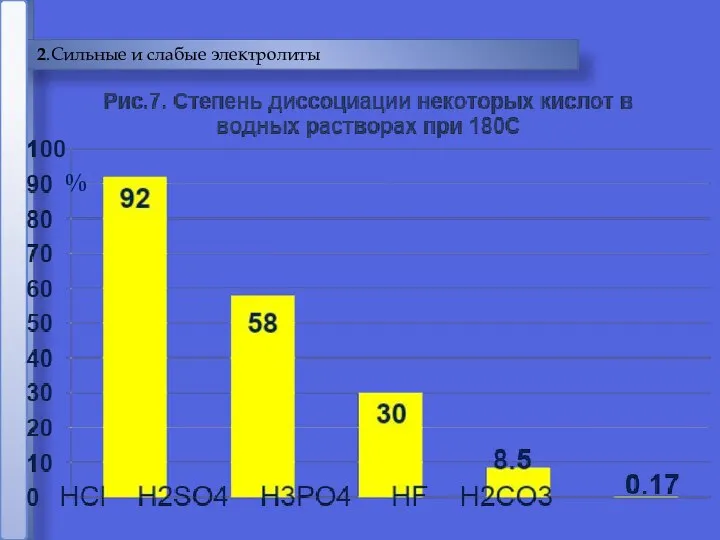
- 14. 2.Сильные и слабые электролиты %
- 15. 1. Все металлы проводят электрический ток, следовательно, все металлы -электролиты.
- 16. 2. Если встать в лужу, в которой лежит оголенный провод, находящийся под напряжением, можно получить смертельный
- 17. 3. В дистиллированной воде приготовили настой лечебных плодов (шиповника, черники, калины). Настой стал проводить электрический ток.
- 18. 4. При рентгеноскопии желудка пациенту дают выпить взвесь BaSO4. Объясните, почему чистый BaSO4 не вызывает отравлений,
- 19. это сложные вещества, при диссоциации которых в водных растворах в качестве катионов отщепляются только ионы водорода.
- 20. это сложные вещества, при диссоциации которых в водных растворах в качестве анионов отщепляются только гидроксид-ионы. Основания
- 21. это сложные вещества, которые в водных растворах диссоциируют на катионы металла и анионы кислотного остатка. Соли
- 22. Электролитическая диссоциация Лабораторный опыт 1. В две пробирки насыпать обезвоженный сульфат меди. В одну из пробирок
- 23. Электролитическая диссоциация Лабораторный опыт 2. В две сухие пробирки насыпать немного кристаллического гидроксида кальция (или оксида
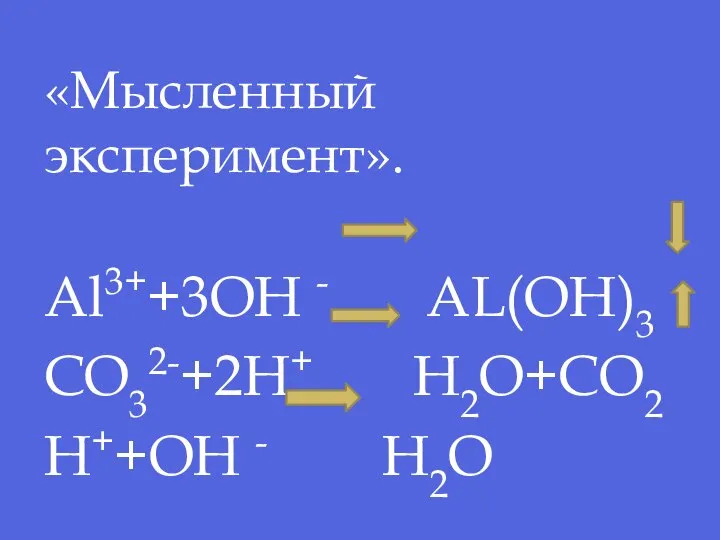
- 24. «Мысленный эксперимент». Al3++3OH - AL(OH)3 CO32-+2H+ H2O+CO2 H++OH - H2O
- 25. 6. Рис.8. Характерные симптомы дефицита химических элементов в организме человека
- 26. 6. О значении электролитов для живых организмов Электролитическая диссоциация Электролиты – составная часть жидкостей и плотных
- 28. Скачать презентацию


















 Химические формулы
Химические формулы 9-8 кислоты в свете ТЭД (1)
9-8 кислоты в свете ТЭД (1) Спирты
Спирты Адсорбционно-десорбционные взаимодействия фосфатов кальция и аминокислот
Адсорбционно-десорбционные взаимодействия фосфатов кальция и аминокислот Соли как производные кислот и оснований
Соли как производные кислот и оснований Интерактивная интеллектуальная игра Юный химик
Интерактивная интеллектуальная игра Юный химик Класс оксиды
Класс оксиды Обобщение знаний об углеводородах
Обобщение знаний об углеводородах ЕГЭ по химии: документы, регламентирующие структуру и содержание контрольных измерительных материалов
ЕГЭ по химии: документы, регламентирующие структуру и содержание контрольных измерительных материалов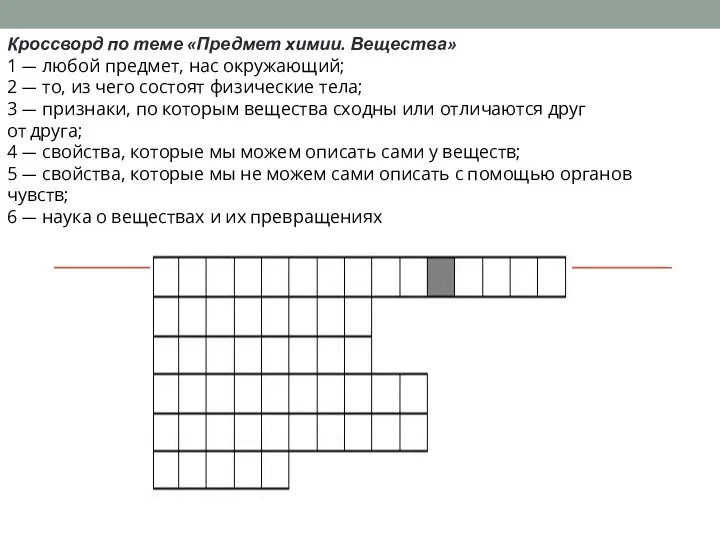 Предмет химии. Вещества
Предмет химии. Вещества 3bc28ca0711047a6880d20a6763f17db
3bc28ca0711047a6880d20a6763f17db Общая характеристика оксидов
Общая характеристика оксидов Золото
Золото Органическая химия. Ароматические углеводороды
Органическая химия. Ароматические углеводороды Методы получения нафтиридинов (всех изомеров)
Методы получения нафтиридинов (всех изомеров) Нефть и её переработка
Нефть и её переработка Оксид кремния
Оксид кремния Основания: номенклатура, классификация, применение, физические свойства
Основания: номенклатура, классификация, применение, физические свойства Алмаз. Свойства алмазов
Алмаз. Свойства алмазов Презентация на тему Соединения серы
Презентация на тему Соединения серы  Свойства солей, оксидов, оснований
Свойства солей, оксидов, оснований Модель химического образования на основе технологического подхода. Методическая система учителя химии
Модель химического образования на основе технологического подхода. Методическая система учителя химии Техника титрования и лабораторная посуда
Техника титрования и лабораторная посуда Уровень С1 в ГИА
Уровень С1 в ГИА Задачи. Периодическая система. Строение атома. Повторение
Задачи. Периодическая система. Строение атома. Повторение Азотсодержащие гетероциклические соединения пиррол
Азотсодержащие гетероциклические соединения пиррол Предельные углеводороды. Тест 19
Предельные углеводороды. Тест 19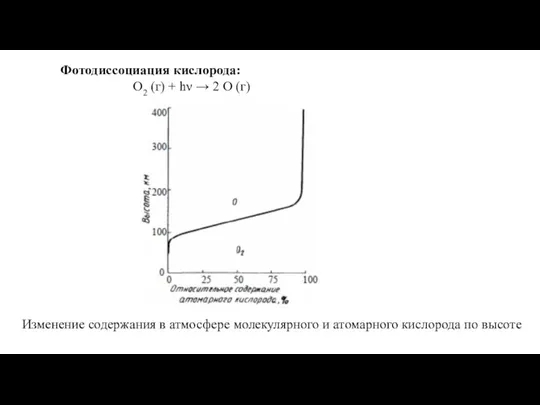 Фотодиссоциация кислорода
Фотодиссоциация кислорода