Содержание
- 2. Учителя химии: Гершановская Евгения Владимировна ГБОУ СОШ № 880 Город Москва Попова Светлана Анатольевна ГБОУ СОШ
- 3. СОДЕРЖАНИЕ Ученые, получившие алюминий Характеристика элемента - алюминия Нахождение в природе Физические свойства Химические свойства Применение
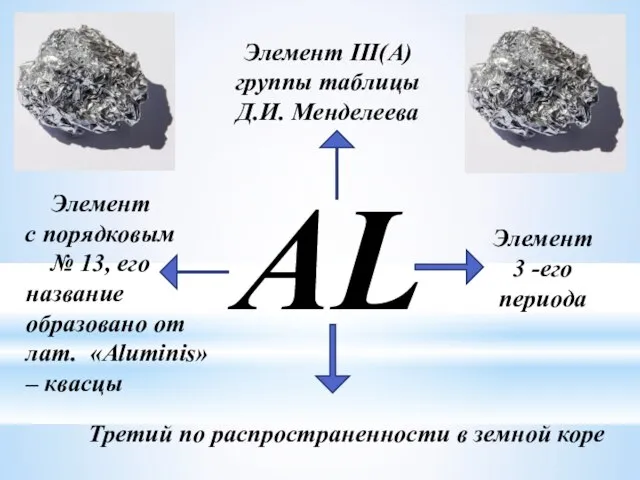
- 4. AL Элемент III(A) группы таблицы Д.И. Менделеева Элемент с порядковым № 13, его Элемент 3 -его
- 5. Датский физик Ганс Эрстед (1777-1851) Впервые алюминий был получен им в 1825 году действием амальгамы калия
- 6. Современное получение алюминия Современные метод получения был разработан независимо друг от друга: американцем Чарльзом Холлом и
- 7. Будучи студентом Оберлинского колледжа, он узнал, что можно разбогатеть и получить благодарность человечества, если изобрести способ
- 8. Поль Эру (1863-1914) – французский инженер - химик В 1889 году открыл алюминиевый завод во Фроне
- 9. Нахождение в природе Важнейшим на сегодня минералом алюминия является боксит Основной химический компонент боксита - глинозем
- 10. Физические свойства мягкий легкий (с малой плотностью – 2,7 г/см3) с высокой тепло- и электропроводностью легкоплавкий
- 11. с серой, образуя сульфид алюминия: 2Al + 3S = Al2S3 с азотом, образуя нитрид алюминия: 2Al
- 12. Химические свойства 1. с водой (после удаления защитной оксидной пленки) 2Al + 6H2O = 2Al(OH)3 +
- 13. ПРИМЕНЕНИЕ АЛЮМИНИЯ Легкий сплав дюраль используется в различных областях В Авиации В Космической технике В Электротехнике
- 14. Соединения алюминия Оксид алюминия (AL2O3) Гидроксид алюминия AL(OH)3
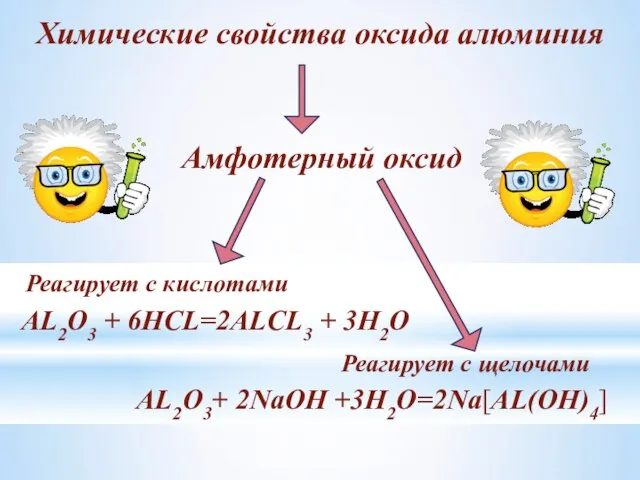
- 15. Химические свойства оксида алюминия Амфотерный оксид Реагирует с кислотами Реагирует с щелочами AL2O3 + 6HCL=2ALCL3 +
- 16. AL2O3 Глинозём Корунд сапфир рубин Боксит
- 17. Применение сапфиров знаменитые сапфиры английской королевской семьи
- 18. Применение рубинов
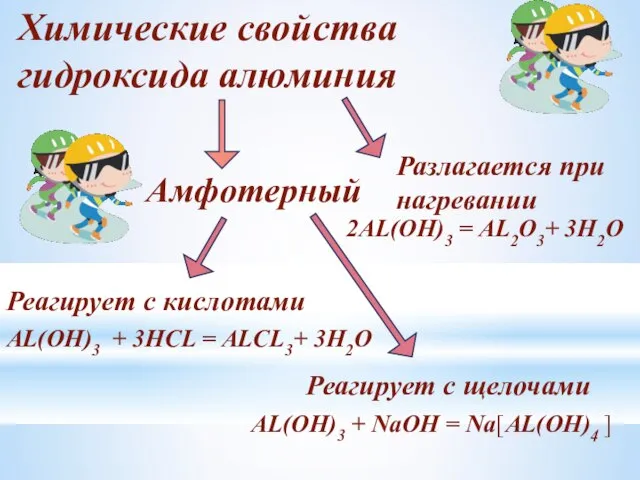
- 19. Химические свойства гидроксида алюминия Амфотерный Реагирует с кислотами Реагирует с щелочами AL(OH)3 + 3HCL = ALCL3+
- 20. Соли алюминия Растворимые в воде Нерастворимые в воде При реакции растворимых солей алюминия с щелочами получается
- 21. Вставьте пропущенные слова в текст: Проверьте себя: Алюминий – это металл, у которого в соединениях степень
- 22. Какие из соединений вступят в реакцию с алюминием: Cl2 K2O CuSO4 H2O S BaSO4 HCL Cr
- 24. Скачать презентацию
















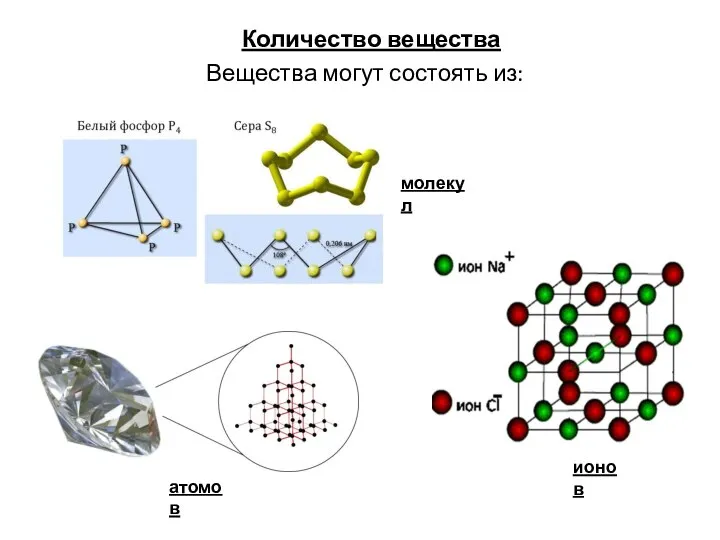 Количество вещества
Количество вещества Кислоты в химии
Кислоты в химии Алкадиены. Строение. свойства и применение
Алкадиены. Строение. свойства и применение Малотоннажные термопласты
Малотоннажные термопласты Органика из аптеки
Органика из аптеки Три секрета прочности волокнистых композитов
Три секрета прочности волокнистых композитов Определение качества дизельного топлива
Определение качества дизельного топлива Строение атома в ЭЖ (1)
Строение атома в ЭЖ (1) Основания, их классификация и свойства в свете теории электролитической диссоциации
Основания, их классификация и свойства в свете теории электролитической диссоциации Характеристика кислорода и серы
Характеристика кислорода и серы Химические реакции
Химические реакции Предельные одноосновные карбоновые кислоты. Сложные эфиры
Предельные одноосновные карбоновые кислоты. Сложные эфиры Количество вещества. Моль. Молярная масса
Количество вещества. Моль. Молярная масса Кислоты
Кислоты Классификация органических соединений
Классификация органических соединений Каскадный синтез пептидов
Каскадный синтез пептидов Халькогены. Электронное строение кислорода и серы
Халькогены. Электронное строение кислорода и серы Химия в быту
Химия в быту Презентация Повторение к СОЧ-10 кл (1)
Презентация Повторение к СОЧ-10 кл (1) Органическая химия. Подготовка к экзамену
Органическая химия. Подготовка к экзамену Алкины. Понятие об алкинах
Алкины. Понятие об алкинах Презентация на тему Производство стекла
Презентация на тему Производство стекла  Сeквенирование нуклеиновых кислот
Сeквенирование нуклеиновых кислот Химическое равновесие
Химическое равновесие Применение неметаллов
Применение неметаллов Тепловой эффект химических реакций
Тепловой эффект химических реакций Проект по химии. Минералы на нашей коже
Проект по химии. Минералы на нашей коже Основные классы неорганических соединений
Основные классы неорганических соединений