Содержание
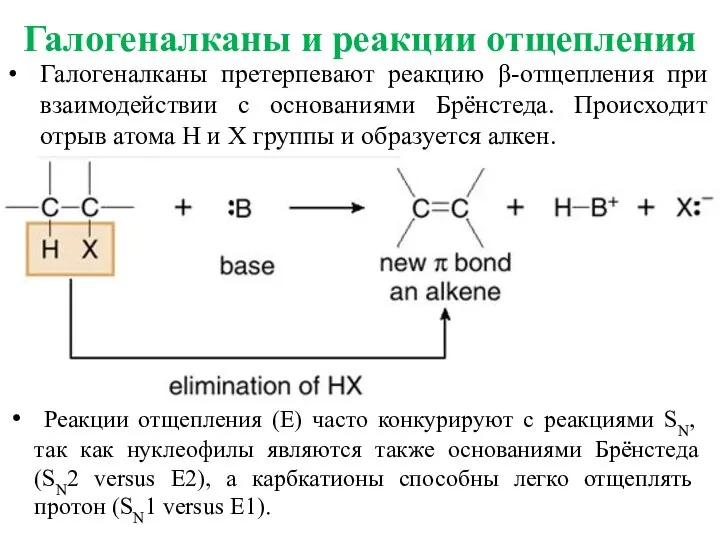
- 2. Галогеналканы и реакции отщепления Галогеналканы претерпевают реакцию β-отщепления при взаимодействии с основаниями Брёнстеда. Происходит отрыв атома
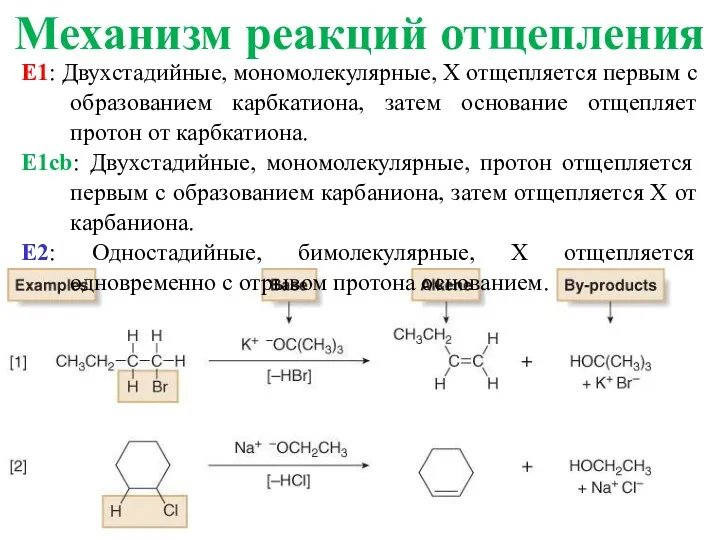
- 3. E1: Двухстадийные, мономолекулярные, X отщепляется первым с образованием карбкатиона, затем основание отщепляет протон от карбкатиона. E1cb:
- 4. Основания используются для реакций отщепления Для реакций отщепления используются сильные основания. Как правило это натриевые или
- 5. Основания и нуклеофилы Нуклеофил/основание попадет в одну из четырех категорий: сильный нуклеофил/ сильное основание, сильный нуклеофил/
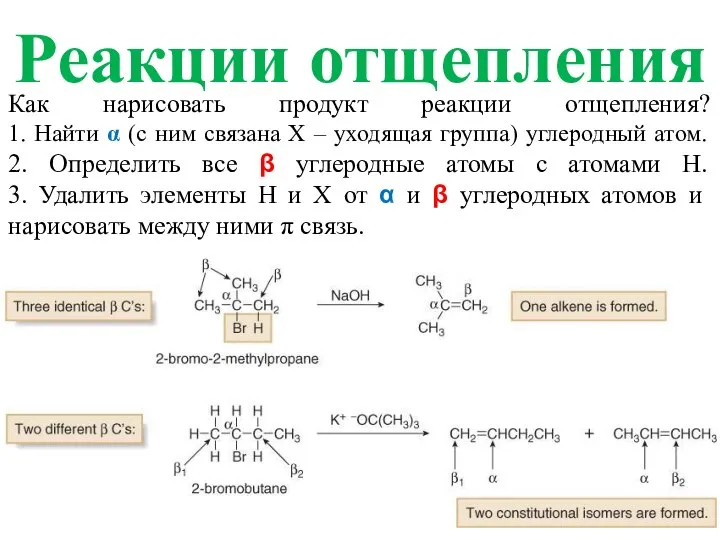
- 6. Реакции отщепления Как нарисовать продукт реакции отщепления? 1. Найти α (с ним связана Х – уходящая
- 7. Кинетика второго порядка: скорость реакции определяют концентрации и галогеналкана и основания. Механизм реакции отщепления — E2
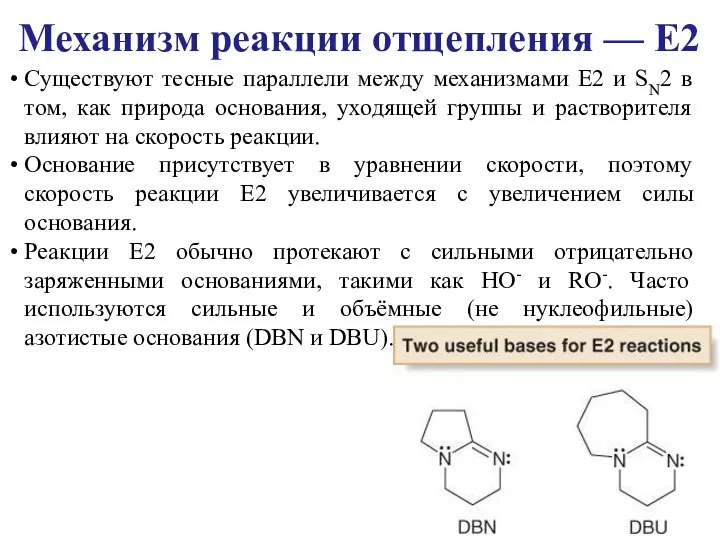
- 8. Существуют тесные параллели между механизмами E2 и SN2 в том, как природа основания, уходящей группы и
- 9. 1,5-диазабицикло[4.3.0]нон-5-ен и 1.8-диазабицикло[5.4.0]ундец-7-ен Объёмные азотистые основания (DBN и DBU)
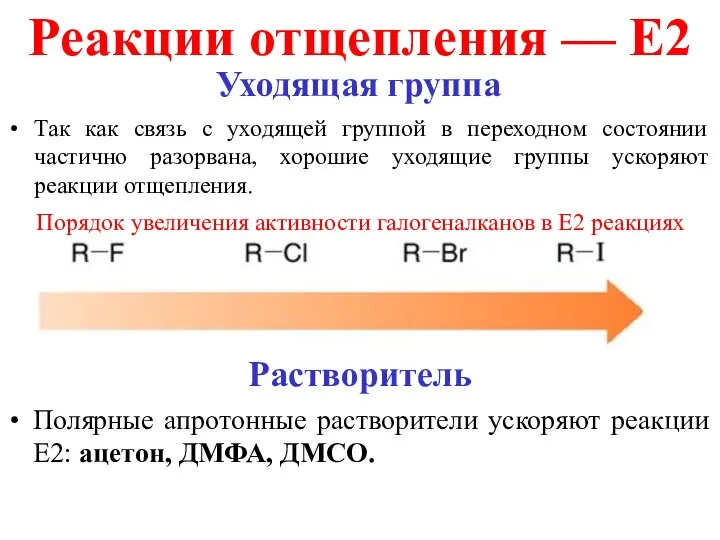
- 10. Реакции отщепления — E2 Растворитель Полярные апротонные растворители ускоряют реакции Е2: ацетон, ДМФА, ДМСО. Уходящая группа
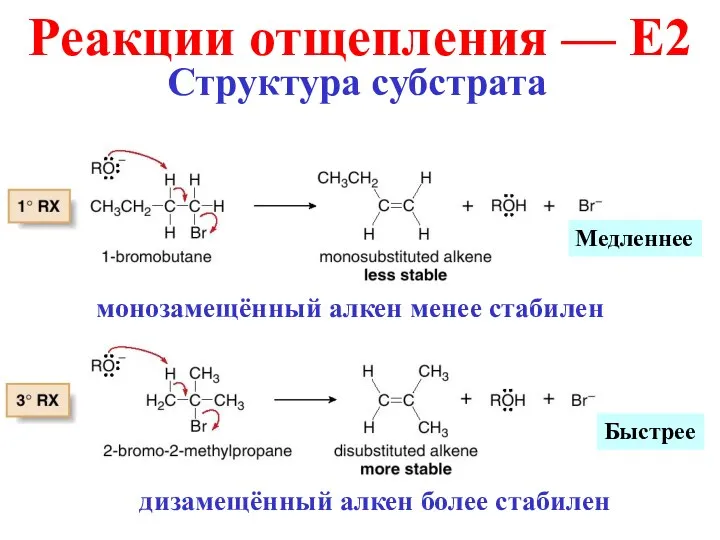
- 11. Замещение vs. отщепление Структура субстрата Реакции отщепления — E2 С увеличением количества R-групп в субстрате, связанных
- 12. Медленнее Быстрее Реакции отщепления — E2 Структура субстрата монозамещённый алкен менее стабилен дизамещённый алкен более стабилен
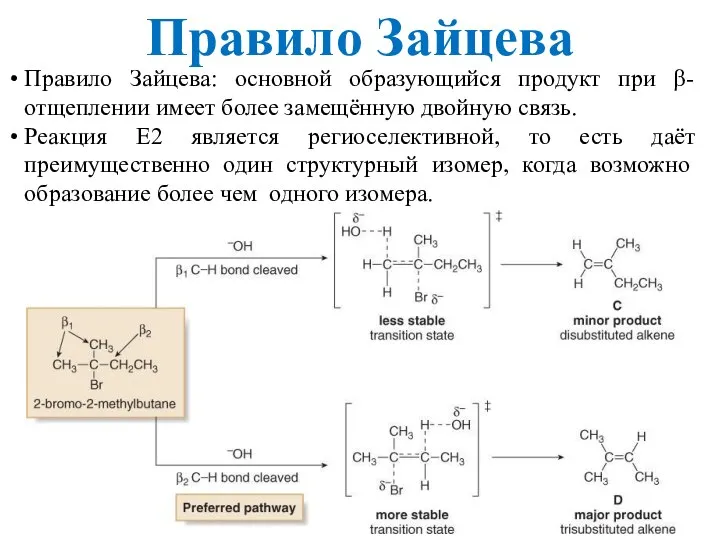
- 13. Правило Зайцева: основной образующийся продукт при β-отщеплении имеет более замещённую двойную связь. Реакция Е2 является региоселективной,
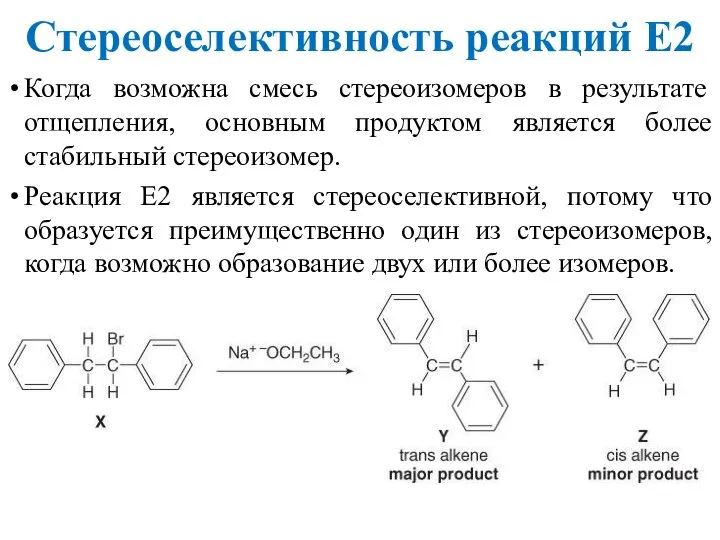
- 14. Стереоселективность реакций Е2 Когда возможна смесь стереоизомеров в результате отщепления, основным продуктом является более стабильный стереоизомер.
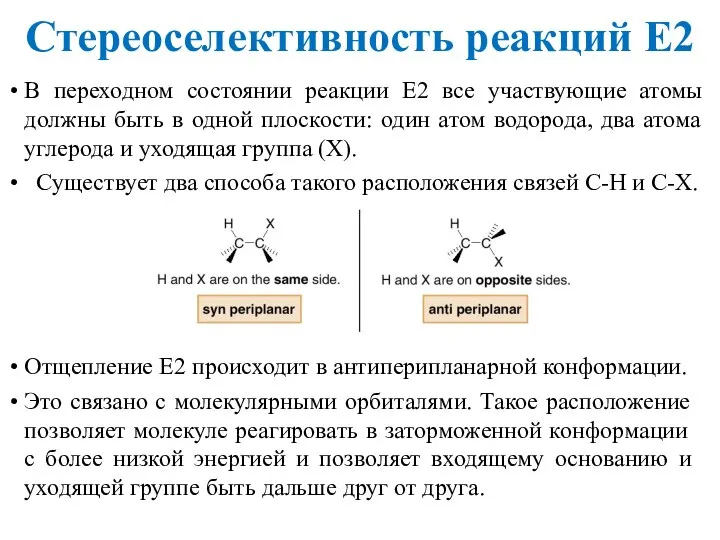
- 15. В переходном состоянии реакции E2 все участвующие атомы должны быть в одной плоскости: один атом водорода,
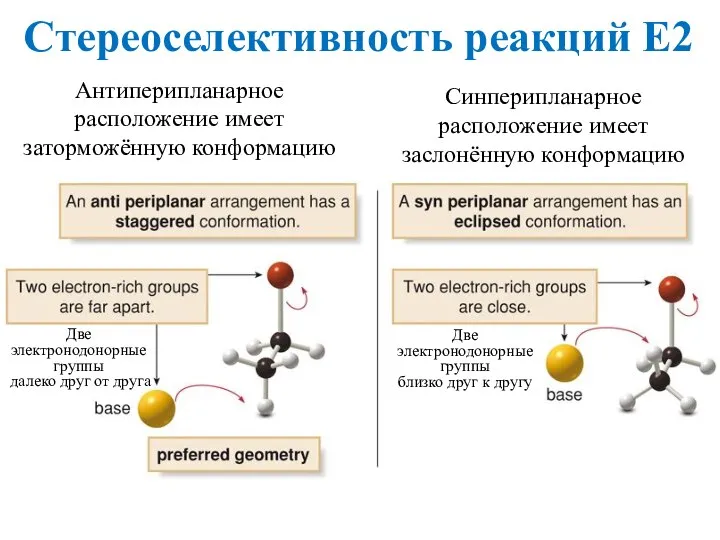
- 16. Стереоселективность реакций Е2 Антиперипланарное расположение имеет заторможённую конформацию Синперипланарное расположение имеет заслонённую конформацию Две электронодонорные группы
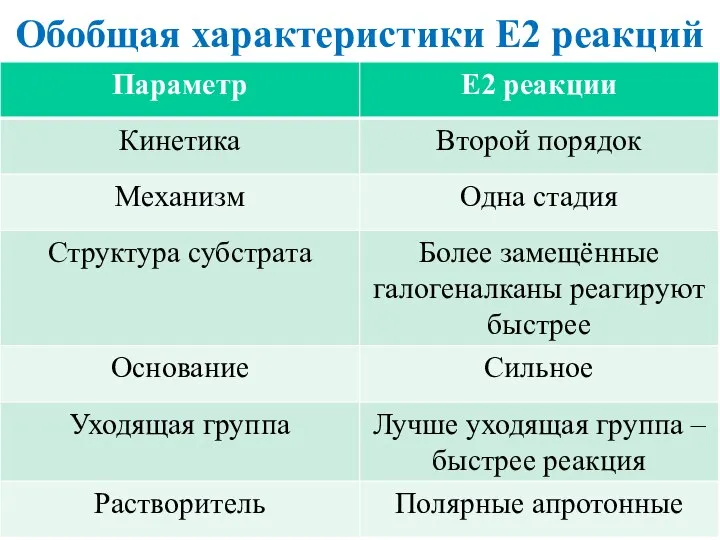
- 17. Обобщая характеристики E2 реакций
- 18. Реакции E1 имеют кинетику первого порядка: Реакции отщепления E1 Сокрость = k[(CH3)3CCI] Реакция E1 протекает по
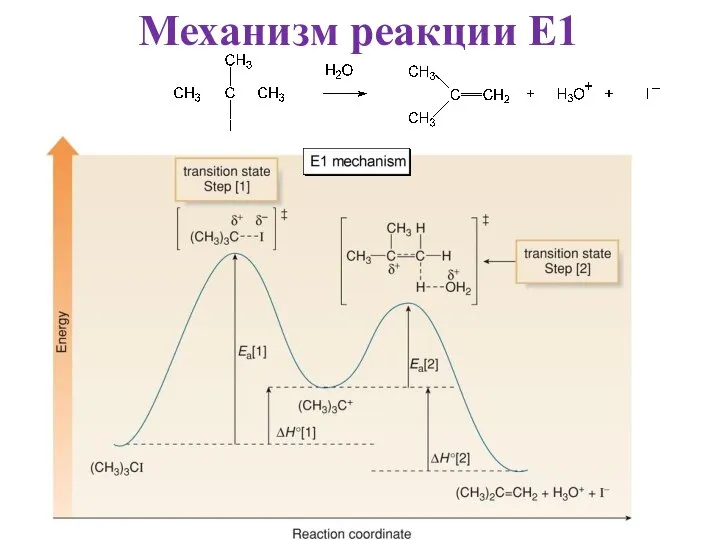
- 19. Механизм реакции E1
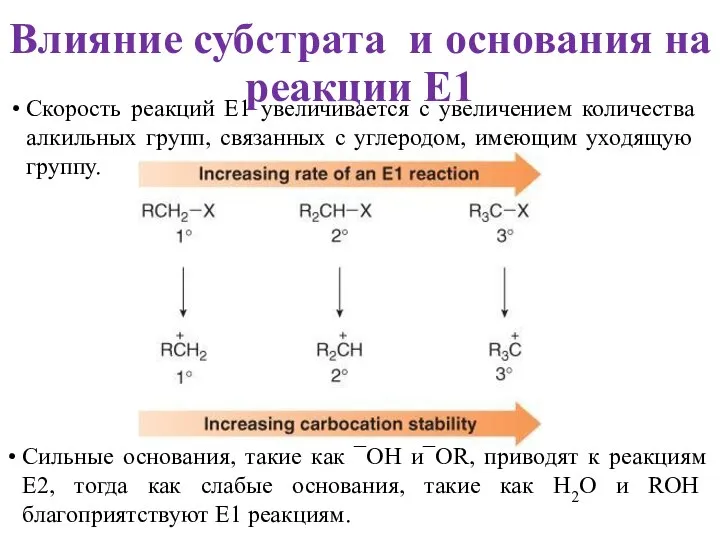
- 20. Скорость реакций E1 увеличивается с увеличением количества алкильных групп, связанных с углеродом, имеющим уходящую группу. Влияние
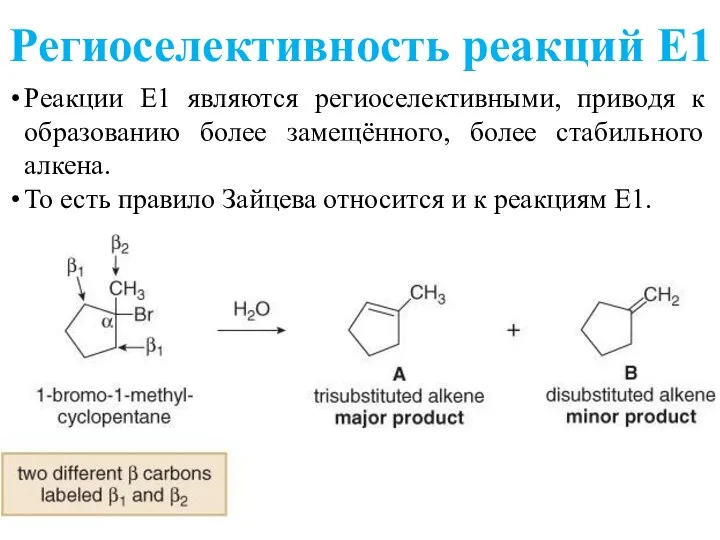
- 21. Региоселективность реакций Е1 Реакции E1 являются региоселективными, приводя к образованию более замещённого, более стабильного алкена. То
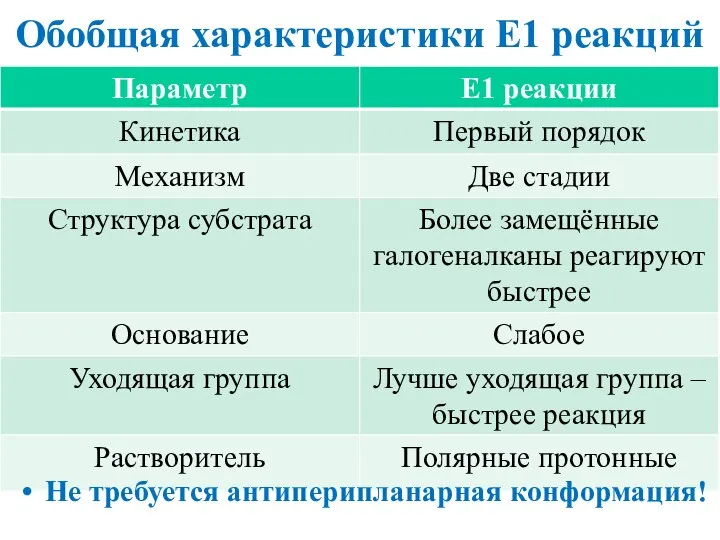
- 22. Обобщая характеристики E1 реакций Не требуется антиперипланарная конформация!
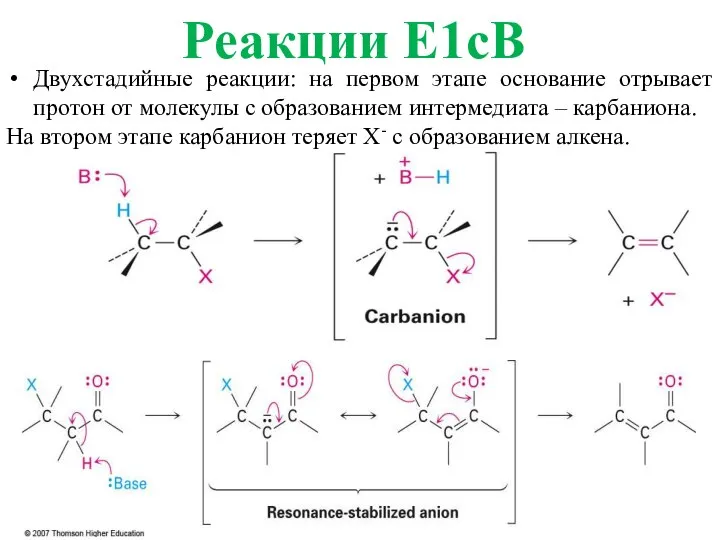
- 23. Реакции E1cB Двухстадийные реакции: на первом этапе основание отрывает протон от молекулы с образованием интермедиата –
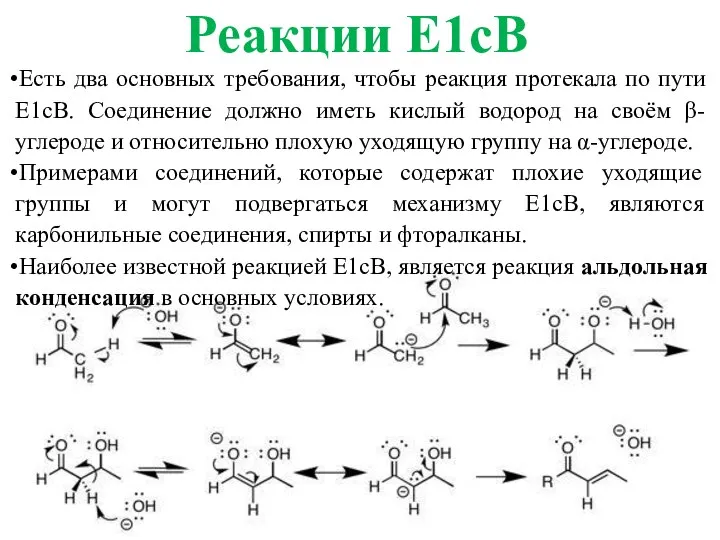
- 24. Есть два основных требования, чтобы реакция протекала по пути E1cB. Соединение должно иметь кислый водород на
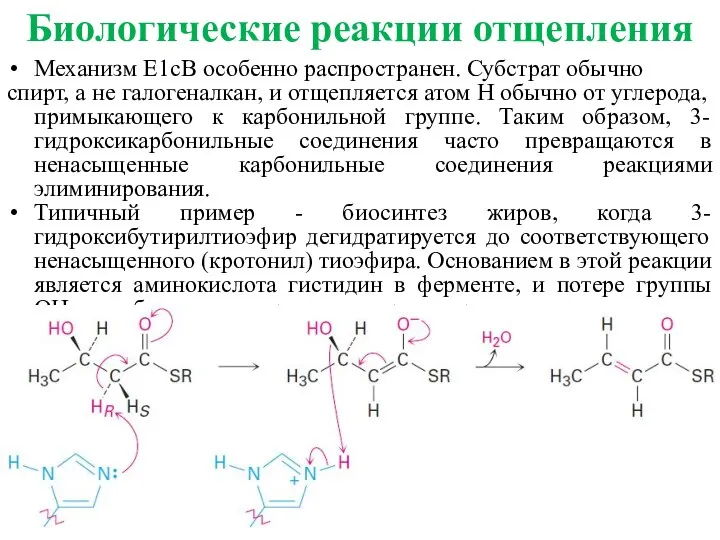
- 25. Механизм E1cB особенно распространен. Субстрат обычно спирт, а не галогеналкан, и отщепляется атом H обычно от
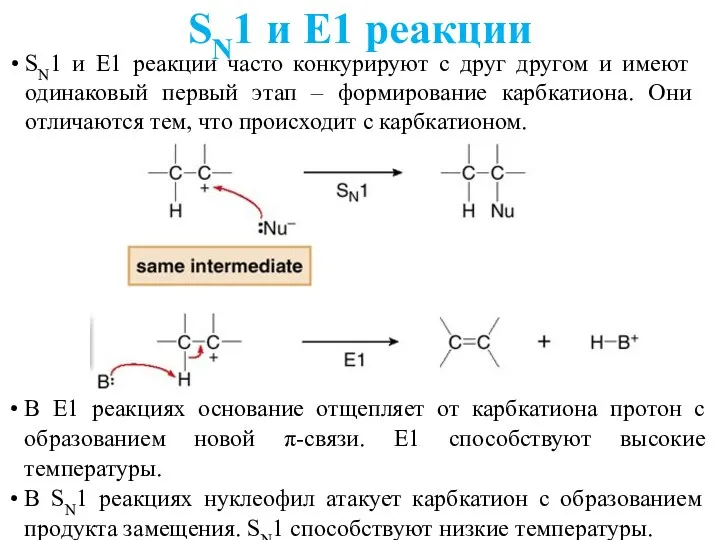
- 26. SN1 и E1 реакции часто конкурируют с друг другом и имеют одинаковый первый этап – формирование
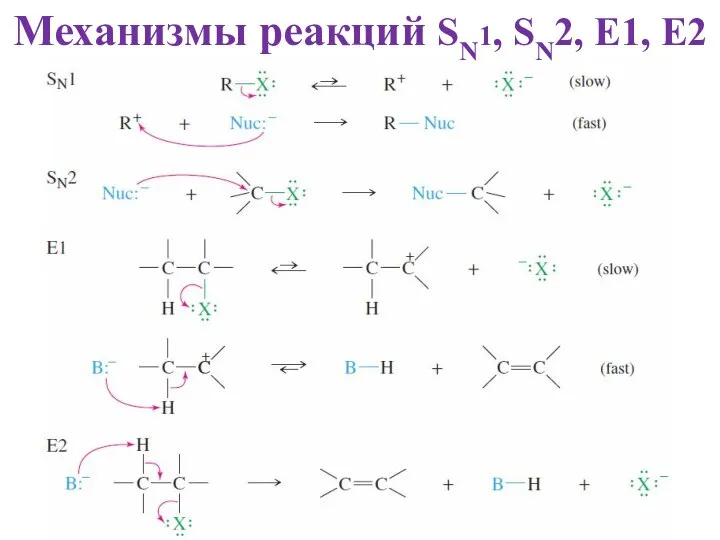
- 27. Механизмы реакций SN1, SN2, E1, E2
- 28. Выбор механизма реакций: SN1, SN2, E1, E2 Необходимо рассмотреть 4 момента: нуклеофил, структура галогеналкана, растворитель, температура
- 29. Выбор механизма реакций: SN1, SN2, E1, E2 Необходимо рассмотреть 4 момента: нуклеофил, структура галогеналкана, растворитель, температура
- 30. Выбор механизма реакций: SN1, SN2, E1, E2 Необходимо рассмотреть 4 момента: нуклеофил, структура галогеналкана, растворитель, температура
- 31. Выбор механизма реакций: SN1, SN2, E1, E2 Необходимо рассмотреть 4 момента: нуклеофил, структура галогеналкана, растворитель, температура
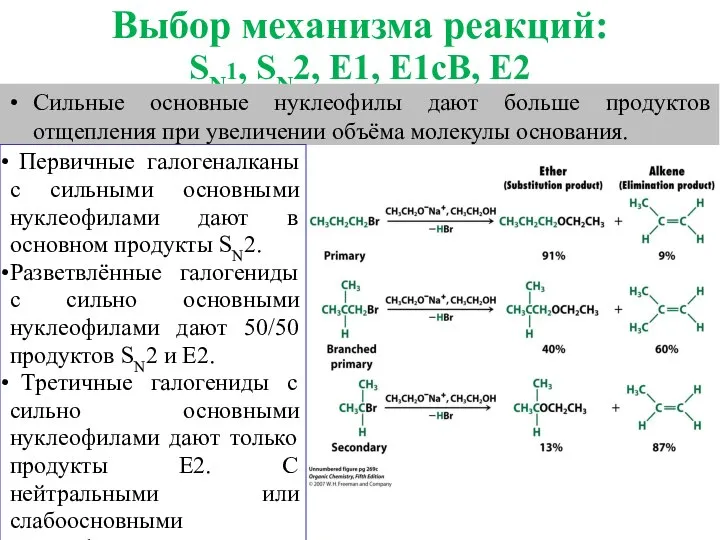
- 32. Выбор механизма реакций: SN1, SN2, E1, E1cB, E2 Сильные основные нуклеофилы дают больше продуктов отщепления при
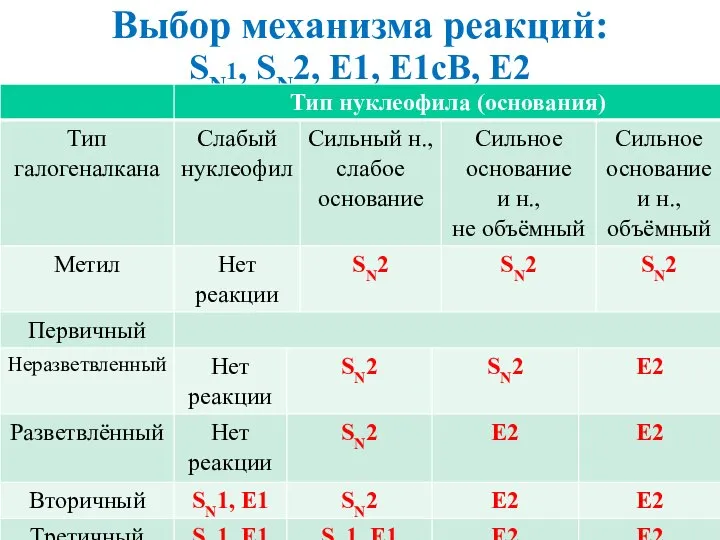
- 33. Выбор механизма реакций: SN1, SN2, E1, E1cB, E2
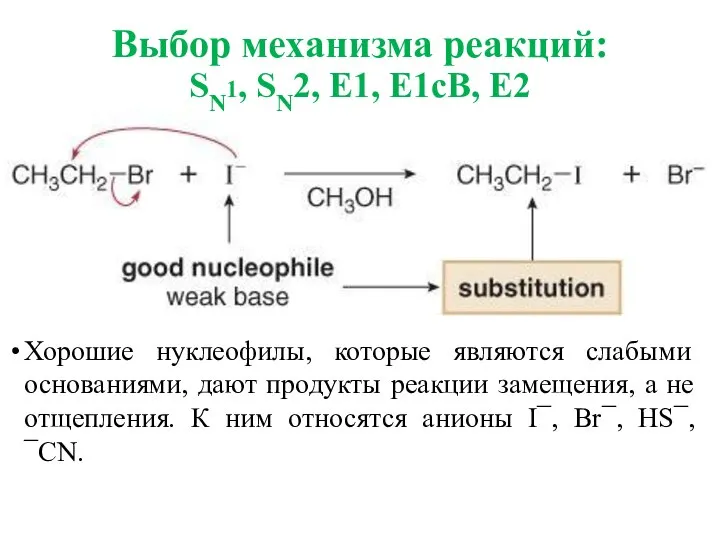
- 34. Хорошие нуклеофилы, которые являются слабыми основаниями, дают продукты реакции замещения, а не отщепления. К ним относятся
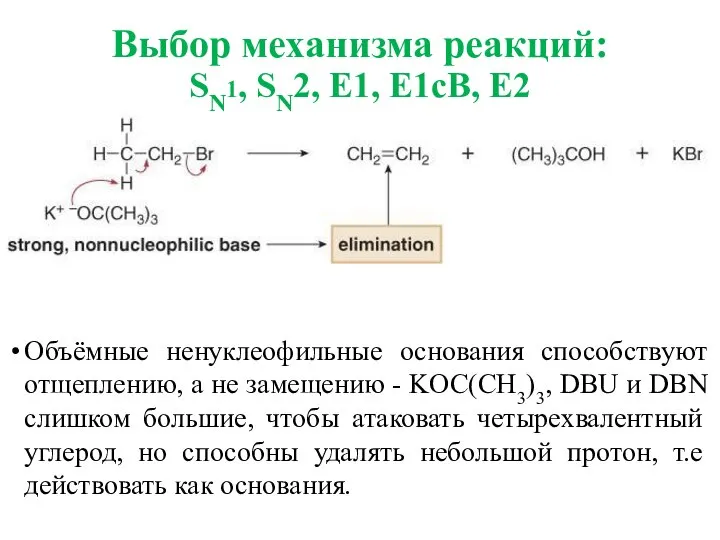
- 35. Объёмные ненуклеофильные основания способствуют отщеплению, а не замещению - KOC(CH3)3, DBU и DBN слишком большие, чтобы
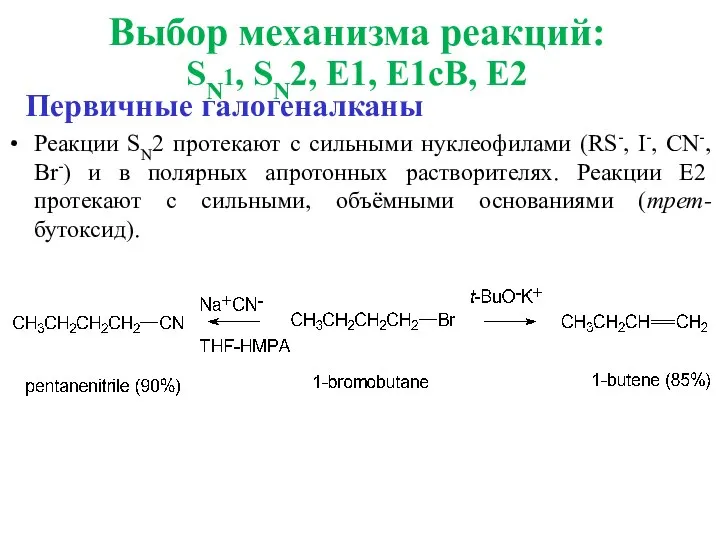
- 36. Первичные галогеналканы Реакции SN2 протекают с сильными нуклеофилами (RS-, I-, CN-, Br-) и в полярных апротонных
- 37. Вторичные галогеналканы Конкурируют SN2 и E2. Если используется слабоосновный и сильный нуклеофил (CH3COO-, Br-, I-) и
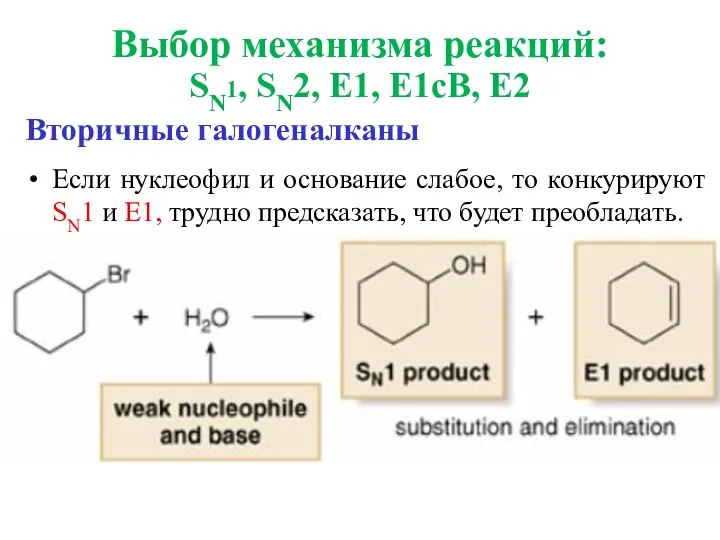
- 38. Вторичные галогеналканы Если нуклеофил и основание слабое, то конкурируют SN1 и E1, трудно предсказать, что будет
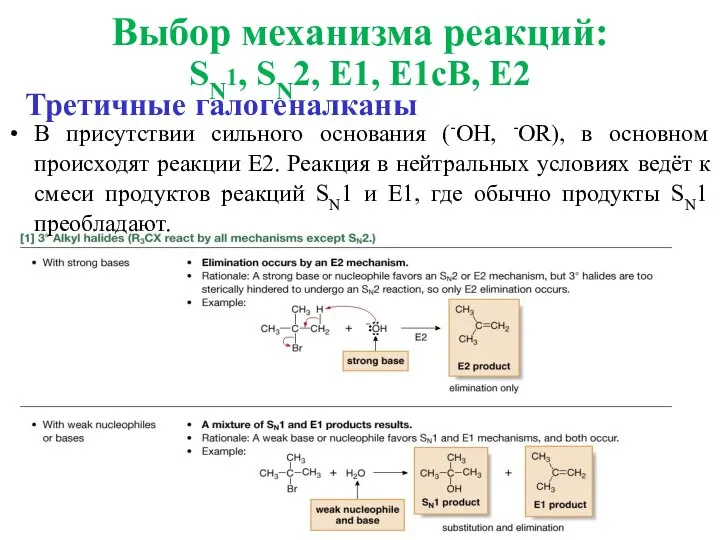
- 39. Третичные галогеналканы В присутствии сильного основания (-OH, -OR), в основном происходят реакции E2. Реакция в нейтральных
- 40. Галоагеналканы вступают в два вида реакций нуклеофильного замещения : SN1 и SN2, и два вида реакций
- 41. Замещение vs. отщепление Помните, что любая частица с парой электронов может в принципе выступать в качестве
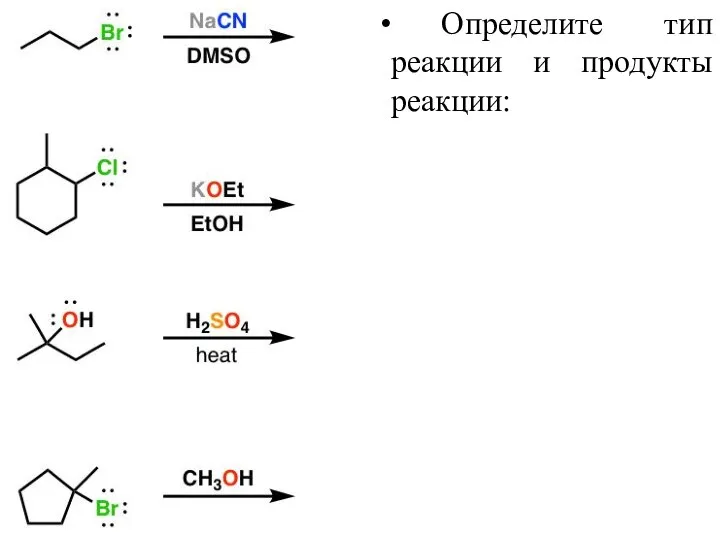
- 43. Определите тип реакции и продукты реакции:
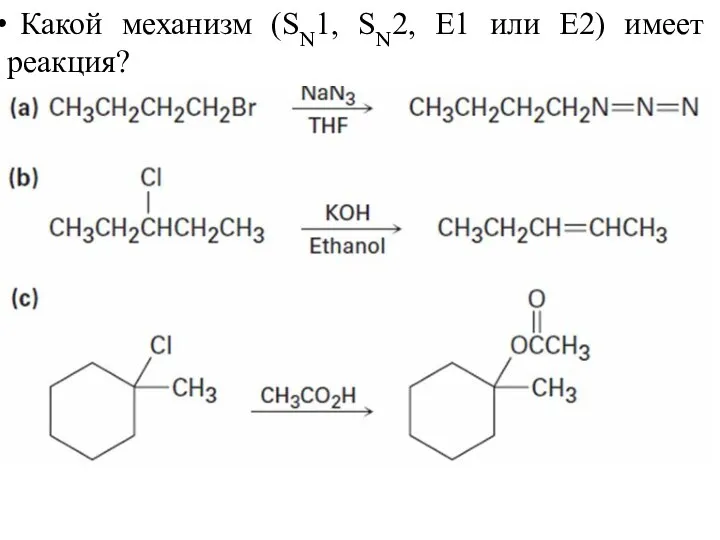
- 44. Какой механизм (SN1, SN2, E1 или E2) имеет реакция?
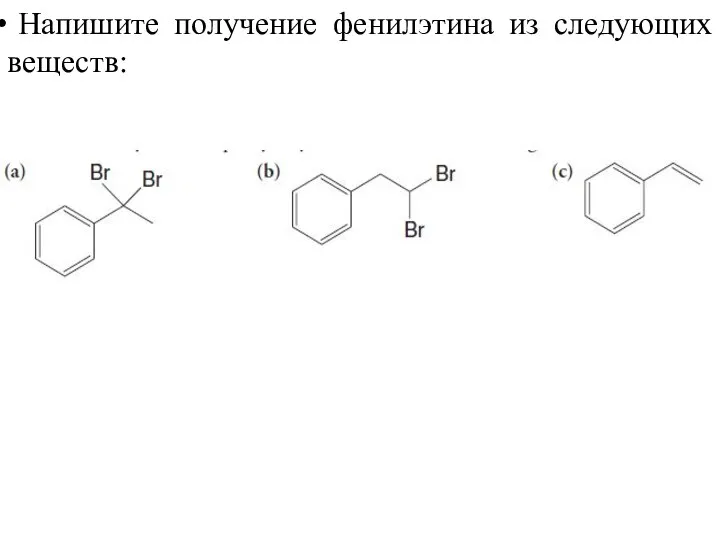
- 45. Напишите получение фенилэтина из следующих веществ:
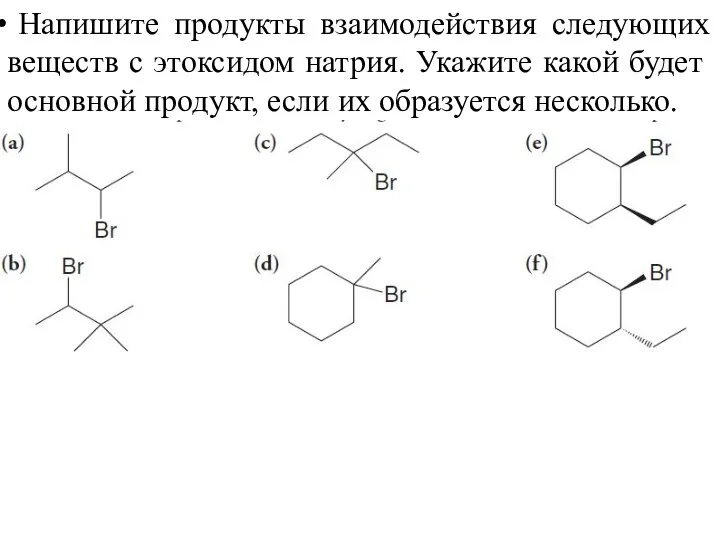
- 46. Напишите продукты взаимодействия следующих веществ с этоксидом натрия. Укажите какой будет основной продукт, если их образуется
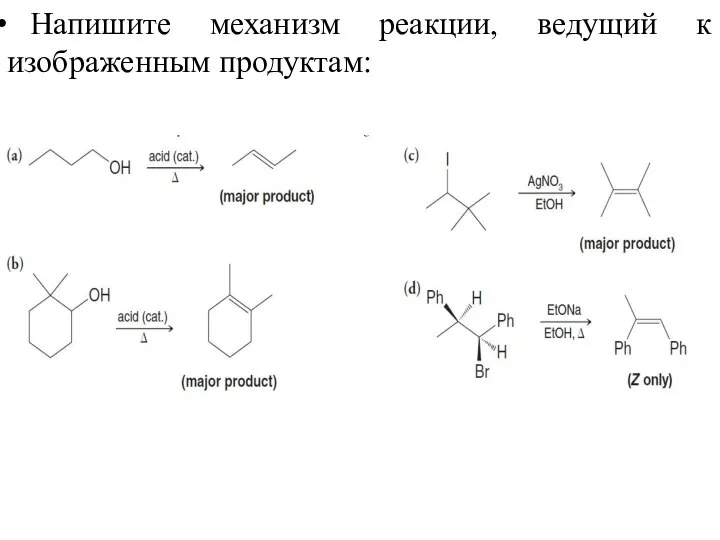
- 47. Напишите механизм реакции, ведущий к изображенным продуктам:
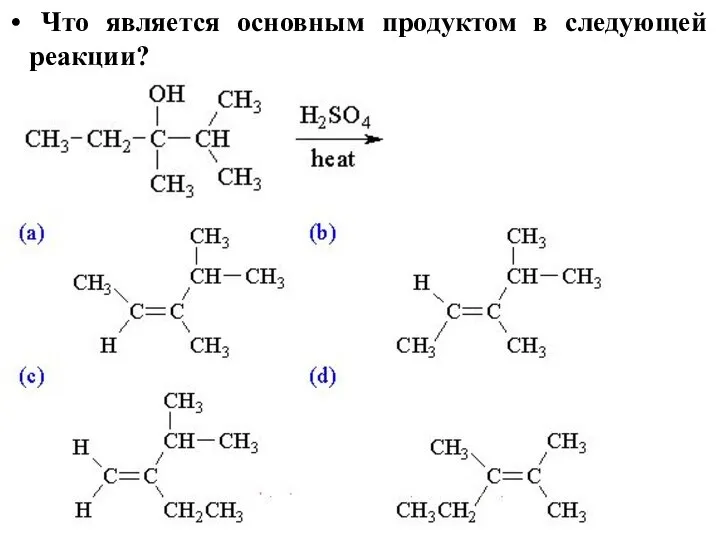
- 48. Что является основным продуктом в следующей реакции?
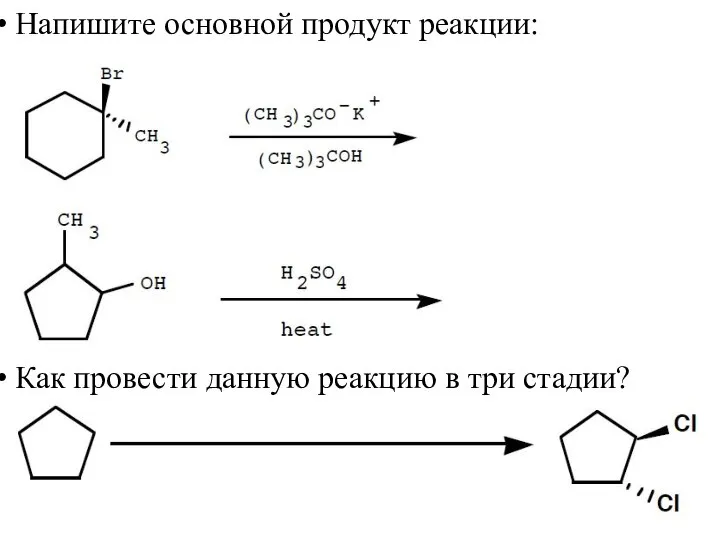
- 49. Напишите основной продукт реакции: Как провести данную реакцию в три стадии?
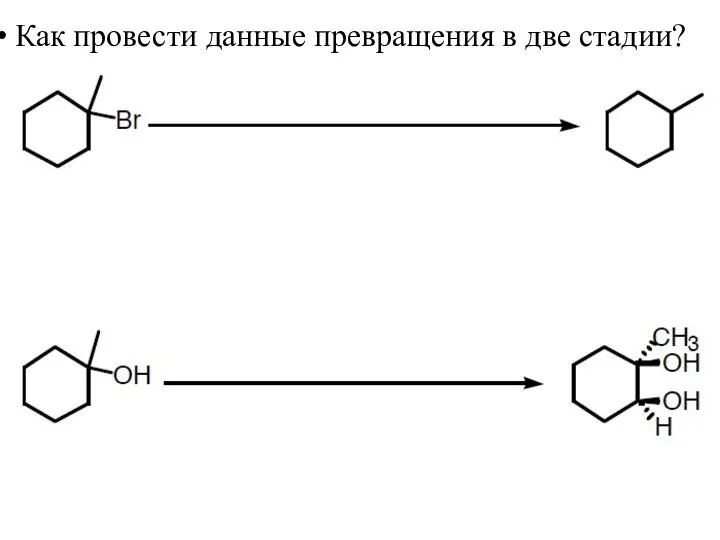
- 50. Как провести данные превращения в две стадии?
- 52. Скачать презентацию



![1,5-диазабицикло[4.3.0]нон-5-ен и 1.8-диазабицикло[5.4.0]ундец-7-ен Объёмные азотистые основания (DBN и DBU)](/_ipx/f_webp&q_80&fit_contain&s_1440x1080/imagesDir/jpg/1161265/slide-8.jpg)

![Реакции E1 имеют кинетику первого порядка: Реакции отщепления E1 Сокрость = k[(CH3)3CCI]](/_ipx/f_webp&q_80&fit_contain&s_1440x1080/imagesDir/jpg/1161265/slide-17.jpg)







 Проточные реакторы непрерывного действия. (Лекция 5)
Проточные реакторы непрерывного действия. (Лекция 5) Нобелевские лауреаты и их достижения
Нобелевские лауреаты и их достижения Общая химическая технология. Составление материального баланса технологического процесса. Практическое занятие 6
Общая химическая технология. Составление материального баланса технологического процесса. Практическое занятие 6 Презентация на тему Генетическая связь между классами неорганических вещ-в
Презентация на тему Генетическая связь между классами неорганических вещ-в  Презентация на тему Количество вещества
Презентация на тему Количество вещества  Установка ЛЧ-35-11/600. Блок Гидроочистки
Установка ЛЧ-35-11/600. Блок Гидроочистки Презентация на тему по химии витамины
Презентация на тему по химии витамины  Химия в загадках
Химия в загадках Вещество как система. Номенклатура неорганических веществ
Вещество как система. Номенклатура неорганических веществ 4505ab8713f54e72bb388461c5e134ac (1)
4505ab8713f54e72bb388461c5e134ac (1) Хімічний експеримент
Хімічний експеримент Презентация на тему Алкены. Строение. Изомерия. Химические свойства
Презентация на тему Алкены. Строение. Изомерия. Химические свойства  Презентация на тему Величие гениального творчества великого соотечественника
Презентация на тему Величие гениального творчества великого соотечественника  Винная кислота
Винная кислота Коррозия металлов. Экзаменационные вопросы
Коррозия металлов. Экзаменационные вопросы Составитель: Денисова В.Г.
Составитель: Денисова В.Г. Изучение процесса замерзания воды
Изучение процесса замерзания воды Сераорганические соединения
Сераорганические соединения Теория химического строения органических веществ А.М. Бутлерова
Теория химического строения органических веществ А.М. Бутлерова Исследование молока
Исследование молока Гетероциклические соединения
Гетероциклические соединения Презентация на тему Скорость химических реакций
Презентация на тему Скорость химических реакций  Металлы и их соединения
Металлы и их соединения Кислородные соединения азота. Оксиды. Кислоты. Соли
Кислородные соединения азота. Оксиды. Кислоты. Соли Виды нагрева и материалы резистивных нагревателей, их стойкость к температуре, ростовой атмосфере и расплаву
Виды нагрева и материалы резистивных нагревателей, их стойкость к температуре, ростовой атмосфере и расплаву Карбид кальция. Назначение
Карбид кальция. Назначение Теоретические основы аналитичесой химии. Общие понятия
Теоретические основы аналитичесой химии. Общие понятия Неметаллы. Агрегатные состояния неметаллов
Неметаллы. Агрегатные состояния неметаллов