Слайд 2
Записати рівняння реакцій, вказати їх типи
SO3 + H2O?
Fe + HCl ?
N2O5 +

H2O?
CaO + HCl?
FeO + H2SO4?
Zn + H2SO4?
BaO + H2O?
KOH + H2SO4?
Fe(OH)3?
Fe + CuSO4?
Слайд 3Запишемо рівняння реакції
Fe +CuSO4 = FeSO4 + Сu

Слайд 4Fe 0+Cu+2 SO4 = Fe +2 SO4 + Сu0
Fe0 - 2e =

Fe+2 Cu+2 + 2e = Cu0
Відновник Окисник
Окиснення Відновлення
Слайд 5Основні поняття
Окиснення — це процес віддачі електрона.
Відновлення — процес прийому електрона.

Атом, що віддає електрони, називається відновником.
Атом, що приймає електрони, називається окисником.
Слайд 6Завдання: допишіть число електронів, яке було „віддане“, або „прийняте“ атомами у схемах
О
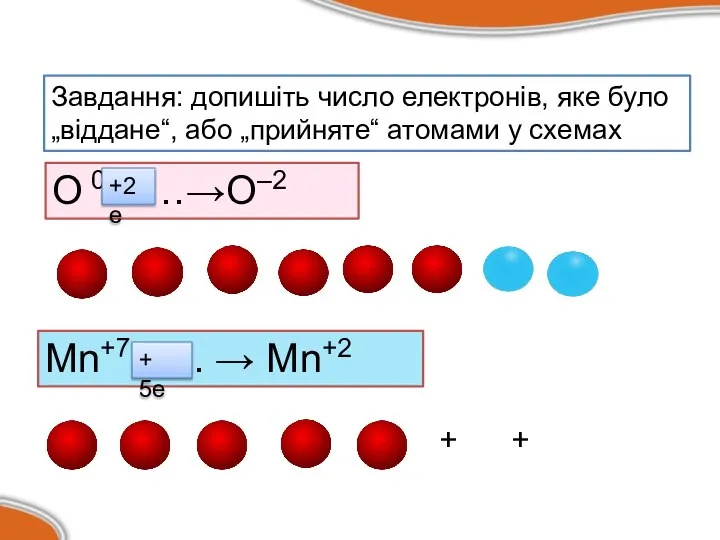
0……→О–2
Mn+7 ….. → Mn+2
+2е
+ 5e





 Химические формулы
Химические формулы 9-8 кислоты в свете ТЭД (1)
9-8 кислоты в свете ТЭД (1) Спирты
Спирты Адсорбционно-десорбционные взаимодействия фосфатов кальция и аминокислот
Адсорбционно-десорбционные взаимодействия фосфатов кальция и аминокислот Соли как производные кислот и оснований
Соли как производные кислот и оснований Интерактивная интеллектуальная игра Юный химик
Интерактивная интеллектуальная игра Юный химик Класс оксиды
Класс оксиды Обобщение знаний об углеводородах
Обобщение знаний об углеводородах ЕГЭ по химии: документы, регламентирующие структуру и содержание контрольных измерительных материалов
ЕГЭ по химии: документы, регламентирующие структуру и содержание контрольных измерительных материалов Предмет химии. Вещества
Предмет химии. Вещества 3bc28ca0711047a6880d20a6763f17db
3bc28ca0711047a6880d20a6763f17db Общая характеристика оксидов
Общая характеристика оксидов Золото
Золото Органическая химия. Ароматические углеводороды
Органическая химия. Ароматические углеводороды Методы получения нафтиридинов (всех изомеров)
Методы получения нафтиридинов (всех изомеров) Нефть и её переработка
Нефть и её переработка Оксид кремния
Оксид кремния Основания: номенклатура, классификация, применение, физические свойства
Основания: номенклатура, классификация, применение, физические свойства Алмаз. Свойства алмазов
Алмаз. Свойства алмазов Презентация на тему Соединения серы
Презентация на тему Соединения серы  Свойства солей, оксидов, оснований
Свойства солей, оксидов, оснований Модель химического образования на основе технологического подхода. Методическая система учителя химии
Модель химического образования на основе технологического подхода. Методическая система учителя химии Техника титрования и лабораторная посуда
Техника титрования и лабораторная посуда Уровень С1 в ГИА
Уровень С1 в ГИА Задачи. Периодическая система. Строение атома. Повторение
Задачи. Периодическая система. Строение атома. Повторение Азотсодержащие гетероциклические соединения пиррол
Азотсодержащие гетероциклические соединения пиррол Предельные углеводороды. Тест 19
Предельные углеводороды. Тест 19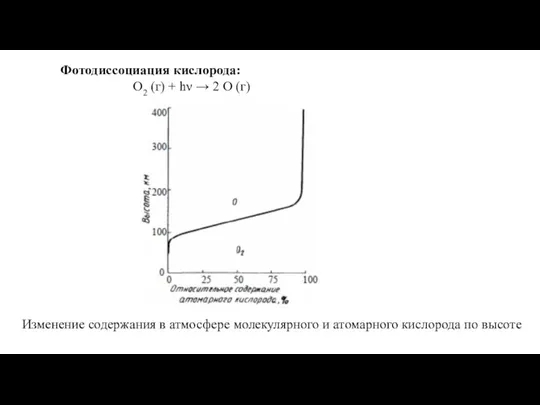 Фотодиссоциация кислорода
Фотодиссоциация кислорода