Слайд 2Эрнест Резерфорд
В 1911 году Эрнест Резерфорд предложил планетарную модель строения атома

Слайд 5Состав ядра
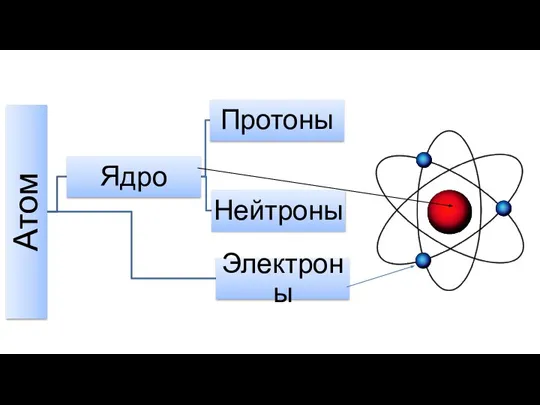
ЯДРО
протоны
нейтроны
ē
ē
ē

Слайд 7А - массовое число
А = Z + N
Z - число протонов
N -

число нейтронов
А = Ar
Р
15
30,97
ФОСФОР
Порядковый
номер
N = A - Z
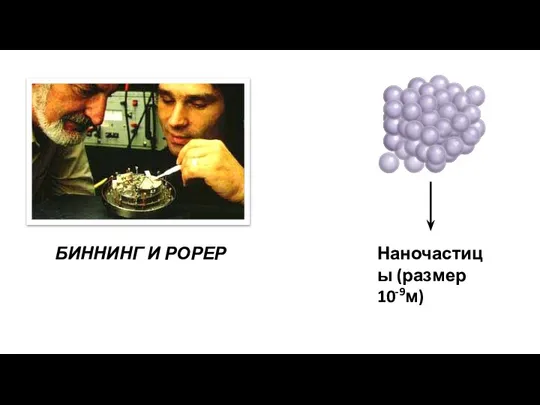
Слайд 8БИННИНГ И РОРЕР
Наночастицы (размер 10-9м)
Слайд 9Вывод
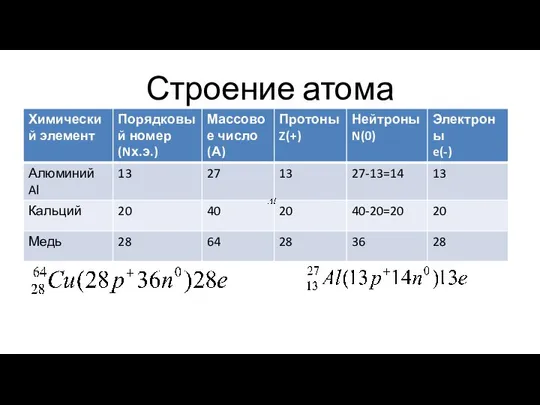
1.Суммарное число протонов и нейтронов в ядре называют массовым
числом. Его обозначают

латинской буквой А.
2.Заряд ядра численно совпадает с порядковым (атомным) номером
элемента (Z) в периодической системе.
3.Массовое число указывают слева вверху от химического знака элемента,
например, а заряд ядра — слева внизу, например
4.Число нейтронов (N) можно вычислить по формуле:
N = А – Z.






 Нобелевские лауреаты и их достижения
Нобелевские лауреаты и их достижения Алканы. Строение,номенклатура, изомерия
Алканы. Строение,номенклатура, изомерия Органическая химия
Органическая химия Презентация на тему Увлекательные факты из жизни Менделеева
Презентация на тему Увлекательные факты из жизни Менделеева  Презентация на тему Изучение реакции среды в зависимости от типа гидролиза соли
Презентация на тему Изучение реакции среды в зависимости от типа гидролиза соли  Растворы электролитов
Растворы электролитов Пятичленные гетероциклы с двумя и более атомами азота
Пятичленные гетероциклы с двумя и более атомами азота Гидролиз солей
Гидролиз солей Скорость химических реакций
Скорость химических реакций Веселый химический КВН
Веселый химический КВН Понятие об ароматических спиртах и фенолах. Особенности строения фенола
Понятие об ароматических спиртах и фенолах. Особенности строения фенола Химическая коррозия
Химическая коррозия Строение атома
Строение атома Проблемы и меры по защите окружающей среды ПМР
Проблемы и меры по защите окружающей среды ПМР Алкены. Гомологический ряд алкенов. Изомерия алкенов
Алкены. Гомологический ряд алкенов. Изомерия алкенов Современные способы защиты ОТТ
Современные способы защиты ОТТ Закон сохранения массы веществ. 8 класс
Закон сохранения массы веществ. 8 класс Криогенный разрыв пласта
Криогенный разрыв пласта Виготовлення водних розчинів з заданою масовою часткою розчиненої речовини
Виготовлення водних розчинів з заданою масовою часткою розчиненої речовини Применение неметаллов
Применение неметаллов Растворение
Растворение алотропні модифікації неметалів
алотропні модифікації неметалів Закон Авогадро. Молярный объём газов
Закон Авогадро. Молярный объём газов Разбор заданий на амины
Разбор заданий на амины Интеллектуальный турнир для старшеклассников Умножая таланты 2020
Интеллектуальный турнир для старшеклассников Умножая таланты 2020 Презентация на тему Теория электролитической диссоциации обобщающий урок
Презентация на тему Теория электролитической диссоциации обобщающий урок  Теория химического строения органических веществ А.М. Бутлерова
Теория химического строения органических веществ А.М. Бутлерова Сода: мифы и реальность
Сода: мифы и реальность