Содержание
- 2. Щелочные металлы — элементы 1-й группы периодической таблицы химических элементов (по устаревшей классификации — элементы главной
- 3. Литий
- 4. Натрий
- 5. Калий
- 6. Рубидий
- 7. Цезий
- 8. Франций
- 9. История открытия щелочных металлов Натрий В 1907 году натрий был впервые получен ученым Гемфри Дэви путем
- 10. История открытия щелочных металлов Калий 19 ноября 1807 года английский химик Дэви сообщил о выделении калия
- 11. Промышленные способы получения натрия Электролиз расплава хлорида натрия : 2NaCl 2Na + Cl2 2. Натрий можно
- 12. Промышленные способы получения калия Калий получают, пропуская пары натрия через расплав хлорида калия при 800°С, выделяющие
- 13. Применение натрия В химической промышленности натрий используется для получения перекиси натрия(на подводных лодках), цианистого натрия, гидрида
- 14. Применение натрия В пищевой отрасли это весьма необходимая для приготовления пищи поваренная соль, в химической отрасли
- 15. Применение калия Львиная часть получаемого промышленностью калия (более 90%) идет на производство калийных удобрений, которые жизненно
- 16. Применения калия В качестве лекарственного средства находит применение иодид калия KI. Иодид калия используют также в
- 17. Признаки отравления щелочными металлами Появление ожога полости рта. Появляется отёчность, ткани меняют цвет на ярко-красный, пострадавший
- 18. Правила первой медицинской помощи при отравлении щелочами Поврежденную ротовую полость и горло необходимо прополоскать. Подойдёт лёгкий
- 20. Правила работы и хранения щелочных металлов Хранят щелочные металлы и работают с ними вдали от воды,
- 21. Правила работы и хранения щелочных металлов Все работы с щелочными металлами проводятся с применением средств индивидуальной
- 22. Правила работы и хранения щелочных металлов Пинцетом вынимают из банки кусок металла, помещают его в заполненную
- 23. Утилизация щелочных металлов Литий - Небольшие твердые кусочки размером с горошину растворяют в большом количестве холодной
- 24. !!! Все процедуры по утилизации рекомендуется осуществлять в вытяжном шкафу при закрытых створках. Также нелишним будет
- 26. Скачать презентацию























 Химические уравнения. 8 класс
Химические уравнения. 8 класс Коррозия металлов
Коррозия металлов Нітратна кислота Презентація вчителя хімії Смілянської загальноосвітньої школи І-ІІІ ст. № 11 Л.В.Заруби
Нітратна кислота Презентація вчителя хімії Смілянської загальноосвітньої школи І-ІІІ ст. № 11 Л.В.Заруби Углеводы
Углеводы Окислительно-восстановительные реакции
Окислительно-восстановительные реакции Презентация на тему Процессы в растворах электролитическая диссоциация
Презентация на тему Процессы в растворах электролитическая диссоциация  Коррозия металлов
Коррозия металлов Основания. 8 класс
Основания. 8 класс Химические соединения в живых организмах. Неорганические вещества
Химические соединения в живых организмах. Неорганические вещества Общие химические свойства металлов
Общие химические свойства металлов Презентация на тему Соли
Презентация на тему Соли  Классификация реакций и реагентов. Кислотные и основные свойства биомолекул
Классификация реакций и реагентов. Кислотные и основные свойства биомолекул Характеристика углерода
Характеристика углерода Комплексные соединения
Комплексные соединения Спирты и фенолы
Спирты и фенолы Средства для мытья окон
Средства для мытья окон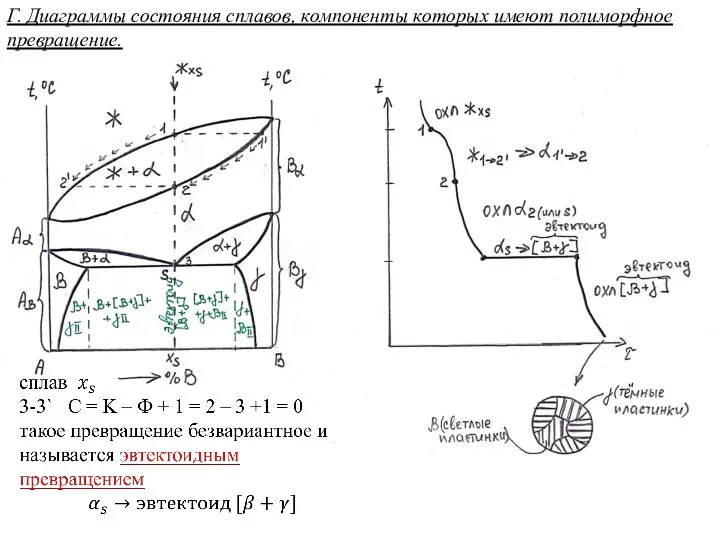 Диаграммы состояния сплавов, компоненты которых имеют полиморфное превращение
Диаграммы состояния сплавов, компоненты которых имеют полиморфное превращение Термодинамика. Лекция №2
Термодинамика. Лекция №2 Новейшие достижения в области высокомолекулярных соединений
Новейшие достижения в области высокомолекулярных соединений Химия, химия, химия!
Химия, химия, химия! Изомерия аминокислот
Изомерия аминокислот Структура периодической таблицы
Структура периодической таблицы Ионные уравнения реакций
Ионные уравнения реакций Тема урока: «Свойства тканей из химических волокон»
Тема урока: «Свойства тканей из химических волокон» Строение атома алюминия. Физические и химические свойства алюминия
Строение атома алюминия. Физические и химические свойства алюминия Аммиак. Соли аммония
Аммиак. Соли аммония Тесты для самопроверки
Тесты для самопроверки Кислоты в химии
Кислоты в химии