Слайд 2Цели урока.
Познакомить учащихся с составом, названиями, классификацией и представителями класса кислот.
Продолжить знакомство

со сложными ионами на примере кислотных остатков кислородных кислот.
Продолжить формирование знаний о различиях между зарядами ионов и с.о. элементов, об индикаторах.
Слайд 3Актуализация опорных ЗУНов.
Что называется основаниями?
Какие реакции называются качественными?
Как изменяют окраску индикаторы в

щелочной среде?
Работа по группам:
1 группа – проверочная робота по теме «Основания».
2 группа – по учебнику выполнить упр 4, 6 стр. 70.
Слайд 4Развитие новых ЗУНов
Попробуйте кристаллики лимонной кислоты на вкус.
Он кислый, отсюда

и название класса (кислоты).
Но ни один химик и не один грамотный человек даже и не подумает распознавать таким образом кислоты –это может быть смертельно опасно!
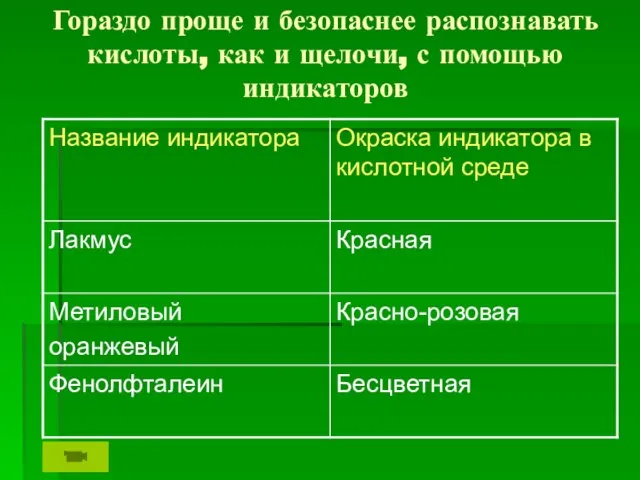
Слайд 5Гораздо проще и безопаснее распознавать кислоты, как и щелочи, с помощью индикаторов
Слайд 6Кислоты
HCL – хлороводородная (соляная)
HNO3 - азотная
HNO2 - азотистая
H2SO4 - серная
H2SO3 - сернистая
H2S

- сероводородная
H3PO4 - фосфорная
H2CO3 - угольная
H2SiO3 - кремниевая
HBr - бромоводородная
HI - иодоводородная
HF – фтороводородная (плавиковая)
Слайд 7Кислоты – это сложные вещества, молекулы которых состоят из атомов водорода и

кислотных остатков
Слайд 8Классификация кислот
По числу атомов водорода:
а) одноосновные – HCL, HNO3, HNO2, HBr, HI,
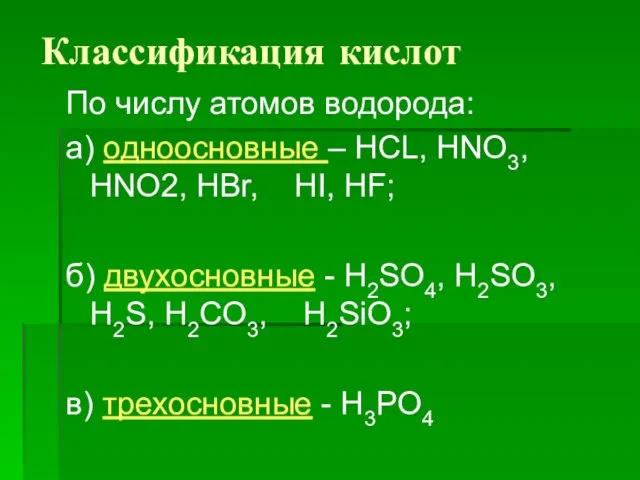
HF;
б) двухосновные - H2SO4, H2SO3, H2S, Н2CO3, H2SiO3;
в) трехосновные - H3PO4
Слайд 9 По наличию атомов кислорода в кислотных остатках:
а) кислородсодержащие - HNO3, HNO2,

H2SO4, H2SO3, Н2CO3, H3PO4, H2SiO3;
б) бескислородные - HCL, HBr, H2S.
Слайд 10По признаку растворимости:
а) растворимые - HNO3, HNO2, H2SO4, H2SO3, Н2CO3, H3PO4,

HCL, HBr, H2S;
б) нерастворимые - H2SiO3.
Слайд 11Степени окисления элементов и заряды ионов кислот
Кислоты это своеобразный мостик, который связывает

полярную ковалентную связь с ионной.
В растворах между водородом и кислотным остатком ковалентная связь переходит в ионную.
Кислоты образуют ионы двух видов: простые – ионы водорода Н+ и сложные – ионы кислотного остатка (SO42-, NO3-, PO43-)
Слайд 12Отличия между степенью окисления и зарядом иона.
Число видов степени окисления элементов

в соединениях равно числу элементов в составе вещества, число видов ионов равно числу частей вещества. Так, для H2SO4:
а) заряды ионов H2+SO42-;
б) с.о. элементов H2+1S+6O42-.
Слайд 13Представители кислот.
Техника безопасности при работе с кислотами.
HCL – хлороводородная (соляная)
HNO3 – азотная
H2SO4

- серная
Слайд 14Развитие новых ЗУНов.
Определите для кислоты: а) заряды ионов; б) с.о. элементов; в)

соответствующий ей оксид.
2. Какое количество вещества содержится в













 Типы химической связи
Типы химической связи Прикладная геохимия
Прикладная геохимия Чистые вещества и смеси
Чистые вещества и смеси Классификация сложных неорганических веществ. Оксиды
Классификация сложных неорганических веществ. Оксиды Минералы. Сокровища земли. Ко дню геолога
Минералы. Сокровища земли. Ко дню геолога Тест 1 задание
Тест 1 задание Химическое равновесие
Химическое равновесие Презентация на тему Виды химической связи и типы кристаллических решеток
Презентация на тему Виды химической связи и типы кристаллических решеток  Учебное задание Расчет теплоты сгорания
Учебное задание Расчет теплоты сгорания Презентация на тему Полезная химия во фруктах и овощах
Презентация на тему Полезная химия во фруктах и овощах  Донорно-акцепторный механизм образование связи
Донорно-акцепторный механизм образование связи Консультация по химии
Консультация по химии Нефть и продукты ее переработки. Лабораторная работа
Нефть и продукты ее переработки. Лабораторная работа Методы защиты металлов от электрохимической коррозии. Классификация методов защиты
Методы защиты металлов от электрохимической коррозии. Классификация методов защиты Кислотно-основные равновесия
Кислотно-основные равновесия Природный газ
Природный газ Сера
Сера Структура електронної оболонки атома. Енергетичні рівні та підрівні
Структура електронної оболонки атома. Енергетичні рівні та підрівні Генетическая связь между классами неорганических веществ
Генетическая связь между классами неорганических веществ Атомы. Нахождение в природе
Атомы. Нахождение в природе Оксиды и гидрооксиды
Оксиды и гидрооксиды 9-12 Гидролиз солей -
9-12 Гидролиз солей - Презентация на тему Неметаллы
Презентация на тему Неметаллы  Стекло
Стекло Карбоцепные полимеры
Карбоцепные полимеры Полиэтилен. Получение полиэтилена
Полиэтилен. Получение полиэтилена Группа веществ, требующих особых методов изолирования. Характеристика соединений. Токсикологическое значение
Группа веществ, требующих особых методов изолирования. Характеристика соединений. Токсикологическое значение Применение личностно-ориентированного подхода в обучении химии
Применение личностно-ориентированного подхода в обучении химии