Содержание
- 2. это процессы, в результате которых из одних веществ образуются другие, отличающиеся от них по составу и
- 3. По числу и составу реагирующих и образующихся веществ По изменению степени окисления атомов элементов По использованию
- 4. I. По числу и составу реагирующих и образующихся веществ: Реакции, идущие без изменения состава веществ. В
- 5. Реакции, идущие с изменением состава вещества 1. Реакции соединения – реакции, при которых из двух и
- 6. 2. Реакции разложения – это такие реакции, при которых из одного сложного вещества образуется несколько новых
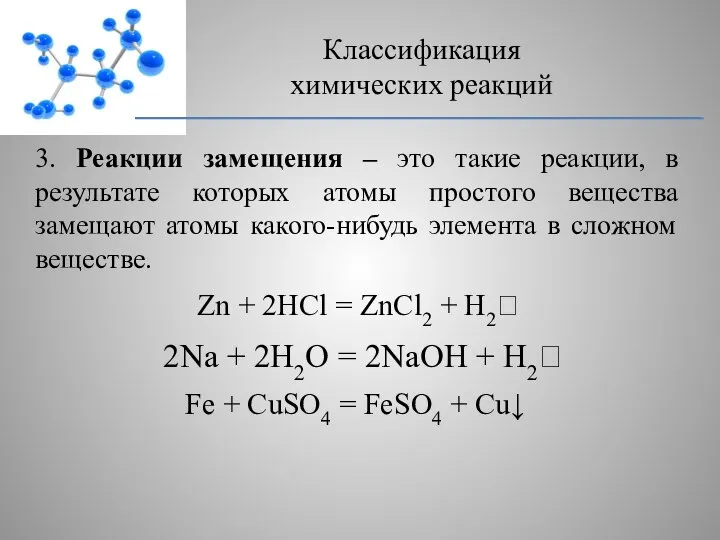
- 7. 3. Реакции замещения – это такие реакции, в результате которых атомы простого вещества замещают атомы какого-нибудь
- 8. 4. Реакции обмена – это такие реакции, при которых два сложных вещества обмениваются своими составными частями.
- 9. II. По изменению степеней окисления химических элементов: Окислительно-восстановительные реакции – реакции, идущие с изменением степеней окисления
- 10. III. По использованию катализатора: 1. Некаталитические реакции – реакции, идущие без участия катализатора: Классификация химических реакций
- 11. III. По использованию катализатора: 1. Каталитические реакции – реакции, идущие с участием катализатора: Классификация химических реакций
- 12. IV. По направлению действия: 1. Необратимые реакции протекают в данных условиях только в одном направлении: Классификация
- 13. V. По тепловому эффекту: 1. Экзотермические реакции протекают с выделением энергии: Классификация химических реакций 4P +
- 14. V. По тепловому эффекту: 2. Эндотермические реакции протекают с поглощением энергии: Классификация химических реакций N2 +
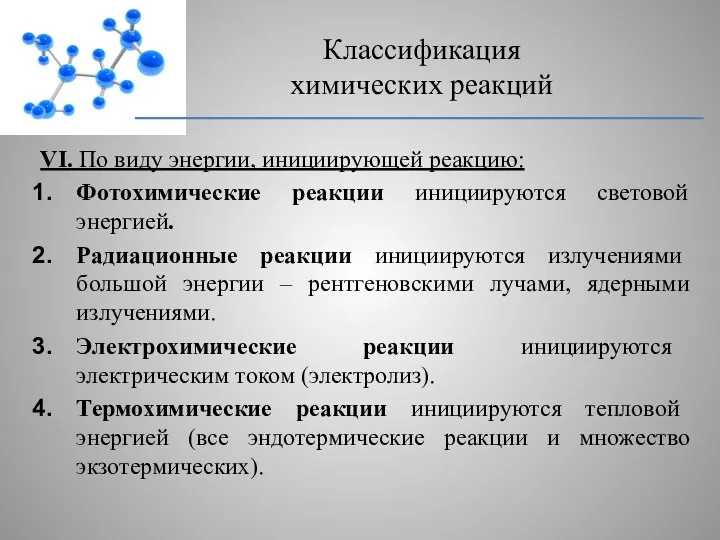
- 15. VI. По виду энергии, инициирующей реакцию: Фотохимические реакции инициируются световой энергией. Радиационные реакции инициируются излучениями большой
- 16. VII. По фазовому составу: 1. Гетерогенные реакции – реакции, в которых реагирующие вещества и продукты находятся
- 17. VIII. По фазовому составу: 2. Гомогенные реакции – реакции, в которых реагирующие вещества и продукты находятся
- 19. Скачать презентацию














 Понятие о химической реакции. Реакции, идущие без изменения состава веществ. 11 класс
Понятие о химической реакции. Реакции, идущие без изменения состава веществ. 11 класс Обсидиан
Обсидиан Основные классы неорганических соединений (урок - семинар)
Основные классы неорганических соединений (урок - семинар)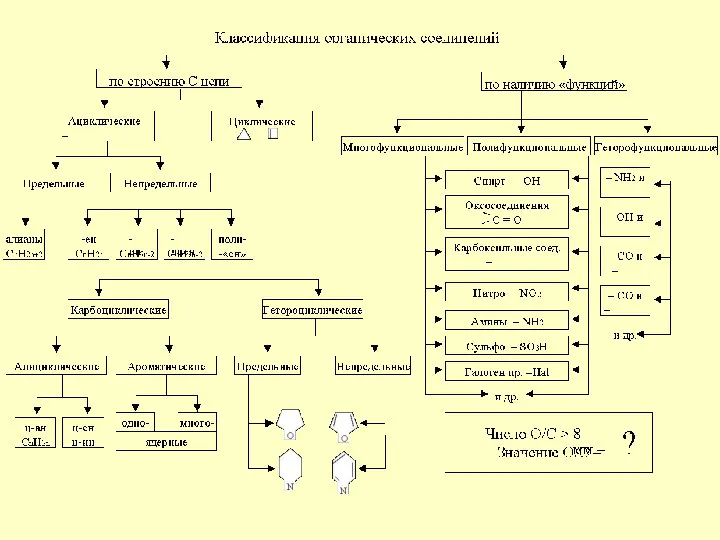 Классификация органических соединений
Классификация органических соединений Строение электронных оболочек атомов химических элементов
Строение электронных оболочек атомов химических элементов Химические процессы на кухне (урок №7)
Химические процессы на кухне (урок №7) Галогены. Элементы главной подгруппы 7 группы Периодической системы Менделеева
Галогены. Элементы главной подгруппы 7 группы Периодической системы Менделеева Применение хидких кристалов в промышленности
Применение хидких кристалов в промышленности Ministry of Education and Science of the Russian Federation
Ministry of Education and Science of the Russian Federation Презентация на тему Угарный газ
Презентация на тему Угарный газ  Prezentatsia1 (1)
Prezentatsia1 (1) Медиатехнологии на уроках химии
Медиатехнологии на уроках химии Классификация оксидов
Классификация оксидов Соли, их классификация и свойства
Соли, их классификация и свойства Соли азотной кислоты – нитраты. 9 класс
Соли азотной кислоты – нитраты. 9 класс Фракционный состав нефти. Химический состав нефти
Фракционный состав нефти. Химический состав нефти Алкадиены
Алкадиены Комплексные соединения
Комплексные соединения Анализ образцов колбасных изделий, образцов бытовой химии, напитков
Анализ образцов колбасных изделий, образцов бытовой химии, напитков Спирты. Классификация, изомерия
Спирты. Классификация, изомерия Особенности решения практикоориентированного задания №26 ГИА-11
Особенности решения практикоориентированного задания №26 ГИА-11 Учебно-познавательные задачи на уроках химии
Учебно-познавательные задачи на уроках химии Карбоновые кислоты
Карбоновые кислоты Теоретические основы органической химии
Теоретические основы органической химии относительная атомная масса
относительная атомная масса Разбор ДЗ. Титрование – общие моменты
Разбор ДЗ. Титрование – общие моменты Тест по химии
Тест по химии Презентация 1
Презентация 1