Содержание
- 4. Открытие Ломоносова в создании атомно-молекулярного учения Михаил Васильевич Ломоносов в XVIII в. разработал учение о молекулах
- 5. Открытие Дальтона в создании атомно-молекулярного учения Дальнейшее развитие эта теория получила в трудах Д. Дальтона. В
- 6. Таблица атомов Дальтона
- 7. Модель Атома
- 9. Скачать презентацию
Слайд 4Открытие Ломоносова в создании атомно-молекулярного учения
Михаил Васильевич Ломоносов в XVIII в. разработал
Открытие Ломоносова в создании атомно-молекулярного учения
Михаил Васильевич Ломоносов в XVIII в. разработал

учение о молекулах и атомах:
• утверждал что тела в природе состоят из корпускул (молекул) , в состав которых входят неделимые элементы (атомы) .
• Многообразие веществ объяснял соединением разных атомов в молекулах и различным расположением атомов в них.
• Предполагал, что некоторые молекулы могут состоять из одинаковых атомов.
Слайд 5Открытие Дальтона в создании атомно-молекулярного учения
Дальнейшее развитие эта теория получила в трудах
Открытие Дальтона в создании атомно-молекулярного учения
Дальнейшее развитие эта теория получила в трудах

Д. Дальтона. В 1808 году английский химик Дальтон сформулировал атомистическую теорию.
• Утверждал, что все вещества состоят из атомов, мельчайших неделимых частиц, которые не могут быть ни созданы, ни уничтожены. Ввёл понятие атомного веса.
• Дальтон считал, что все атомы одного итого же элемента совершенно идентичны, например, имеют одинаковые массы.
• На основе химических законов (закон кратных отношений, закон эквивалентов и закон постоянства состава) создал атомистическую теорию, основанную на количественных соотношениях, возникающих при взаимодействии между химическими элементами. Основы используются до сих пор.
Открытие в XX веке изотопов и ядерных реакций внесло изменения в атомистическую теорию Дальтона.
Слайд 6 Таблица атомов Дальтона
Таблица атомов Дальтона

Слайд 7 Модель Атома
Модель Атома



 Химическое равновесие
Химическое равновесие Химия и география. Блиц-опрос. 7 класс
Химия и география. Блиц-опрос. 7 класс Амилаза. Строение амилазы
Амилаза. Строение амилазы Моющие и чистящие средства
Моющие и чистящие средства Основные химические законы
Основные химические законы Соли: получение
Соли: получение Синтетическое моторное масло. Маркировка моторных масел
Синтетическое моторное масло. Маркировка моторных масел Khim_8
Khim_8 Химические реакции
Химические реакции Систематизация знаний по периодической системе химических элементов
Систематизация знаний по периодической системе химических элементов химия
химия Nevarne snovi
Nevarne snovi Основания. Классификация
Основания. Классификация Стелс-материалы
Стелс-материалы Тип кристаллической решетки у белого фосфора…. Тест
Тип кристаллической решетки у белого фосфора…. Тест Классификация и свойства кислот
Классификация и свойства кислот Сeквенирование нуклеиновых кислот
Сeквенирование нуклеиновых кислот Набор для выращивания монокристалла. Защита проекта
Набор для выращивания монокристалла. Защита проекта Алканы. Строение, номенклатура, изомерия, физические свойства
Алканы. Строение, номенклатура, изомерия, физические свойства Реакции разложения и соединения
Реакции разложения и соединения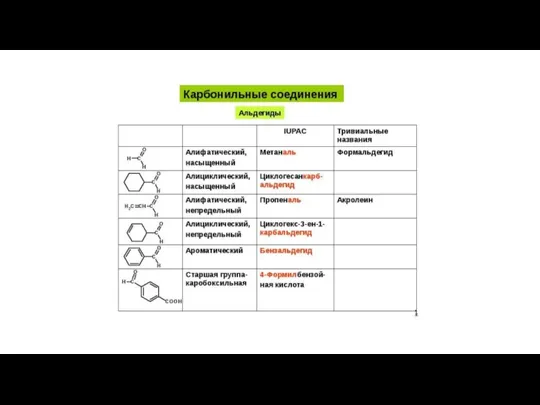 Карбонильные соединения (альдегиды)
Карбонильные соединения (альдегиды) карбоновые кислоты
карбоновые кислоты Вуглеводи. Групи
Вуглеводи. Групи Вычисление температур стеклования полимера при различных степенях отверждения смолы
Вычисление температур стеклования полимера при различных степенях отверждения смолы Сера
Сера Валенттілік. Атом-молекулалы ілім
Валенттілік. Атом-молекулалы ілім Классификация органических соединений
Классификация органических соединений Метанол. Краткая характеристика
Метанол. Краткая характеристика