Содержание
- 2. Индуктивный эффект +I, -I 1. Индуктивный эффект быстро затухает (на четвертый атом почти не влияет) знаки
- 3. Индуктивный эффект +I, -I 2. Влияние нескольких заместителей суммируется (но не аддитивно) 3. Чем больше ЭО,
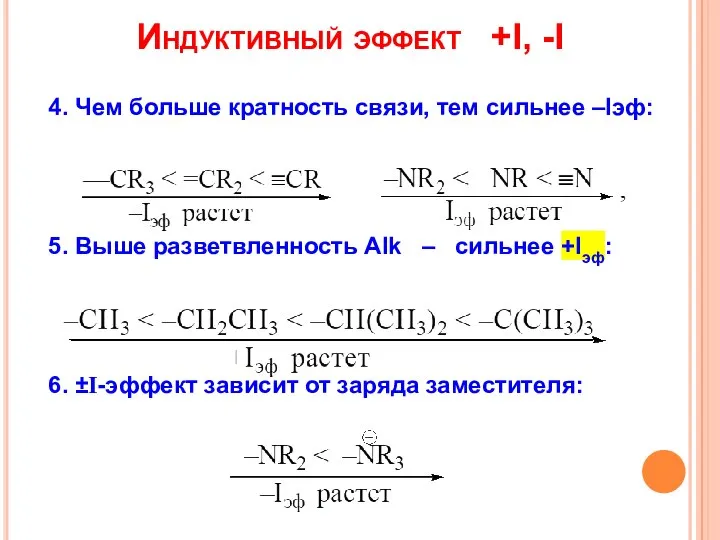
- 4. Индуктивный эффект +I, -I 4. Чем больше кратность связи, тем сильнее –Iэф: 5. Выше разветвленность Alk
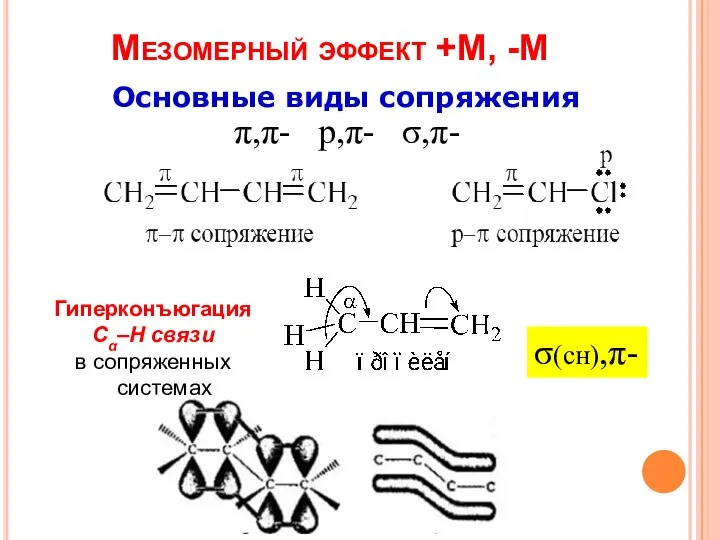
- 5. Мезомерный эффект +М, -М Основные виды сопряжения π,π- р,π- σ,π- σ(сн),π- Гиперконъюгация Cα–H связи в сопряженных
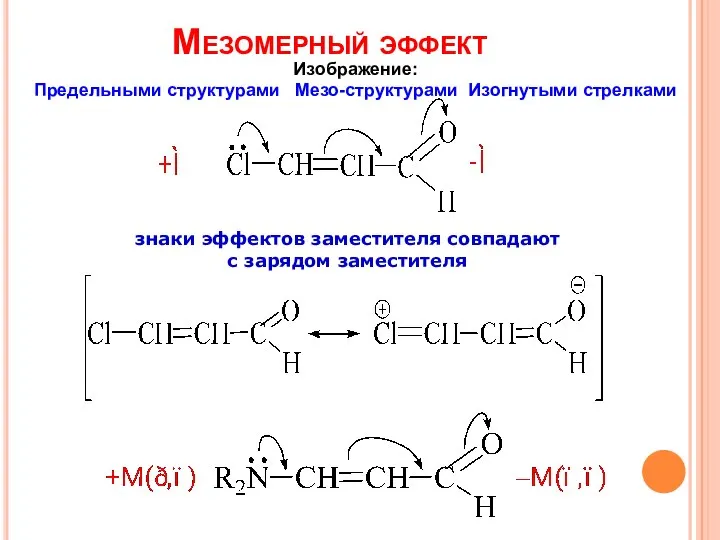
- 6. Мезомерный эффект знаки эффектов заместителя совпадают с зарядом заместителя Изображение: Предельными структурами Мезо-структурами Изогнутыми стрелками
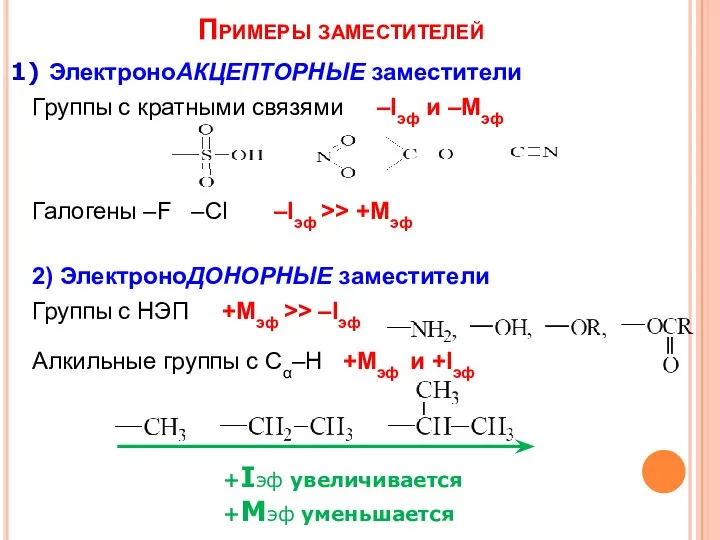
- 7. Примеры заместителей 1) ЭлектроноАКЦЕПТОРНЫЕ заместители Группы с кратными связями –Iэф и –Мэф Галогены –F –Cl –Iэф
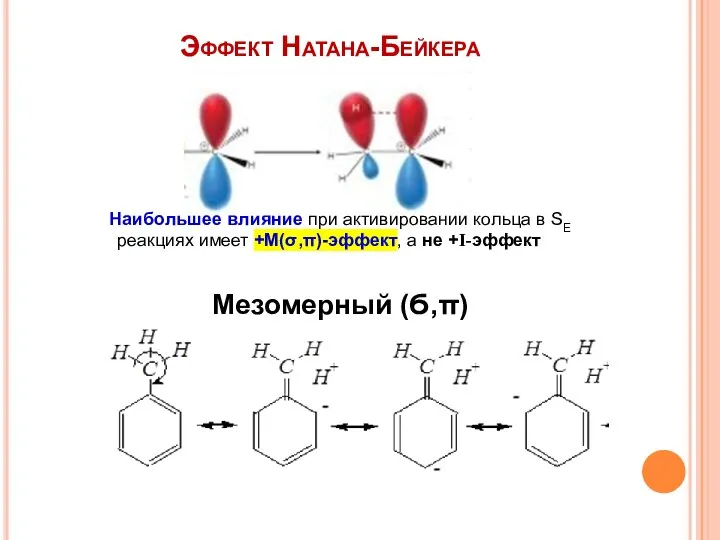
- 8. Эффект Натана-Бейкера Наибольшее влияние при активировании кольца в SE реакциях имеет +М(σ,π)-эффект, а не +I-эффект Мезомерный
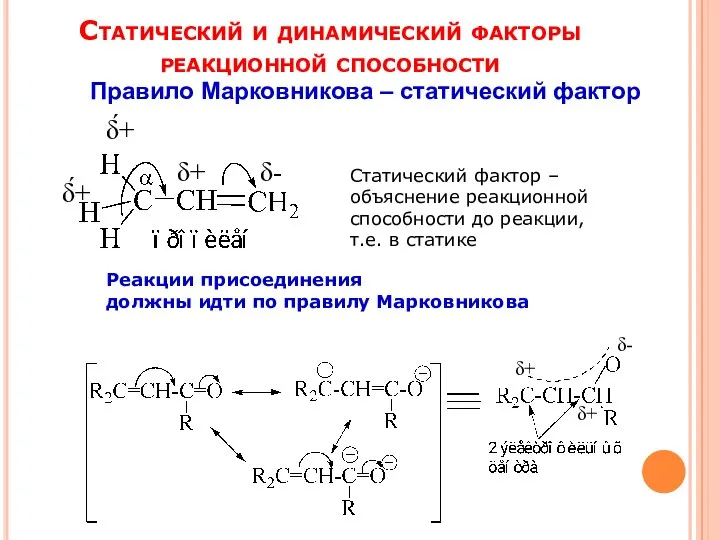
- 9. Статический и динамический факторы реакционной способности δ- δ+ δ́+ δ́+ Статический фактор – объяснение реакционной способности
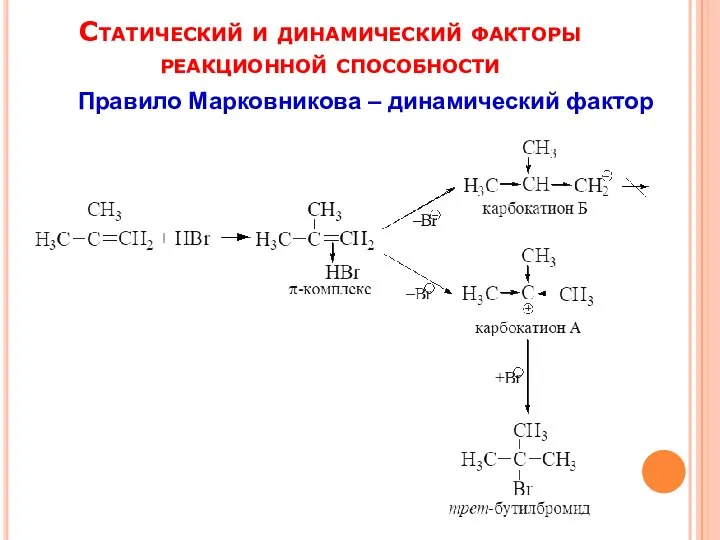
- 10. Статический и динамический факторы реакционной способности Правило Марковникова – динамический фактор
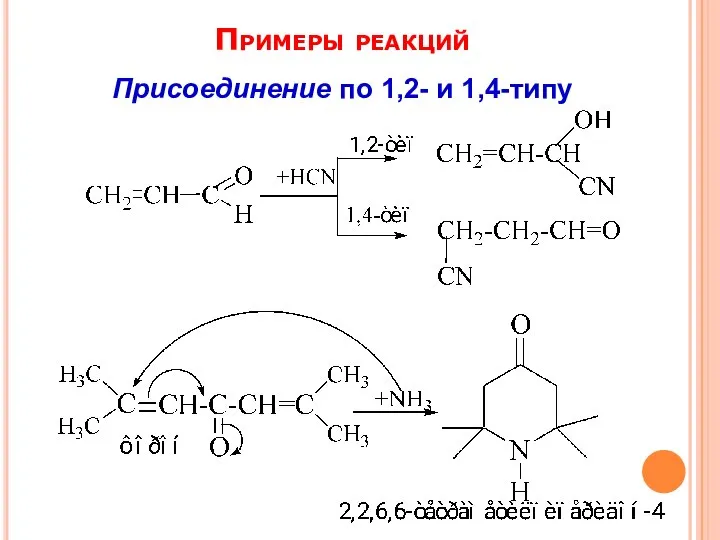
- 11. Примеры реакций Присоединение по 1,2- и 1,4-типу
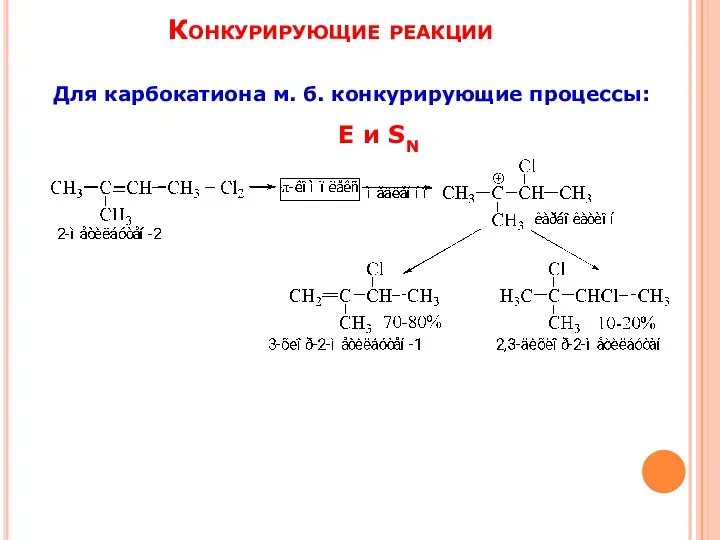
- 12. Конкурирующие реакции Для карбокатиона м. б. конкурирующие процессы: Е и SN
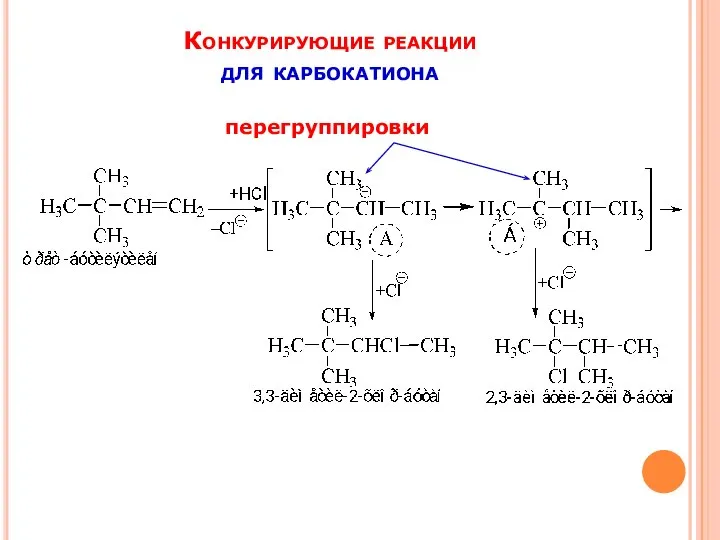
- 13. Конкурирующие реакции для карбокатиона перегруппировки
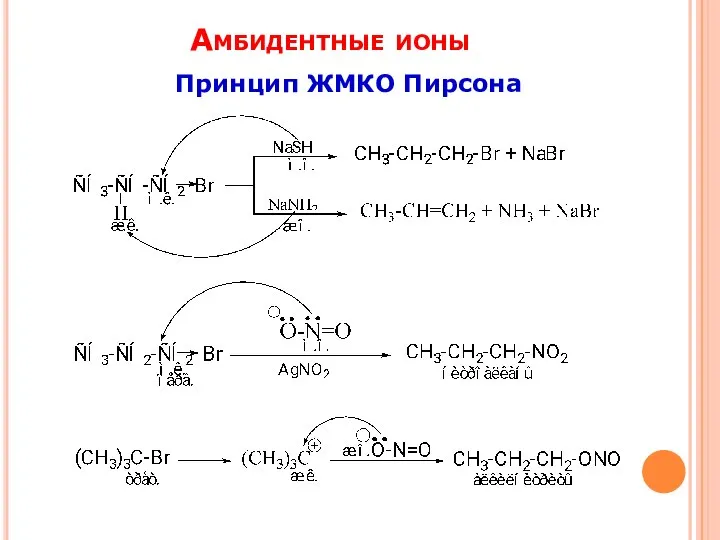
- 14. Амбидентные ионы Принцип ЖМКО Пирсона
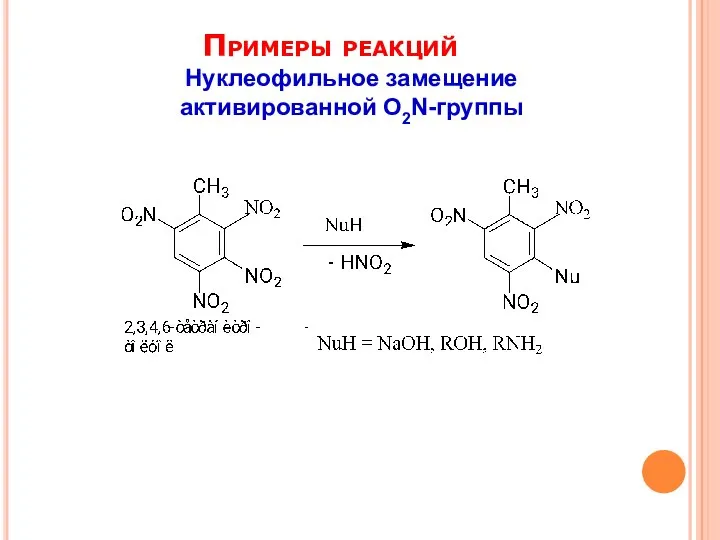
- 15. Примеры реакций Нуклеофильное замещение активированной O2N-группы
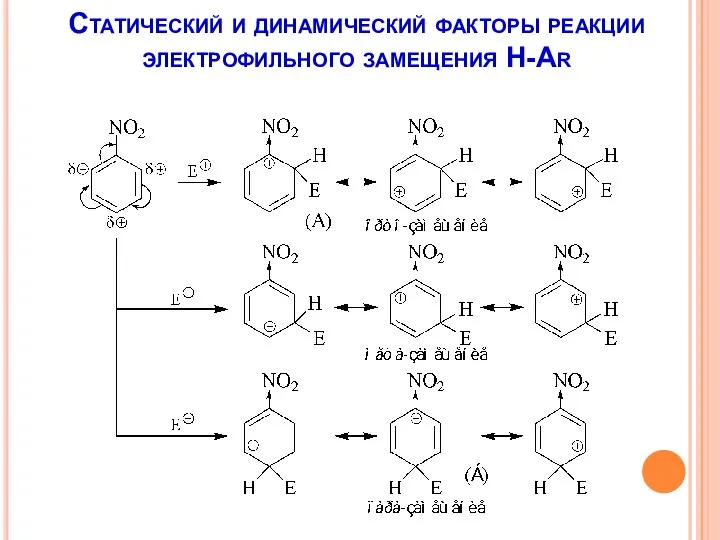
- 16. Статический и динамический факторы реакции электрофильного замещения Н-Ar
- 17. Статический и динамический факторы реакции нуклеофильного замещения Ar-Х Для 2,3,4,6-тетранитротолуола: (доска) ВЫВОД: При планировании незнакомой реакции
- 18. Стереохимия Поляриметры: 1 - монохроматический свет 2, 4 - призма Николя из исландского шпата 3 –
- 19. СТЕРЕОХИМИЯ Хиральность - способность соединений существовать в виде пары несовместимых зеркальных изображений - стереоизомеров. Хиральный центр
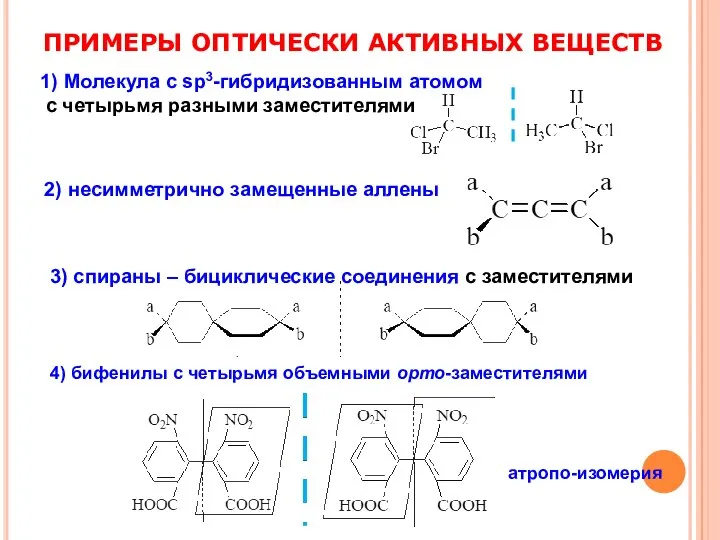
- 20. ПРИМЕРЫ ОПТИЧЕСКИ АКТИВНЫХ ВЕЩЕСТВ 1) Молекула с sp3-гибридизованным атомом с четырьмя разными заместителями 2) несимметрично замещенные
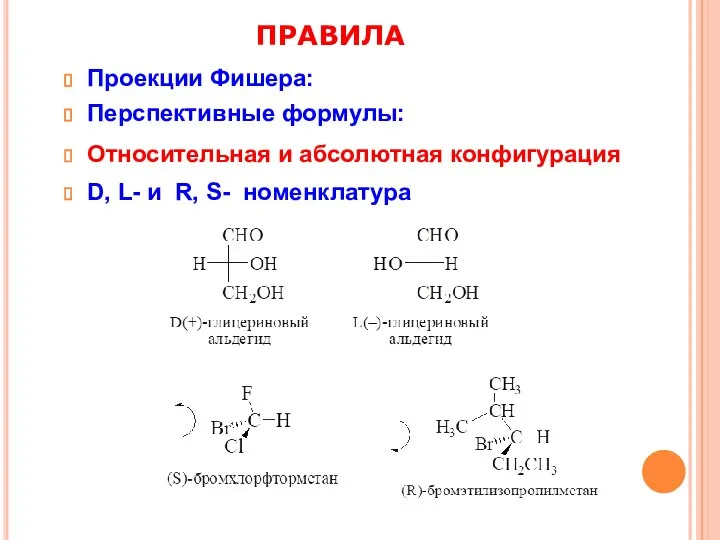
- 21. ПРАВИЛА Проекции Фишера: Перспективные формулы: Относительная и абсолютная конфигурация D, L- и R, S- номенклатура
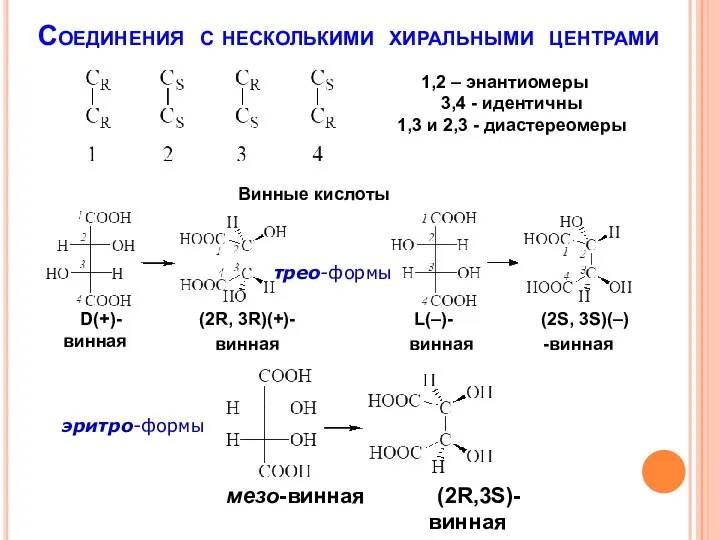
- 22. Соединения с несколькими хиральными центрами 1,2 – энантиомеры 3,4 - идентичны 1,3 и 2,3 - диастереомеры
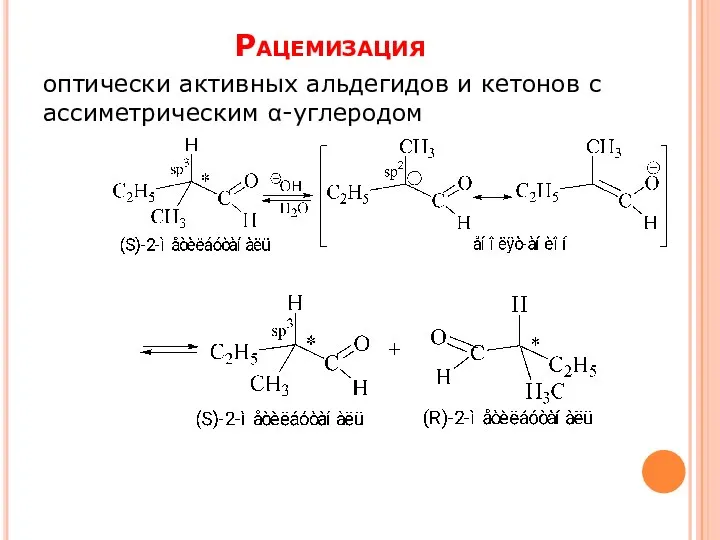
- 23. Рацемизация оптически активных альдегидов и кетонов с ассиметрическим α-углеродом
- 24. Задача 1, 2 Из ацетилена, этилбромида и других необходимых реагентов получите мезо-гександиол-3,4. Приведите формулы Фишера, Ньюмена
- 26. Скачать презентацию






 Химическая связь
Химическая связь Дополнительный_материал_11.15_23.09.2022_e4f87550
Дополнительный_материал_11.15_23.09.2022_e4f87550 Белки. Химия
Белки. Химия Фізика гірських порід і процесів. Хімічні зв'язки в мінералах. Іонний зв'язок
Фізика гірських порід і процесів. Хімічні зв'язки в мінералах. Іонний зв'язок Классы неорганических соединений
Классы неорганических соединений Промышленный метод получения ацетилена
Промышленный метод получения ацетилена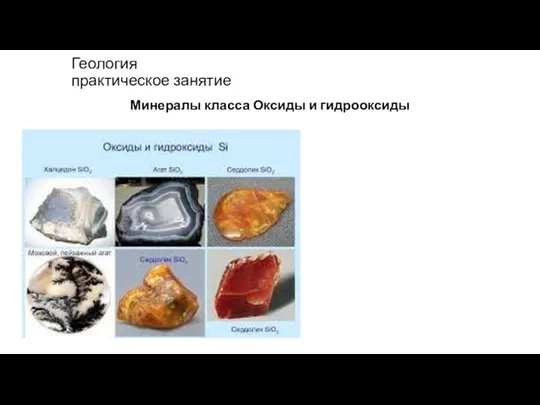 Оксиды и гидрооксиды
Оксиды и гидрооксиды Водород
Водород валентность (1)
валентность (1) Идеальный газ
Идеальный газ Азот, соединения азота
Азот, соединения азота кристаллические решетки (2) (2)
кристаллические решетки (2) (2) Презентация на тему Электролиз
Презентация на тему Электролиз  Алканы: состав, строение, изомерия, номенклатура, получение
Алканы: состав, строение, изомерия, номенклатура, получение Презентация на тему Неогранические соединения. Периодическая таблица
Презентация на тему Неогранические соединения. Периодическая таблица  Коррозия металлов. Экзаменационные вопросы
Коррозия металлов. Экзаменационные вопросы Температурная зависимость скорости химической реакции
Температурная зависимость скорости химической реакции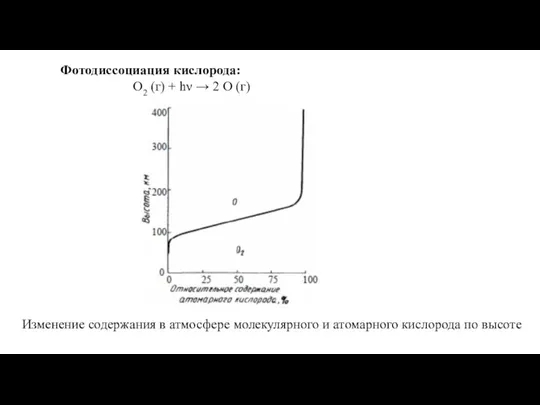 Фотодиссоциация кислорода
Фотодиссоциация кислорода Основы теории сплавов. Типы сплавов (твердые растворы, сплавы-смеси, сплавы- химические соединения. Диаграммы
Основы теории сплавов. Типы сплавов (твердые растворы, сплавы-смеси, сплавы- химические соединения. Диаграммы Особенности решения практикоориентированного задания №26 ГИА-11
Особенности решения практикоориентированного задания №26 ГИА-11 Звездный час. Конкурс химиков
Звездный час. Конкурс химиков Щелочные металлы
Щелочные металлы Плотность вещества
Плотность вещества Молекулярная химия
Молекулярная химия Башня плотности
Башня плотности Химия в нашем доме. Введение в курс. Урок №1
Химия в нашем доме. Введение в курс. Урок №1 Галогены
Галогены Нітрогеновмісні сполуки
Нітрогеновмісні сполуки