Содержание
- 2. цели урока Сформировать представление о практическом значении соляной кислоты; Актуализировать прежние знания о химических и физических
- 3. вопросы Назовите формулу соляной кислоты? Из каких двух элементов состоит соляная кислота? Элементы образующие молекулу хлороводорода
- 4. Задания Запишите электронное строение для атома хлора и водорода. Запишите электронно-графическую формулу для атома хлора и
- 5. С какими из перечисленных веществ будет реагировать бром. Хлор; Медь; Вода; Цинк; Водород;
- 6. Осуществите цепочку превращений и запишите химические реакции. Хлор Хлорид меди(II) Гидроксид меди(II) Оксид меди(II) Медь Хлорид
- 7. Химические свойства соляной кислоты. 1. Изменение окраски индикаторов(лакмуса метилоранжа); 2. Взаимодействие с металлами, стоящими в ряду
- 8. 3. Взаимодействие с основными и амфотерными оксидами. 2HCI + CaO = CaCI2 + H2O 6HCI +
- 9. 5.Взаимодействие с солями: 2HCI + CaCO3 = CaCI2 + H2CО3 Качественная реакция на соляную кислоту и
- 10. Получение хлороводорода. В промышленности H2 + CI2 = 2HCI В лаборатории 2NaCI(тв)+H2SO4 = Na2SO4+2HCI
- 11. Каменная соль (NaCI)
- 12. Вычислите массу осадка, который образуется при взаимодействии хлорида натрия массой 30г с раствором нитрата серебра. задача
- 13. задание с какими веществами будет реагировать соляная кислота ZnO, Fe(OH)3, Cu, Ca,
- 15. Скачать презентацию












 Типы кристаллических решеток
Типы кристаллических решеток Судын оксидтермен реакциясы
Судын оксидтермен реакциясы Ионная химическая связь
Ионная химическая связь Классы неорганических соединений
Классы неорганических соединений Истина - дочь времени, а не авторитета
Истина - дочь времени, а не авторитета Презентация на тему Виды кристаллических решеток
Презентация на тему Виды кристаллических решеток 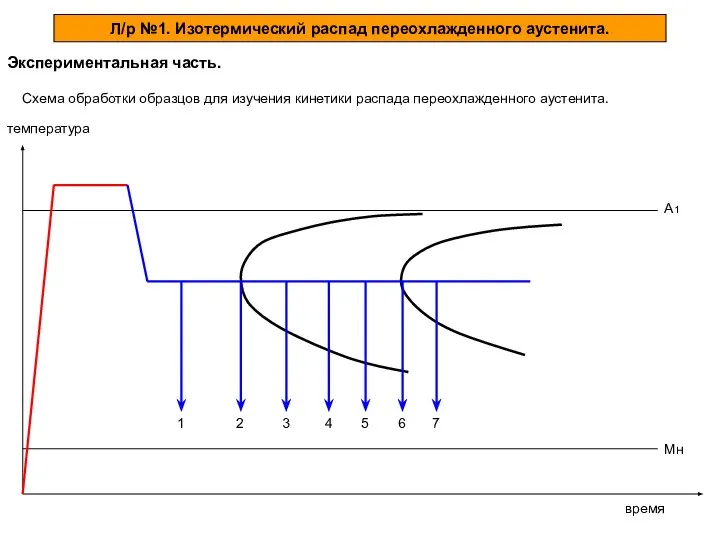 Изотермический распад переохлажденного аустенита. Экспериментальная часть
Изотермический распад переохлажденного аустенита. Экспериментальная часть Содержание варианта ЕГЭ
Содержание варианта ЕГЭ 11_.21
11_.21 Использование комплексно-ориентированных заданий на уроках
Использование комплексно-ориентированных заданий на уроках Окислительно-восстановительные реакции (ОВР)
Окислительно-восстановительные реакции (ОВР) Реакции окисления-восстановления в химическом анализе. (Лекция 7.2)
Реакции окисления-восстановления в химическом анализе. (Лекция 7.2) Алканы
Алканы Химия и автомобиль
Химия и автомобиль Общая характеристика элементов подгруппы углерода. Углерод – его строение и свойства
Общая характеристика элементов подгруппы углерода. Углерод – его строение и свойства Природный каучук
Природный каучук Классификация оксидов
Классификация оксидов Химические реакции
Химические реакции Образование и получение веществ. 6 класс
Образование и получение веществ. 6 класс Металлы
Металлы Закон сохранения массы веществ. Уравнения химических реакций.
Закон сохранения массы веществ. Уравнения химических реакций. Сравнительная характеристика стиральных порошков
Сравнительная характеристика стиральных порошков Валентность. Определение валентности по формулам
Валентность. Определение валентности по формулам Кроссворд. Плотность
Кроссворд. Плотность Алкены
Алкены Коррозия металлов
Коррозия металлов Вещества с атомной кристаллической решеткой
Вещества с атомной кристаллической решеткой Cкорость химических реакций
Cкорость химических реакций