Содержание
- 2. Фарадей Майкл 22. IX.1791 – 25.VIII. 1867 Английский физик и химик. В первой половине 19 в.
- 3. ТЕОРИЯ ЭЛЕКТРОЛИТИЧЕСКОЙ ДИССОЦИАЦИИ (ТЭД) В 1887 году шведский учёный С. Аррениус для объяснения особенностей водных растворов
- 4. Вещества Электролиты – Неэлектролиты – проводят эл.ток в растворах не проводят эл. ток в растворах Тип
- 5. ЭЛЕКТРОЛИТИЧЕСКАЯ ДИССОЦИАЦИЯ 1 ПОЛОЖЕНИЕ Все вещества по их способности проводить электрический ток в растворах делятся на
- 6. Процесс распада электролита на ионы называется электролитической диссоциацией. Химический словарь
- 7. 2 ПОЛОЖЕНИЕ При растворении в воде электролиты диссоциируют (распадаются) на положительные и отрицательные ионы Ионы –
- 8. ИОНЫ - это положительно или отрицательно заряженные частицы, в которые превращаются атомы или группы атомов в
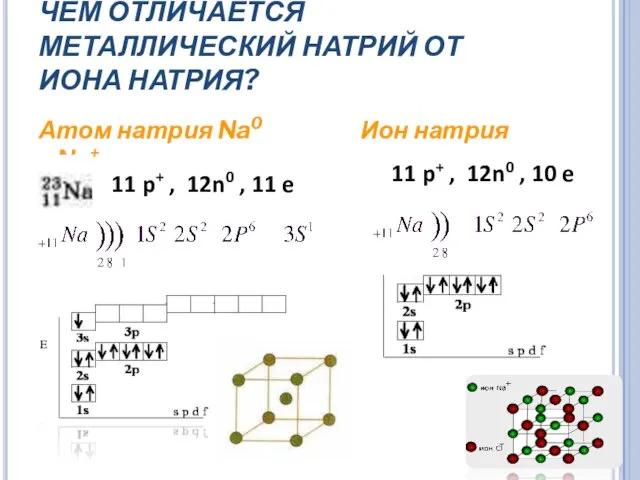
- 9. ЧЕМ ОТЛИЧАЕТСЯ МЕТАЛЛИЧЕСКИЙ НАТРИЙ ОТ ИОНА НАТРИЯ? Атом натрия Na0 Ион натрия Na+ 11 p+ ,
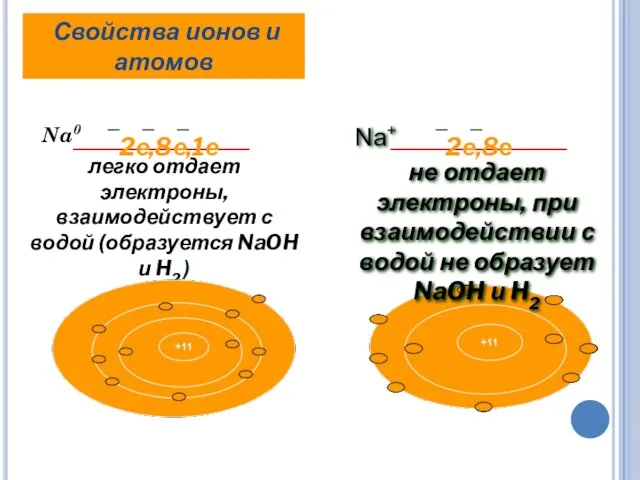
- 10. Na0 легко отдает электроны, взаимодействует с водой (образуется NaOH и H2 ) Свойства ионов и атомов
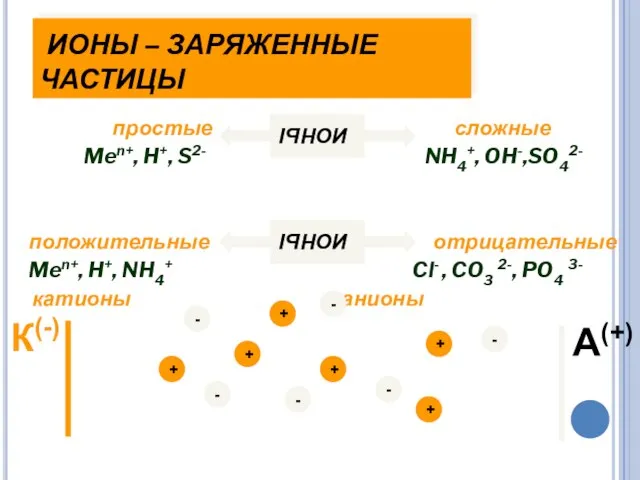
- 11. ИОНЫ – ЗАРЯЖЕННЫЕ ЧАСТИЦЫ простые сложные Men+, H+, S2- NH4+, OH-,SO42- положительные отрицательные Men+, H+, NH4+
- 12. 3 ПОЛОЖЕНИЕ Причиной диссоциации электролита является его взаимодействие с молекулами воды и разрыв химической связи в
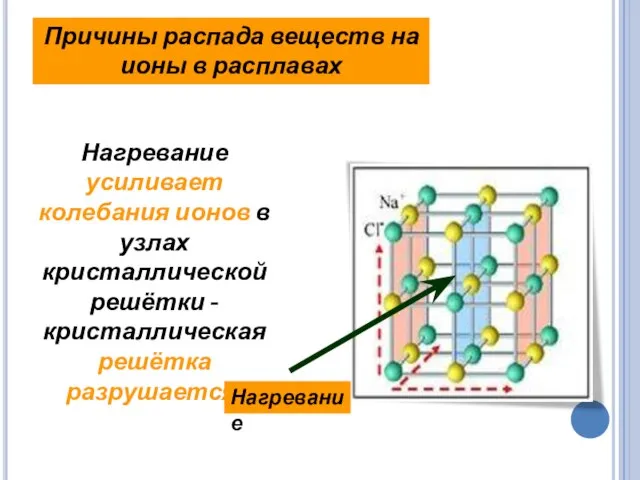
- 13. Нагревание усиливает колебания ионов в узлах кристаллической решётки -кристаллическая решётка разрушается. Причины распада веществ на ионы
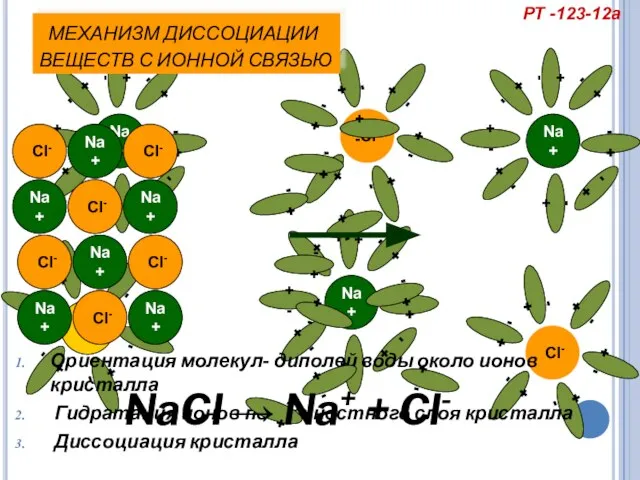
- 14. МЕХАНИЗМ ДИССОЦИАЦИИ ВЕЩЕСТВ С ИОННОЙ СВЯЗЬЮ Ориентация молекул- диполей воды около ионов кристалла Гидратация ионов поверхностного
- 15. СУЩНОСТЬ ПРОЦЕССА ЭЛЕКТРОЛИТИЧЕСКОЙ ДИССОЦИАЦИИ ВЕЩЕСТВ С КОВАЛЕНТНОЙ ПОЛЯРНОЙ СВЯЗЬЮ ориентация молекул воды вокруг полюсов молекулы электролита
- 17. Скачать презентацию









 Металлы побочных подгрупп
Металлы побочных подгрупп Kristālisku vielu uzbūve
Kristālisku vielu uzbūve Кислород – основа жизни?
Кислород – основа жизни? Основи масообміну
Основи масообміну Энергетический обмен
Энергетический обмен Пластик и его применение в быту
Пластик и его применение в быту Ниобий. Химические свойства
Ниобий. Химические свойства 热塑性复合材料的分类及特性
热塑性复合材料的分类及特性 Нанотехнологии в быту
Нанотехнологии в быту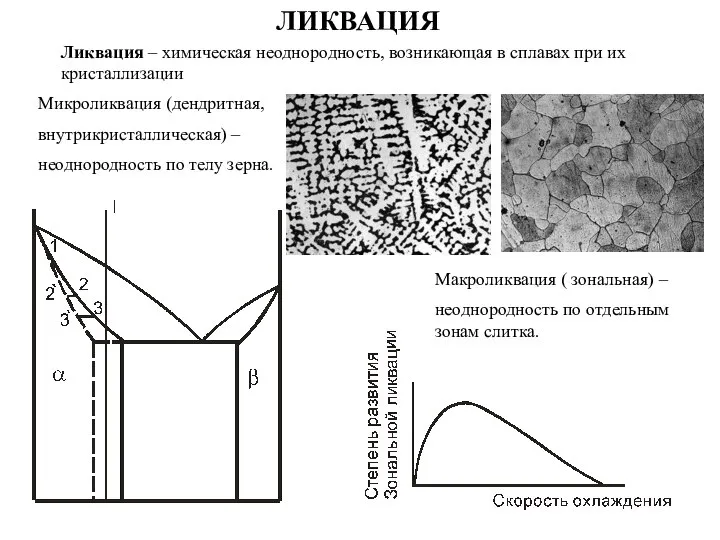 Ликвация. Микроликвация
Ликвация. Микроликвация Вода в природе
Вода в природе Урок изучения и первичного усвоения знаний с элементами исследования на тему: «Окислительно-восстановительные свойства соединен
Урок изучения и первичного усвоения знаний с элементами исследования на тему: «Окислительно-восстановительные свойства соединен Конструирование макромолекул методом ATRP
Конструирование макромолекул методом ATRP Презентация на тему Строение Бензола
Презентация на тему Строение Бензола  Химическая Кинетика
Химическая Кинетика Криптон. Самостоятельная работа
Криптон. Самостоятельная работа Диффузия и осмос
Диффузия и осмос Валентность
Валентность Стехиометрические законы химии
Стехиометрические законы химии Электролитическая диссоциация. 9 класс
Электролитическая диссоциация. 9 класс Золото. Золотые сплавы
Золото. Золотые сплавы Оливины. Структура оливинов
Оливины. Структура оливинов Модульная технология на уроках химии
Модульная технология на уроках химии Обобщение металлов
Обобщение металлов Сравнительный анализ питьевой бутилированной воды
Сравнительный анализ питьевой бутилированной воды Процессы массопередачи в гомогенных средах
Процессы массопередачи в гомогенных средах Преобразование уравнения Нернста. Коэффициент Кда. Причины различия в значениях Кда для различных пород
Преобразование уравнения Нернста. Коэффициент Кда. Причины различия в значениях Кда для различных пород Составление уравнений окислительно-восстановительных реакций
Составление уравнений окислительно-восстановительных реакций