Содержание
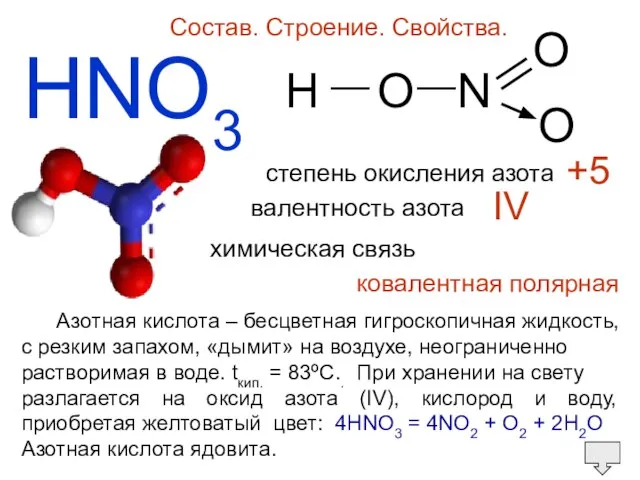
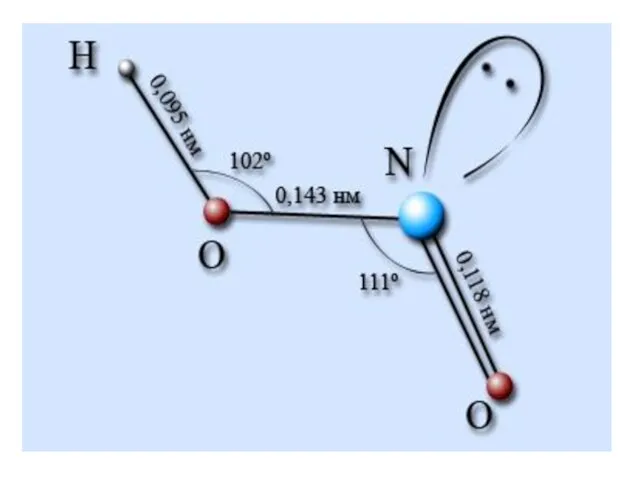
- 2. HNO3 Состав. Строение. Свойства. H O N O O — — степень окисления азота валентность азота
- 4. При разложении азотной кислоты выделяется кислород, поэтому скипидар вспыхивает.
- 5. Азотная кислота (HNO3) Классификация наличию кислорода: основности: растворимости в воде: летучести: степени электролитической диссоциации: кислородсодержащая одноосновная
- 6. Получение азотной кислоты в промышленности NH3 NO NO2 HNO3 4NH3+ 5O2 = 4NO + 6H2O 2NO+O2
- 7. В лаборатории азотную кислоту получают действием концентрированной серной кислоты на нитраты при слабом нагревании. Составьте уравнение
- 8. Химические свойства азотной кислоты 1. Типичные свойства кислот 2. Взаимодействие азотной кислоты с металлами 3. Взаимодействие
- 9. Химические свойства азотной кислоты Азотная кислота проявляет все типичные свойства кислот. Перечислите свойства характерные для кислот.
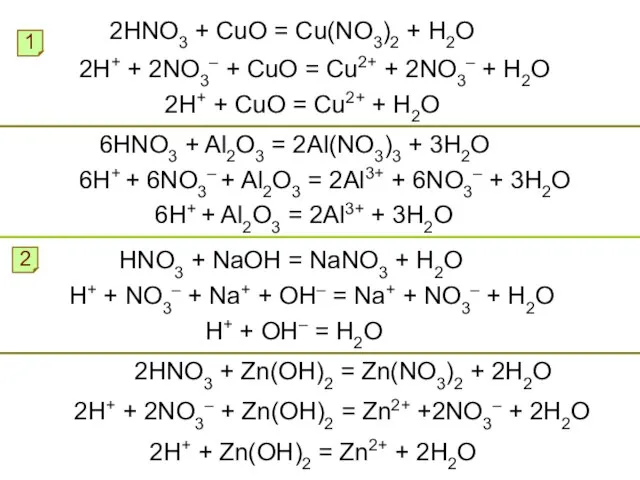
- 10. 2HNO3 + CuO = Cu(NO3)2 + H2O 1 2H+ + 2NO3– + CuO = Cu2+ +
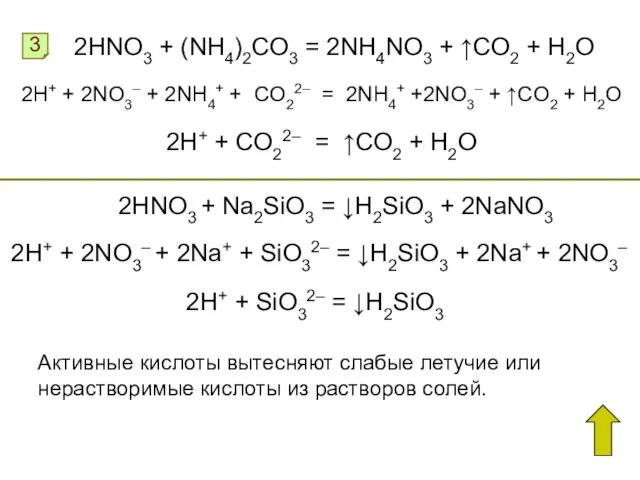
- 11. 3 2HNO3 + (NH4)2CO3 = 2NH4NO3 + ↑CO2 + H2O 2H+ + 2NO3– + 2NH4+ +
- 12. Взаимодействие азотной кислоты с металлами Как реагируют металлы с растворами кислот? Металлы, стоящие в ряду активности
- 13. Окислительные свойства азотной кислоты
- 14. Составьте уравнение реакции взаимодействия концентрированной азотной кислоты с ртутью. Рассмотрите реакцию с т. зр. ОВР. 4HN+5O3
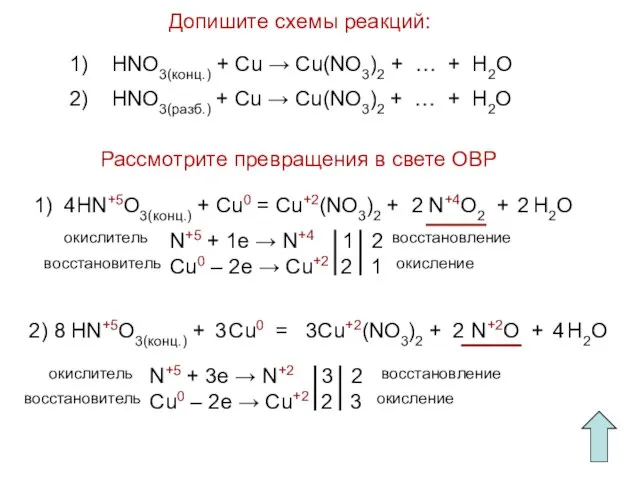
- 15. Допишите схемы реакций: Рассмотрите превращения в свете ОВР 1) HNO3(конц.) + Cu → Cu(NO3)2 + …
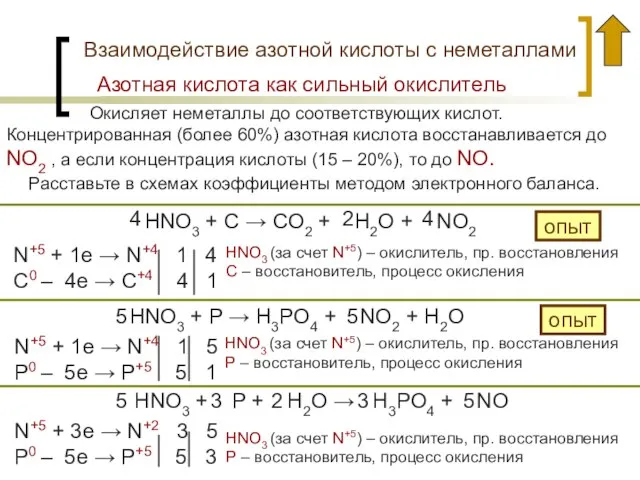
- 17. Взаимодействие азотной кислоты с неметаллами Окисляет неметаллы до соответствующих кислот. Концентрированная (более 60%) азотная кислота восстанавливается
- 18. Взаимодействие азотной кислоты с углем
- 19. Взаимодействие азотной кислоты с белым фосфором
- 20. Применение азотной кислоты 1 5 4 6 2 3 Производство азотных и комплексных удобрений. Производство взрывчатых
- 21. Соли азотной кислоты Как называются соли азотной кислоты? нитраты Нитраты K, Na, NH4+ называют селитрами Составьте
- 22. Нитрат калия (калиевая селитра) Бесцветные кристаллы Значительно менее гигроскопична по сравнению с натриевой, поэтому широко применя-ется
- 23. Кристаллическое вещество белого цвета. Температура плавления 169,6 °C, при нагреве выше этой температуры начинается постепенное разложение
- 24. При нагревании нитраты разлагаются тем полнее, чем правее в электрохимическом ряду напряжений стоит металл, образующий соль.
- 26. Скачать презентацию

















 Методы восстановления. Формирование СН-связей декарбоксилированием и декарбонилированием
Методы восстановления. Формирование СН-связей декарбоксилированием и декарбонилированием Основные понятия химической термодинамики
Основные понятия химической термодинамики Биологическая роль III(A) группы
Биологическая роль III(A) группы Органические вещества
Органические вещества Презентация на тему Кристаллические решетки
Презентация на тему Кристаллические решетки  Адсорбция твёрдыми адсорбентами
Адсорбция твёрдыми адсорбентами Фторсодержащие полимеры
Фторсодержащие полимеры Презентация на тему Волокна
Презентация на тему Волокна  Презентация на тему Путешествие по континенту Химия
Презентация на тему Путешествие по континенту Химия  Соли в природе и их значение
Соли в природе и их значение Задача №3: Трансмутация. Команда: Карбораны
Задача №3: Трансмутация. Команда: Карбораны Курс химии для основных академических направлений подготовки специалистов НИЯУ МИФИ
Курс химии для основных академических направлений подготовки специалистов НИЯУ МИФИ Металлическая химическая связь
Металлическая химическая связь Карбид кремния
Карбид кремния Кетоновые тела
Кетоновые тела Химия в еде
Химия в еде Степени окисления
Степени окисления Алкины
Алкины Презентация на тему Коррозия
Презентация на тему Коррозия  Ренгеноструктурный и рентгеноспектральный анализы
Ренгеноструктурный и рентгеноспектральный анализы Ароматические углеводороды
Ароматические углеводороды Алканы
Алканы Презентация на тему Органическая химия. История развития
Презентация на тему Органическая химия. История развития  Моноенаминирование 4-пиронов и 4-метилен-4н-пиранов
Моноенаминирование 4-пиронов и 4-метилен-4н-пиранов Особенные свойства муравьиной кислоты
Особенные свойства муравьиной кислоты Физическая химия, термодинамика
Физическая химия, термодинамика Теоретические основы органической химии. Лекция 25
Теоретические основы органической химии. Лекция 25 valentnost
valentnost