Содержание
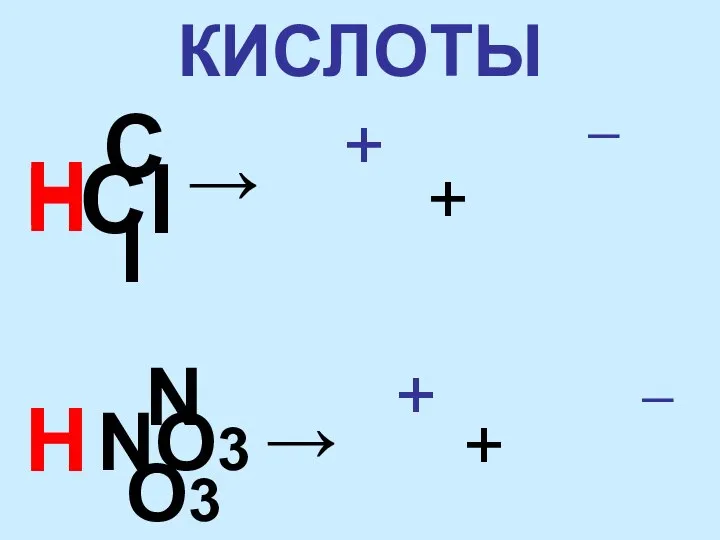
- 2. КИСЛОТЫ H + + → Cl _ H Cl H NO3 → H NO3 _ +
- 3. 1. КИСЛОТЫ – ЭТО СЛОЖНЫЕ ВЕЩЕСТВА, СОСТОЯЩИЕ ИЗ ИОНОВ ВОДОРОДА И КИСЛОТНОГО ОСТАТКА. 2. КИСЛОТЫ –
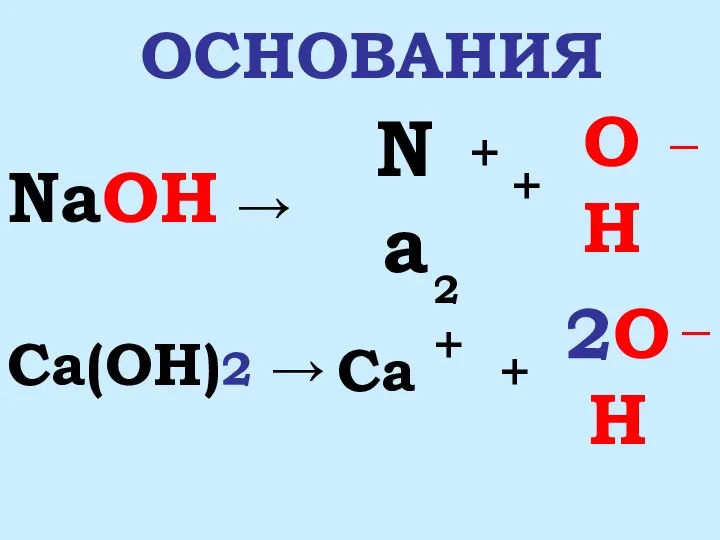
- 4. ОСНОВАНИЯ NaOH → Ca(OH)2 → Na + OH + _ Ca 2OH _ + 2+
- 5. 1. ОСНОВАНИЯ- ЭТО СЛОЖНЫЕ ВЕЩЕСТВА, СОСТОЯЩИЕ ИЗ ИОНОВ МЕТАЛЛА И ГИДРОКСИД-ИОНОВ OH 2. ОСНОВАНИЯ- ЭТО ЭЛЕКТРОЛИТЫ,
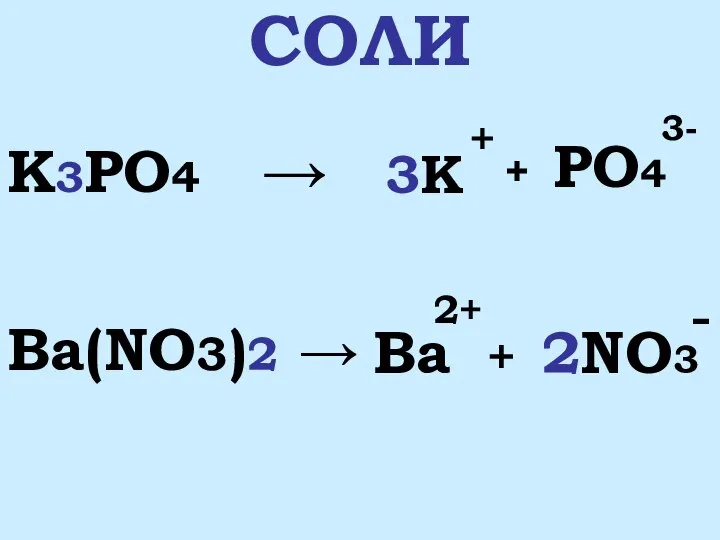
- 6. СОЛИ K3PO4 → Ba(NO3)2 → 3K + PO4 3- Ba 2+ + + 2NO3 -
- 7. 1. Соли – это сложные вещества, состоящие из ионов металла и ионов кислотного остатка 2. Соли
- 8. Реакции ионного обмена Определить растворимость веществ, подчеркнуть их; Под чертой написать уравнение их диссоциации (учитывая коэффициенты!!!).
- 9. Реакции обмена Реакции, в которых электролиты меняются ионами. Реакции между ионами ионного Условия протекания реакций ионного
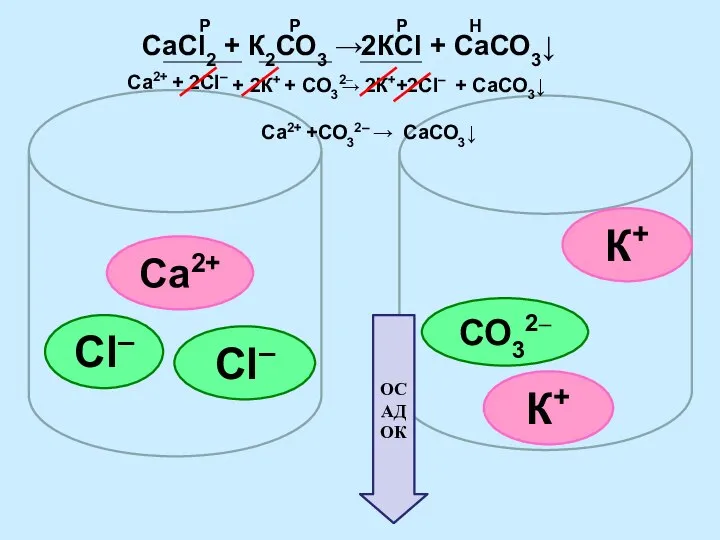
- 10. СаСl2 + К2СО3 → КСl + СаСО3↓ Са2+ Сl– Сl– К+ К+ СО32– ОСАДОК Р Р
- 12. Скачать презентацию





 Растворы. Виды выражения концентрации
Растворы. Виды выражения концентрации Химическая связь
Химическая связь Амины и анилин
Амины и анилин Мышьяк. История. Нахождение в природе
Мышьяк. История. Нахождение в природе Химическая промышленность России входит в авангардную тройку
Химическая промышленность России входит в авангардную тройку Коллоидные системы
Коллоидные системы Химическая связь
Химическая связь Сплавы со специальными свойствами
Сплавы со специальными свойствами Внутренняя среда организма. Система крови. Физико-химические свойства крови
Внутренняя среда организма. Система крови. Физико-химические свойства крови 3bc28ca0711047a6880d20a6763f17db
3bc28ca0711047a6880d20a6763f17db Скорость химической реакции. 9 класс
Скорость химической реакции. 9 класс Химия углеводов
Химия углеводов Хлор
Хлор Уравнение состояния идеального газа
Уравнение состояния идеального газа Моделирование фазовых систем. Тройные взаимные системы
Моделирование фазовых систем. Тройные взаимные системы Адиабатическое приближение, потенциальные поверхности молекулярных систем, неадиабатические переходы
Адиабатическое приближение, потенциальные поверхности молекулярных систем, неадиабатические переходы Расчеты по химическим уравнениям реакций
Расчеты по химическим уравнениям реакций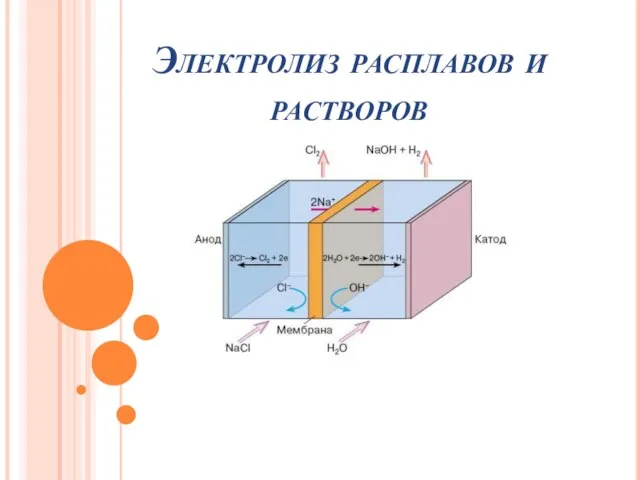 Электролиз расплавов растворов
Электролиз расплавов растворов Первые попытки классификации химических элементов
Первые попытки классификации химических элементов Презентация на тему Важнейшие соединения серы
Презентация на тему Важнейшие соединения серы  Неметаллы. 8 класс
Неметаллы. 8 класс Определение воды по Фишеру. Кислотное число, число омыления. Определение аминного азота
Определение воды по Фишеру. Кислотное число, число омыления. Определение аминного азота Строение углеводородов
Строение углеводородов Характеристика химического элемента-неметалла на основании его положения в ПСХЭ Д.И.Менделеева. 9 класс
Характеристика химического элемента-неметалла на основании его положения в ПСХЭ Д.И.Менделеева. 9 класс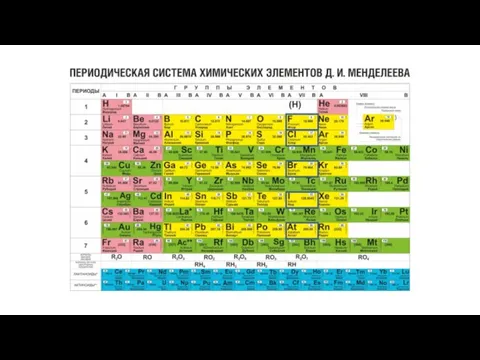 Периодическая система химических элементов Д. И. Менделеева
Периодическая система химических элементов Д. И. Менделеева Кислоты и их свойства
Кислоты и их свойства Вещество. Кристаллические решетки
Вещество. Кристаллические решетки Презентация на тему В мире индикаторов - исследовательская работа
Презентация на тему В мире индикаторов - исследовательская работа