Содержание
- 2. 1. Записать молекулярное уравнение реакции Даны растворы хлорида железа(III) и гидроксида калия. Написать молекулярное и ионные
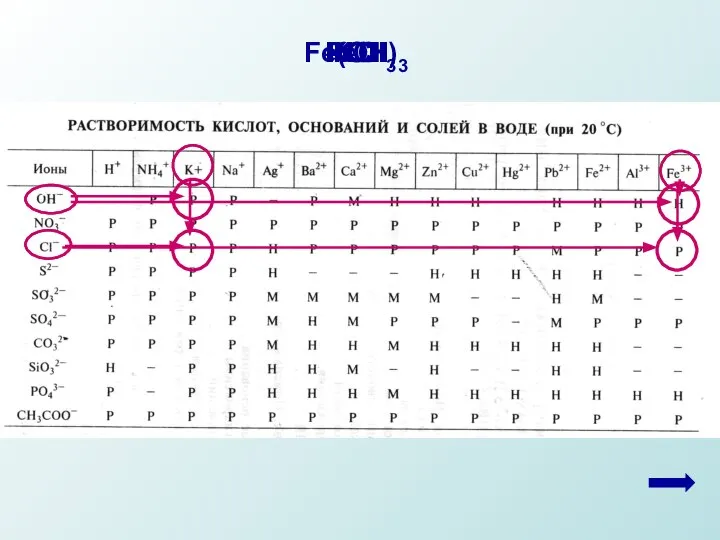
- 3. 2. Подчеркнуть формулы электролитов (формулы кислот, оснований, солей Используя таблицу растворимости определить растворимость электролитов и записать
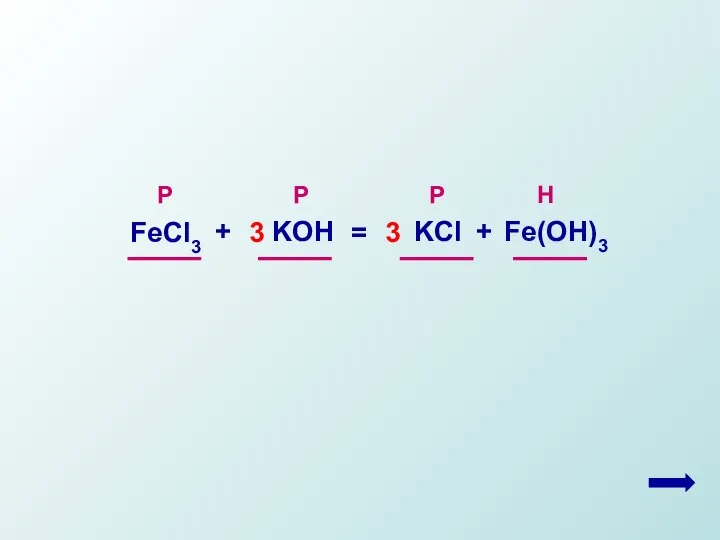
- 4. FeCl3 KOH Fe(OH)3 KCl
- 5. Р Р Р Н
- 6. 3. Написать полное ионное уравнение реакции. ЗАПОМНИТЬ!!! В ионных уравнениях формулы электролитов 1) растворимых в воде
- 8. Скачать презентацию



 Полимеры с включением атомов бора и карборановой группировки - полиборорганосилоксаны и поликарборанорганосилосксаны
Полимеры с включением атомов бора и карборановой группировки - полиборорганосилоксаны и поликарборанорганосилосксаны Химия и сельское хозяйство
Химия и сельское хозяйство Оксидтер мен негіздердің реакциялары
Оксидтер мен негіздердің реакциялары Алгоритмы при изучении химии
Алгоритмы при изучении химии Презентация на тему Витамины. Урок химии 10 класс
Презентация на тему Витамины. Урок химии 10 класс  Алкины и их свойства
Алкины и их свойства Химия и автомобиль
Химия и автомобиль Углеводороды: изомерия
Углеводороды: изомерия Амилаза. Строение амилазы
Амилаза. Строение амилазы Минеральные кислоты. Взаимодействие с простыми веществами
Минеральные кислоты. Взаимодействие с простыми веществами Энергетические уровни
Энергетические уровни Углеводороды (УВ)
Углеводороды (УВ) Олеиновая кислота
Олеиновая кислота Химия һәм сәламәт яшәү рәвеше
Химия һәм сәламәт яшәү рәвеше Презентация на тему Кальций
Презентация на тему Кальций  Арены. Бензол
Арены. Бензол Задания для подготовки к ЕГЭ по химии
Задания для подготовки к ЕГЭ по химии Окислительные свойства концентрированной серной кислоты
Окислительные свойства концентрированной серной кислоты Любовь и химия
Любовь и химия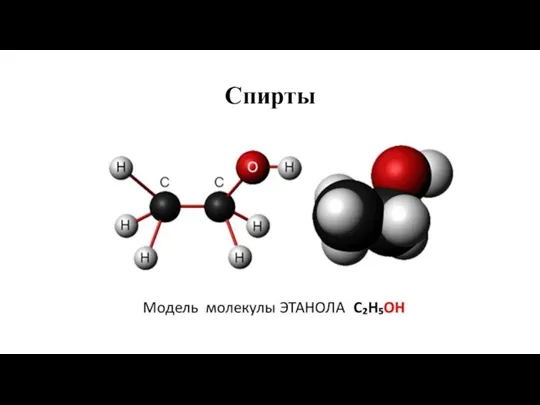 Спирты
Спирты Алкены. Этилен C2H4
Алкены. Этилен C2H4 Сравнительный анализ Фармакопейных статей для субстанций, представленных в мировых Фармакопеях
Сравнительный анализ Фармакопейных статей для субстанций, представленных в мировых Фармакопеях Окисление этанола оксидом меди
Окисление этанола оксидом меди Смачивание и не смачивание жидкости. Капилляры
Смачивание и не смачивание жидкости. Капилляры Карбоновые кислоты
Карбоновые кислоты Предмет органической химии. Урок №1
Предмет органической химии. Урок №1 Характеристика кислорода и серы
Характеристика кислорода и серы Свойства ртути
Свойства ртути