Слайд 2ПОНЯТТЯ ПРО СТУПІНЬ ОКИСНЕННЯ

Слайд 3СТУПІНЬ ОКИСНЕННЯ І ВАЛЕНТНІСТЬ
СТУПІНЬ ОКИСНЕННЯ — ПОНЯТТЯ, ЩО ХАРАКТЕРИЗУЄ СТАН ЕЛЕМЕНТА

В ХІМІЧНІЙ СПОЛУЦІ ТА ЙОГО ПОВЕДІНКУ В ОКИСНО-ВІДНОВНИХ ПРОЦЕСАХ.
ЦЕ УМОВНИЙ ЗАРЯД, ВЕЛИЧИНА ЯКОГО РОЗРАХОВУЄТЬСЯ ВИХОДЯЧИ З ПРИПУЩЕННЯ, ЩО ВСІ ЕЛЕКТРОНИ, ЯКІ УТВОРЮЮТЬ ХІМІЧНИЙ ЗВ’ЯЗОК, ПОВНІСТЮ ПЕРЕХОДЯТЬ ДО БІЛЬШ ЕЛЕКТРОНЕГАТИВНОГО ЕЛЕМЕНТА.
ВАЛЕНТНІСТЬ — ХАРАКТЕРИСТИКА ЗДАТНОСТІ АТОМА УТВОРЮВАТИ ХІМІЧНІ ЗВ’ЯЗКИ.
ВИЗНАЧАЄТЬСЯ ЧИСЛОМ ЗВ’ЯЗКІВ, ЯКІ УТВОРЮЮТЬ ДАНИЙ АТОМ З ІНШИМИ АТОМАМИ В МОЛЕКУЛІ.
Слайд 5СТУПІНЬ ОКИСНЕННЯ І ВАЛЕНТНІСТЬ
(НА ПРИКЛАДІ N2)
ЕЛЕКТРОННА ФОРМУЛА АТОМА НІТРОГЕНУ:
НА ЗОВНІШНЬОМУ ЕНЕРГЕТИЧНОМУ РІВНІ

5 ЕЛЕКТРОНІВ,
ТРИ ІЗ ЯКИХ НЕСПАРЕНІ.
У МОЛЕКУЛІ АЗОТУ N2 НІТРОГЕН УТВОРЮЄ ТРИ КОВАЛЕНТНІ ЗВ’ЯЗКИ
ЙОГО ВАЛЕНТНІСТЬ ДОРІВНЮЄ ТРЬОМ.
ЗМІЩЕННЯ СПІЛЬНИХ ЕЛЕКТРОННИХ ПАР НЕ ВІДБУВАЄТЬСЯ, ВОНИ РІВНОВІДДАЛЕНІ ВІД ЯДЕР ОБОХ АТОМІВ
ТОМУ СТУПІНЬ ОКИСНЕННЯ НІТРОГЕНУ НУЛЬОВИЙ, А ТОДІ ЯК ОБИДВА АТОМИ – ТРИВАЛЕНТНІ.
Слайд 6ЗНАЧЕННЯ ВАЛЕНТНОСТІ Й СТУПЕНІВ ОКИСНЕННЯ ХІМІЧНИХ ЕЛЕМЕНТІВ У ДЕЯКИХ РЕЧОВИНАХ

Слайд 7ПРАВИЛА ВИЗНАЧЕННЯ СТУПЕНЯ ОКИСНЕННЯ

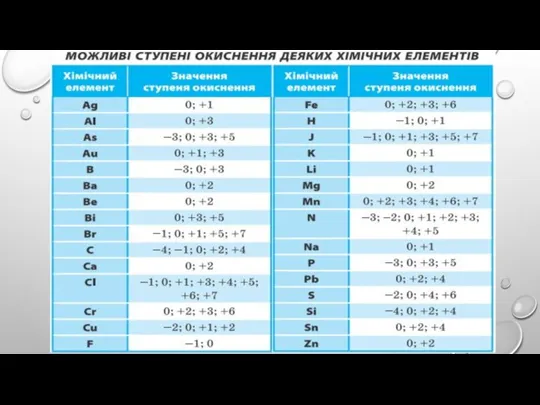
Слайд 9МОЖЛИВІ СТУПЕНІ ОКИСНЕННЯ ЕЛЕМЕНТІВ

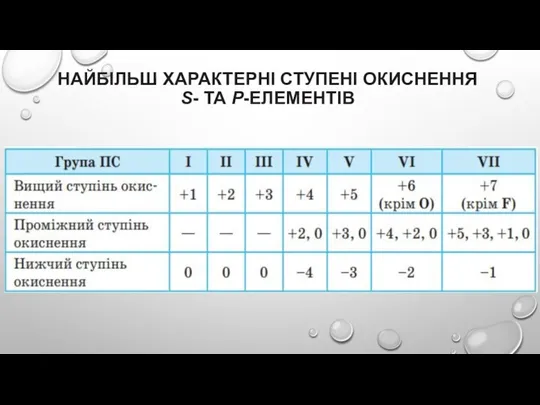
Слайд 10НАЙБІЛЬШ ХАРАКТЕРНІ СТУПЕНІ ОКИСНЕННЯ
S- ТА P-ЕЛЕМЕНТІВ
Слайд 12ДЕЯКІ ХІМІЧНІ ЕЛЕМЕНТИ НЕ ПІДПАДАЮТЬ ПІД ЦІ ПРАВИЛА.
СЕРЕД НИХ ГІДРОГЕН, ОКСИГЕН,
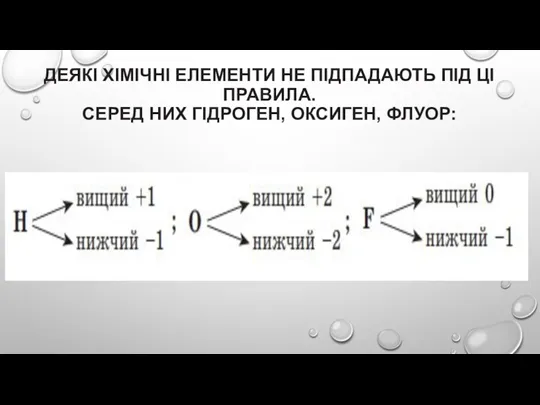
ФЛУОР:
Слайд 13ВИЗНАЧЕННЯ СТУПЕНІВ ОКИСНЕННЯ В БІНАРНИХ СПОЛУКАХ
ДЛЯ ВИЗНАЧЕННЯ СТУПЕНІВ ОКИСНЕННЯ У СПОЛУКАХ

НЕДОСТАТНЬО ЗНАТИ МОЖЛИВІ СТУПЕНІ ОКИСНЕННЯ ЕЛЕМЕНТІВ.
ДЛЯ ЦЬОГО СЛІД КОРИСТУВАТИСЯ ПЕВНИМИ ПРАВИЛАМИ. НАСАМПЕРЕД, ПРИНЦИПОМ ЕЛЕКТРОНЕЙТРАЛЬНОСТІ:
ОСКІЛЬКИ БУДЬ-ЯКА РЕЧОВИНА Є ЕЛЕКТРОНЕЙТРАЛЬНОЮ, ТО СУМА СТУПЕНІВ
ОКИСНЕННЯ АТОМІВ УСІХ ЕЛЕМЕНТІВ, З ЯКИХ СКЛАДАЄТЬСЯ РЕЧОВИНА, МАЄ ДОРІВНЮВАТИ НУЛЮ.
НАПРИКЛАД, ВИЗНАЧИМО СТУПЕНІ ОКИСНЕННЯ ЕЛЕМЕНТІВ У СУЛЬФУР(IV) ОКСИДІ SO2. В ОКСИДАХ СТУПІНЬ ОКИСНЕННЯ ОКСИГЕНУ ЗАВЖДИ ДОРІВНЮЄ –2. ОТЖЕ, ДЛЯ ТОГО ЩОБ НЕЙТРАЛІЗУВАТИ ЗАРЯД НА ДВОХ АТОМАХ ОКСИГЕНУ, В СУЛЬФУРУ СТУПІНЬ ОКИСНЕННЯ МАЄ БУТИ +4:
Слайд 14АЛГОРИТМ ВИЗНАЧЕННЯ СТУПЕНЯ ОКИСНЕННЯ ЕЛЕМЕНТІВ У БІНАРНИХ СПОЛУКАХ

Слайд 15ВИЗНАЧЕННЯ СТУПЕНІВ ОКИСНЕННЯ В КИСЛОТАХ, ГІДРОКСИДАХ ТА СОЛЯХ
ДЛЯ СПОЛУК, УТВОРЕНИХ БІЛЬШЕ

НІЖ ДВОМА ХІМІЧНИМИ ЕЛЕМЕНТАМИ, ПРИНЦИП ЕЛЕКТРОНЕЙТРАЛЬНОСТІ ТАКОЖ Є ОСНОВНИМ.
ПІДХІД ДЛЯ ВИЗНАЧЕННЯ СТУПЕНІВ ОКИСНЕННЯ ТАКИЙ САМИЙ, ЯК І ДЛЯ БІНАРНИХ СПОЛУК.
ТАКОЖ СЛІД ПАМ’ЯТАТИ, ЩО В ПЕРЕВАЖНІЙ БІЛЬШОСТІ СПОЛУК СТУПІНЬ ОКИСНЕННЯ ОКСИГЕНУ ДОРІВНЮЄ –2, А ГІДРОГЕНУ — +1.
Слайд 16АЛГОРИТМ ВИЗНАЧЕННЯ СТУПЕНІВ ОКИСНЕННЯ ЕЛЕМЕНТІВ У КИСЛОТАХ ТА ГІДРОКСИДАХ

Слайд 17ПРИКЛАД:
РОЗГЛЯНЕМО, ЯК ВИЗНАЧИТИ СТУПЕНІ ОКИСНЕННЯ ТРЬОХ ЕЛЕМЕНТІВ, НА ПРИКЛАДІ КАЛІЙ СУЛЬФІТУ K2SO3.

СТУПІНЬ ОКИСНЕННЯ КАЛІЮ У СПОЛУКАХ МОЖЕ БУТИ ТІЛЬКИ +1, А ОКСИГЕНУ — –2:
ОСКІЛЬКИ СУМА ЗАРЯДІВ МАЄ ДОРІВНЮВАТИ НУЛЮ, ТО ОБЧИСЛИМО СТУПІНЬ ОКИСНЕННЯ СУЛЬФУРУ, РОЗВ’ЯЗАВШИ РІВНЯННЯ:
2 · (+1) + 1 · (Х) + 3 · (–2) = 0, ЗВІДКИ Х = +4
Слайд 18СКЛАДАННЯ ФОРМУЛ СПОЛУК ЗА СТУПЕНЕМ ОКИСНЕННЯ ЕЛЕМЕНТІВ
ВИКОРИСТОВУЮЧИ СТУПЕНІ ОКИСНЕННЯ, СКЛАДАТИ ФОРМУЛИ

БІНАРНИХ СПОЛУК ПРОСТІШЕ, НІЖ ЗА ВАЛЕНТНІСТЮ.
СКЛАДАЮЧИ ФОРМУЛИ, СЛІД КЕРУВАТИСЯ ПРАВИЛОМ ЕЛЕКТРОНЕЙТРАЛЬНОСТІ:
ОСКІЛЬКИ БУДЬ-ЯКА РЕЧОВИНА Є ЕЛЕКТРОНЕЙТРАЛЬНОЮ, ТО СУМА СТУПЕНІВ ОКИСНЕННЯ АТОМІВ УСІХ ЕЛЕМЕНТІВ, З ЯКИХ СКЛАДАЄТЬСЯ РЕЧОВИНА, МАЄ ДОРІВНЮВАТИ НУЛЮ.
Слайд 19АЛГОРИТМ СКЛАДАННЯ ФОРМУЛ СПОЛУК ЗА ВІДОМИМИ СТУПЕНЯМИ ОКИСНЕННЯ ЕЛЕМЕНТІВ



















 Классификация программного обеспечения
Классификация программного обеспечения Сайти Інтернету
Сайти Інтернету Проект Rolling Sky. Интерфейс
Проект Rolling Sky. Интерфейс Моделирование окружающего мира
Моделирование окружающего мира Курсы графического дизайна. (Занятие 10)
Курсы графического дизайна. (Занятие 10) Компьютерные сети
Компьютерные сети Занимательная информатика
Занимательная информатика Оценка эффективности существующих программных и программно-аппаратных средств защиты информации
Оценка эффективности существующих программных и программно-аппаратных средств защиты информации Компьютерная графика
Компьютерная графика Изучаем PowerPoint создание слайдов; демонстрация слайдов
Изучаем PowerPoint создание слайдов; демонстрация слайдов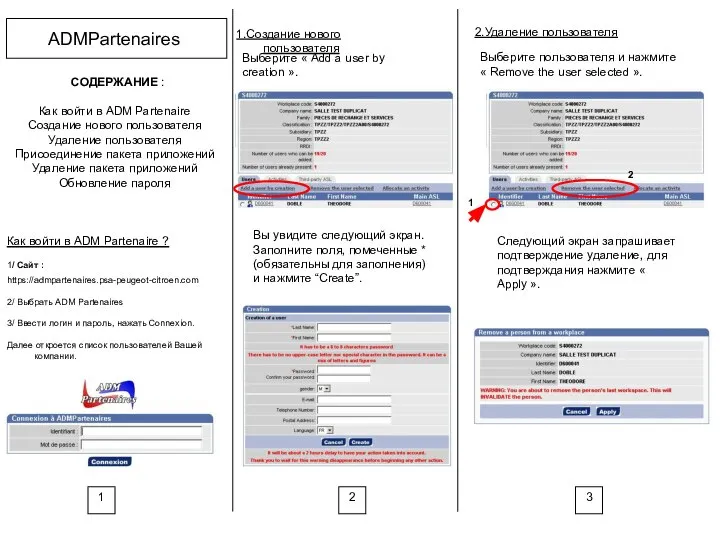 ADM Partenaires. Создание нового пользователя
ADM Partenaires. Создание нового пользователя Интерактивная система помощи иностранным студентам
Интерактивная система помощи иностранным студентам Шифратор и дешифратор
Шифратор и дешифратор Web-страницы. Язык HTML. Списки. Гиперссылки
Web-страницы. Язык HTML. Списки. Гиперссылки Программирование в среде Scratch
Программирование в среде Scratch Лекция2.1
Лекция2.1 Создание веб-сайта салона красоты
Создание веб-сайта салона красоты Дайджест самых важных новостей
Дайджест самых важных новостей Две ритм-игры с душой - Cytus и Deemo
Две ритм-игры с душой - Cytus и Deemo Мобильное приложение дирекции по снабжению ЕВРАЗ
Мобильное приложение дирекции по снабжению ЕВРАЗ Cвязь ФПС, ПФ, ДУ
Cвязь ФПС, ПФ, ДУ Информационные технологии в юридической деятельности
Информационные технологии в юридической деятельности Зарубежный опыт создания информационного общества и реализации электронного правительства (аналитический обзор)
Зарубежный опыт создания информационного общества и реализации электронного правительства (аналитический обзор) Поиск информации
Поиск информации Магия чисел
Магия чисел 10u-2a_Кодирование-I
10u-2a_Кодирование-I Программа Photomath
Программа Photomath Технология производства программных продуктов и услуг. Детальное проектирование программ
Технология производства программных продуктов и услуг. Детальное проектирование программ