Слайд 2Определение относительной плотности мочи урометром
Принцип метода:
Относительная плотность мочи составляет в норме 1,015-1,025

г/см3. Определение относительной плотности мочи производят с помощью специальных ареометров небольшого размера, называемых урометрами. Урометры бывают двух типов: первый - для мочи с низкой и нормальной относительной плотностью (с делениями от 1,000 до 1,030 г/см3), второй - для мочи с высокой относительной плотностью (с делениями от 1,030 до 1,060 г/см3).
Слайд 3ХОД РАБОТЫ
В небольшой цилиндр с таким диаметром, чтобы урометр свободно плавал в

нем, наливают по стенке исследуемую мочу и осторожно погружают в нее урометр. Производят отсчет, беря ту линию на шкале урометра, которая соответствует нижнему мениску жидкости. Все определения производят при температуре 200С, поскольку шкала урометра проградуирована в соответствии с этой температурой. Если моча имеет другую температуру, то на каждые 30С свыше этой температуры нужно прибавить, а на каждые 30С ниже – убавить по 0,001 от показания шкалы урометра.
Слайд 5Определение белка в моче
Все реакции на содержание белка в моче основаны на

его денатурации и осаждении. Перед проведением анализа необходимо профильтровать и подкислить щелочную мочу. Для определения белка в моче применяют пробы кипячения с сульфасалициловой кислотой, Геллера.
Количественное определение белка проводят по методу Робертса — Стольникова (Брандберга). Этот метод получил широкое распространение благодаря достаточной точности и простоте постановки. В его основе лежит проба Геллера с использованием 50%-ной азотной кислоты. При постановке реакции обращают внимание на плотность, ширину и время появления белого кольца на границе разделения сред. Образование белого нитевидного кольца на 3-й минуте после наслоения 50%-ной азотной кислоты на мочу соответствует 0,033 % белка в моче. Если нитевидное кольцо образуется тотчас после наслоения реактива, мочу следует развести дистиллированной водой или изотоническим раствором хлорида натрия в 2 раза. При образовании широкого кольца делают четырехкратное разведение (1 часть мочи на 3 части дистиллированной воды или изотонического раствора хлорида натрия). При необходимости делают восьмикратное разведение и т. д. В разведенной моче снова определяют время появления кольца. Полученное разведение умножают на 0,033, и это произведение отражает количественное содержание белка в моче.
Слайд 6Если реакция с сульфасалициловой кислотой дает положительный результат, а при количественном способе

белок в моче не определяется, то считают, что в ней имеются лишь следы белка.
Слайд 7Определение в моче глюкозы
1. Редуктометрические. Почти не используются
2. Колориметрические. Почти не используются
3. Ферментативные:
а)

глюкозооксидазный
- фотометрический по конечной точке
- фотометрический кинетический
- отражательная фотометрия – сухая химия
- электрохимический
б) гексокиназный.
Первые два метода крайне неудобны, токсичны и обладают низкой точностью, поэтому мы на них не будем останавливаться.
Глюкозооксидазный метод
Сегодня наибольшее распространение получили методы, основанные на использовании фермента – глюкозооксидазы. В основе метода лежит следующая реакция:
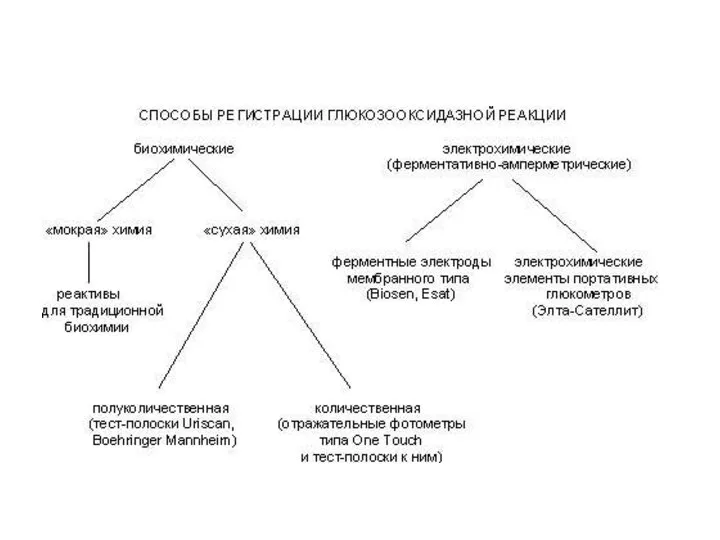
Слайд 9Среди вышеперечисленных способов регистрации наибольшее распространение получил фотометрический биохимический метод, в котором молекулы

перекиси водорода под действием фермента пероксидазы расщепляются с образованием активной формы кислорода – супероксид анион-радикала – О2-, который в свою очередь окисляет хромоген, что приводит к значительному изменению спектра поглощения хромогена.
Слайд 10Наряду с методом фотометрирования по конечной точке, несколько лет назад появились наборы,

в которых реализован кинетический метод фотометрирования. Суть метода состоит в том, что при определенном соотношении активностей глюкозооксидазы и пероксидазы, скорость образования окрашенного соединения некоторое время после внесения пробы в рабочий раствор будет пропорциональна концентрации глюкозы в пробе. Преимущество такого метода состоит в том, что результат не зависит от наличия в пробе других соединений, поскольку поглощение последних стабильно во времени. Этот метод требует применения кинетического фотометра, например Stat Fax 1904+, Stat Fax 3300, полуавтоматических анализаторов, например Clima 15, или автоматических биохимических анализаторов. Измерение концентрации глюкозы из цельной крови удобно выполнять с помощью приборов, работа которых основана на амперометрическом принципе измерения, при помощи специальных ферментных датчиков. Перекись водорода является крайне нестабильным химическим соединением и она может служить источником заряженных частиц. Именно это и используется в ферментных датчиках мембранного типа или электрохимических элементах портативных глюкометров.
Слайд 11Гексокиназный метод
Гексокиназный метод состоит из двух последовательных реакций, но совершенно других:

Слайд 12Регистрация осуществляется при длине волны 340 нм по светопоглощению НАДН. Этот метод

является высокоспецифичным и не дает реакции с другими компонентами сыворотки крови. Гексокиназный метод считается референтным для определения глюкозы. Как правило, он линеен до 50 ммоль/л, что позволило его широко рекомендовать для клиник с эндокринологическими отделениями.










 АИВ инфекциясымен ауыратын науқастағы вирусты гепатиттердің алдын алу және емдеудің ерекшеліктері
АИВ инфекциясымен ауыратын науқастағы вирусты гепатиттердің алдын алу және емдеудің ерекшеліктері Новая коронавирусная инфекция COVID-19
Новая коронавирусная инфекция COVID-19 Влияние лосьона для лица, содержащего гиалуроновую кислоту, на эластичность, гидратацию и коллагеновые показатели кожи лица
Влияние лосьона для лица, содержащего гиалуроновую кислоту, на эластичность, гидратацию и коллагеновые показатели кожи лица 187721 (1)
187721 (1)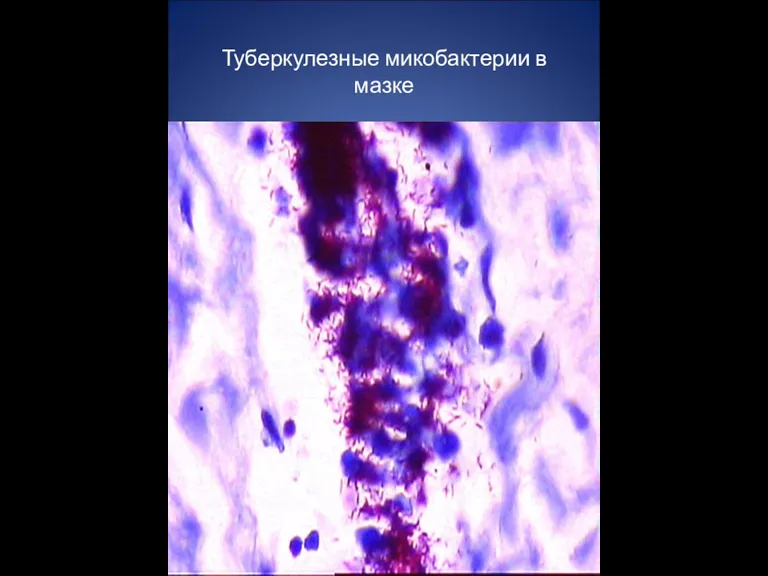 Туберкулезные микобактерии в мазке
Туберкулезные микобактерии в мазке Чистотел против кожных заболеваний
Чистотел против кожных заболеваний Результаты исследования кремов с антивозрастным эффектом
Результаты исследования кремов с антивозрастным эффектом Канцерогенез и иммунная система
Канцерогенез и иммунная система Ультразвуковая диагностика в гинекологии
Ультразвуковая диагностика в гинекологии Частная психопатология
Частная психопатология Полис. Компания Euromed Group - крупнейшая медицинская компания в Санкт-Петербурге
Полис. Компания Euromed Group - крупнейшая медицинская компания в Санкт-Петербурге Минерал 89. Відновлення здорового вигляду шкіри
Минерал 89. Відновлення здорового вигляду шкіри Оказание экстренной медицинской помощи пострадавшим с политравмой
Оказание экстренной медицинской помощи пострадавшим с политравмой Ұрықтың тума ақаулары, эндокрин жүйесі
Ұрықтың тума ақаулары, эндокрин жүйесі Патогенные для человека вибрионы
Патогенные для человека вибрионы Психопатологическая семиотика
Психопатологическая семиотика Патофизиология иммунной системы
Патофизиология иммунной системы Особенности практического применения лечебной липосомальной косметики Айсида
Особенности практического применения лечебной липосомальной косметики Айсида Шаблоны DSD
Шаблоны DSD Лекция_12_Стерилизация_медицинских_изделий_многократного_применения
Лекция_12_Стерилизация_медицинских_изделий_многократного_применения Биохимические исследования при болезнях соединительной ткани. СКВ
Биохимические исследования при болезнях соединительной ткани. СКВ Артериальное давление. Введение
Артериальное давление. Введение Молекулярно-биохимические механизмы опухолевого роста
Молекулярно-биохимические механизмы опухолевого роста Нарушение осанки у школьников
Нарушение осанки у школьников Физиотерапия в стоматологии
Физиотерапия в стоматологии Невынашивание и перенашивание беременности
Невынашивание и перенашивание беременности Профилактика ожирения среди взрослого населения
Профилактика ожирения среди взрослого населения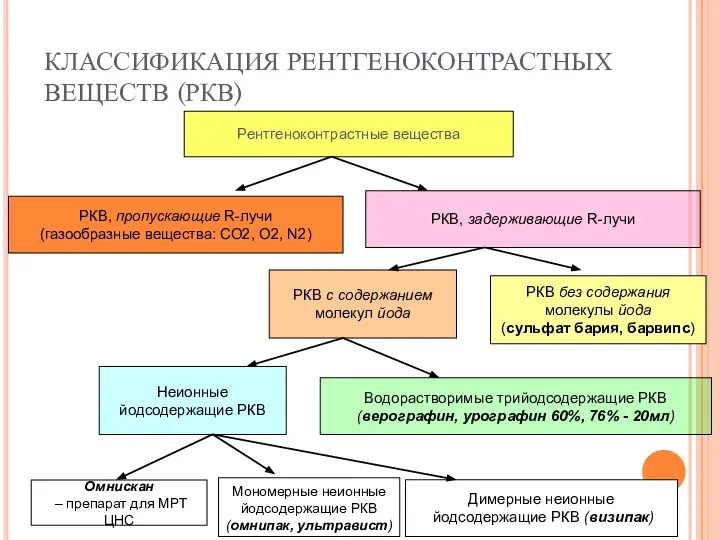 Классификация рентгеноконтрастных веществ (РКВ)
Классификация рентгеноконтрастных веществ (РКВ)