Слайд 2Наследственные болезни крови представляют собой один из важнейших разделов общей клинической гематологии.

К ним, в первую очередь, относятся гемоглобинопатии, анемии, нарушения системы свертывания крови и тромбофилии
Слайд 3Важнейшее практическое значение в медицине имеет учение о группах крови.
В связи

с этим сначала рассмотрим наследование основных групп крови
АВ0 и резус-фактора Rh
Слайд 4Группы крови АВ0 (АВН) и
резус-фактор Rh

Слайд 5Феномен изогемагглютинации заключается в способности сыворотки крови одних людей агглютинировать или склеивать

эритроциты других людей.
В основе этого процесса лежит связывание эритроцитарных гликосфинголипидных антигенов, или агглютиногенов, с природными антителами плазмы крови – агглютининами
Слайд 6Связывание эритроцитов происходит в том случае, если встречаются одноименные агглютиноген и агглютинин.

В настоящее время описано 15 антигенных систем эритроцитов, каждая из которых включает от двух до нескольких десятков антигенов, контролируемых генами с множественными аллелями
Слайд 7Наиболее известными из них являются
группы крови системы АВ0, или ABH.
В

этой системе агглютиногенами являются антигены А, В и Н, а агглютининами — антитела α и β
Слайд 8Антиген Н является предшественником для образования антигенов А и В.
В том

случае, если к антигену Н с помощью фермента гликозилтрансферазы присоединяется N-ацетилгалактозамин,
образуется антиген А,
если же присоединяется галактоза, образуется антиген В
Слайд 9Гликозилтрансфераза кодируется геном AB0,
в котором идентифицированы
3 главных аллеля: A, B

и 0. Аллели A и B кодируют изоформы фермента, пришивающие разные углеводные остатки к предшественнику Н
Слайд 10Аллель 0 — это делеция 1 нуклеотида в гене AB0,
при которой

фермент не синтезируется, и у нулевых гомозигот образуется только предшественник Н.
Аллели A и B доминантны по отношению к аллелю 0 и кодоминантны по отношению друг к другу
Слайд 11Наследование групп крови по системе AB0
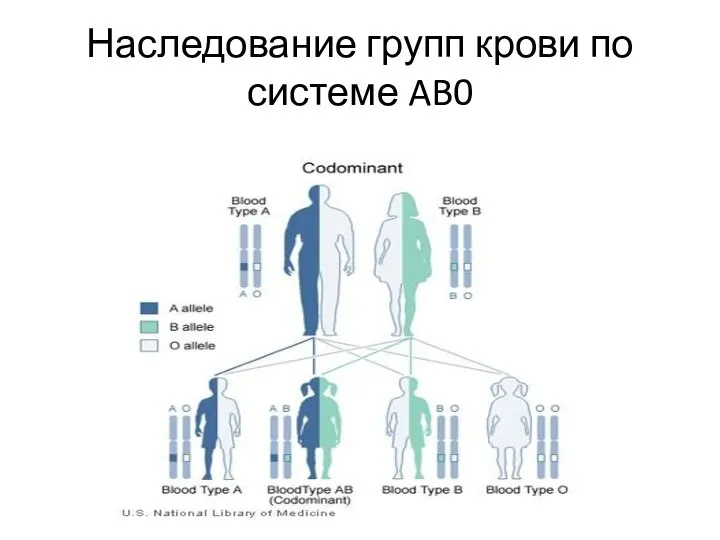
Слайд 12При этом всего могут образовываться 4 группы крови: I, или 0 при

генотипе 00;
II, или A при генотипах AA и A0; III, или B при генотипах BB и B0; IV, или AB при генотипе AB
Слайд 13Группы крови определяют иммунологические свойства агглютиногена,
локализованного на поверхности эритроцитов,
и взаимодействующего

с ними агглютинина, растворенного в сыворотке крови
Слайд 14Взаимодействия между генотипами и фенотипами по системе групп крови АВ0
Группа

Генотип Антигены Антитела
крови эритроцитов сыворотки
I, или 0 00 0 αβ – анти-А
и анти-В
II, или А AA или A0 А β – анти-В
III, или В BB или BO В α – анти-А
IV, или АВ AB АВ 0
Слайд 15Первая, или нулевая группа крови встречается в различных популяциях с частотой от

30 до 40-50%.
Кровь I группы не содержит эритроцитарных антигенов. Поэтому люди с первой, или нулевой группой крови являются «универсальными донорами»
Слайд 16Введениe антигенов А или В лицам с нулевой группой крови приводит к

образованию антител, вызывающих агглютинацию эритроцитов с возможным развитием гемолитического шока
Слайд 17Вторая группа крови, или А встречается среди населения примерно с такой же

частотой, что и первая, в то время как третья группа, или В является более редкой – 10-20%.
У обладателей второй или третьей групп крови вырабатываются антитела соответственно либо против антигена В, либо против антигена А
Слайд 18Четвертая группа крови, или АВ является самой редкой – 3-8%.
У лиц

с такой группой крови антитела против эритроцитарных антигенов в сыворотке крови не вырабатываются, таким образом, они являются «универсальными реципиентами».
Им можно переливать кровь любой группы, однако их эритроцитарную массу можно переливать людям только с той же самой четвертой группой крови
Слайд 19Установлено, что эритроцитарные антигены могут существовать в различных вариантах –
А1, А2,

А3, …, В1, В2, В3 и т.д.
Эти варианты встречаются достаточно редко и не всегда выявляются, что может привести к ошибочному определению групп крови
Слайд 20Поэтому во избежание посттрансфузионных осложнений в настоящее время по жизненным показаниям разрешено

переливание донорской крови
только той же самой группы, что и у реципиента
Слайд 21Другая система групповых антигенов, названная
системой резус-фактора (Rh), находится под более сложным

генетическим контролем.
Она включает три пары антигенов (D, C/c, E/e), кодируемые двумя тесно сцепленными высоко гомологичными генами –
RHD и RHCE
Слайд 22Основная роль в Rh-системе принадлежит антигену D, продукту гена RHD.
При его

наличии кровь является резус-положительной.
Резус-отрицательный фенотип формируется при отсутствии антигена D, обусловленном делецией гена RHD
Слайд 23От 0,2% до 1% людей имеют особый, «слабый» вариант антигена D, обозначаемый

Du.
Причиной появления этого фенотипа являются мутации в гене RHD.
Носители Du-фенотипа также являются резус-отрицательными, им можно переливать только резус-отрицательную кровь
Слайд 24
Антигены C/c и E/e кодируются геном RHCE и образуются в результате альтернативного

сплайсинга.
Доля лиц с резус-положительной принадлежностью – Rh(+) – составляет 85%, остальные 15% - являются "резус-отрицательными" – Rh(-)
Слайд 25Знание групповой принадлежности по Rh-системе имеет определяющее значение для предотвращения резус-конфликта между

матерью и плодом, который может возникнуть во время беременности
Слайд 26Если у резус-отрицательной женщины муж имеет
резус-положительную принадлежность, то с высокой вероятностью

ребенок окажется резус-положительный, и тогда может возникнуть
резус-конфликт
между плодом и матерью
Слайд 27В 15% подобных случаев после
7 недели беременности, когда в крови плода

появляются зрелые эритроциты, в крови матери с Rh(-) начинают вырабатываться специфические противорезусные антитела
Слайд 28Через плаценту они попадают в кровь плода и в отдельных случаях могут

там накапливаться, вызывая агглютинацию эритроцитов и их разрушение. Как правило, первая беременность заканчивается благополучно, мертворождения и выкидыши встречаются редко
Слайд 29Особенно велика вероятность возникновения резус-конфликта
при повторных беременностях.
Во время родов или

медицинском аборте кровь плода может попадать в кровоток матери, и
резус-отрицательная мать будет сенсибилизирована к
резус-положительным
антигенам ребенка
Слайд 30При последующих беременностях резус-несовместимым плодом титр анти-Rh-антител в крови женщины резко возрастает.

Следствием этого процесса является разрушение красных кровяных телец плода и формирование у него желтухи новорожденного, сопровождающейся анемией, отеками, нарушениями слуха и речи, двигательными расстройствами
Слайд 31При такой желтухе имеется риск формирования билирубиновой энцефалопатии, наиболее тяжелым исходом которой

является детский церебральный паралич с эпилептическим синдромом и значительным отставанием психического развития ребенка
Слайд 32Степень поражения ЦНС и
других органов зависит от уровня непрямого билирубина, поступающего

в кровь из разрушенных эритроцитов, и длительности
гипербилирубинемии
Слайд 33Наиболее эффективным средством лечения гемолитической болезни новорожденных является обменное переливание крови в

первые сутки жизни, а иногда и внутриутробно, способствующее удалению продуктов гемолиза и резусных антител матери из крови ребенка
Слайд 34Для профилактики резус-конфликта и гемолитической болезни у плода женщине с отрицательной резус-принадлежностью

при любом внутриматочном вмешательстве во время первой беременности показано введение анти-D-иммуноглобулина.
Этот препарат снижает резус-сенсибилизацию беременной, то есть её чувствительность к резус-фактору и формированию резусных антител
Слайд 35Введение
анти-D-иммуноглобулина при повторных беременностях не показано, так как женщина уже сенсибилизирована,

то есть чувствительна к резус-фактору и имеет резусные антитела
Слайд 37Гемоглобинопатии — это гетерогенная группа наследственных заболеваний, обусловленных мутациями в глобиновых генах.

В организме человека гемоглобин находится в различных изоформах, каждая из которых состоит из четырех полипептидных цепей
Слайд 3898% гемоглобина взрослого человека представлено изоформой HbA, или гемоглобином А, в состав

которого входят две α- и две β-цепи. Его формула записывается как HbA(α2; β2).
От 2 до 2,5% приходится на долю гемоглобина HbA 2,в котором β-цепь заменена на δ-цепь – HbA2(α2; δ2)
Слайд 39В первой половине беременности у плода присутствуют необычные формы эмбрионального гемоглобина
HbCower2 (α2;

ε2)
который в постнатальном периоде не обнаруживается.
Во второй половине внутриутробного развития преобладающим у плода является фетальный гемоглобин
HbF(α2; γ2),
в котором β-цепь заменена на γ-цепь
Слайд 40В течение первого года жизни ребенка происходит замена фетального гемоглобина на гемоглобин

А, и у взрослых фетальный гемоглобин составляет не более 0,1-2%
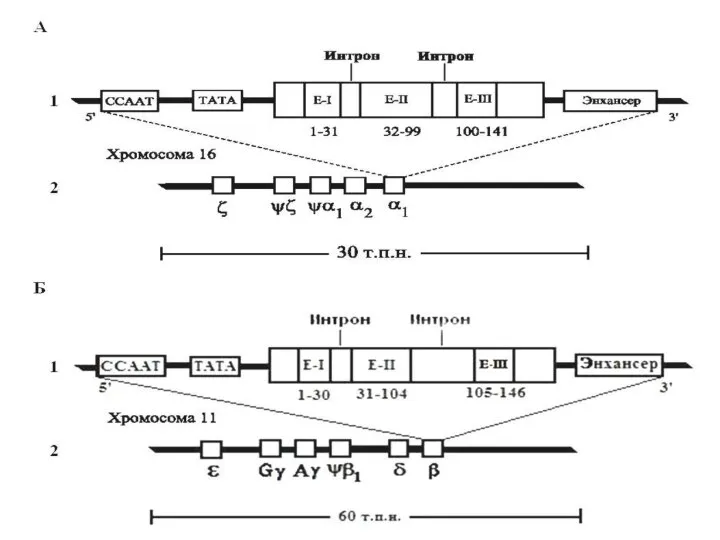
Слайд 41Гены различных цепей гемоглобина кластерированы в двух различных цитогенетических областях и являются

классическим примером генных семейств, содержащих псевдогены.
Альфа-цепь кодируется двумя дуплицированными генами
HBA1 и HBA2, расположенными в области 16pter-p13.3
Слайд 42Продукты этих генов идентичны друг другу, но характер их экспрессии различен.
Ген

HBA2 экспрессируется значительно интенсивнее гена HBA1.
В непосредственной близости от гена HBA2 расположены 2 псевдогена HBAP1
Слайд 43Остальные цепи гемоглобина
(β, δ, γ и ξ) кодируются соответственно генами
HBB,

HBD, HBG1, HBG2 (2 гена для γ-цепи) и HBE1, расположенными в области 11p15.5
Слайд 45Порядок локализации генов на хромосоме соответствует последовательности их экспрессии в онтогенезе, что

ясно указывает на существование единой регуляторной системы для всего этого кластера генов
Слайд 46При снижении экспрессии одного из генов кластера, компенсаторно повышается экспрессия других генов,

и образуются гемоглобины, не свойственные соответствующему периоду развития
Слайд 47В настоящее время описано большое количество мутаций в различных генах гемоглобинов, которые

приводят к развитию гемоглобинопатий – гетерогенной группы наследственных болезней крови, среди которых ведущее положение занимают
α- и β-талассемии, а также серповидноклеточная анемия
Слайд 48α-талассемии – это клинически полиморфная и генетически гетерогенная группа аутосомно-рецессивных заболеваний, обусловленных

мутациями в двух α-глобиновых генах.
В типичных случаях болезнь характеризуется гипохромной микроцитарной анемией
Слайд 49Гемолиз эритроцитов возникает в результате их перегрузки железом, нарушающим эритропоэз и оказывающим

повреждающее действие на мембраны клеток.
Анемия может обостряться при присоединении интеркуррентных инфекций и приеме некоторых лекарственных препаратов, например, из группы сульфаниламидов
Слайд 50У 80% больных развивается гепатоспленомегалия и у 30% - скелетные деформации.
α-талассемии

встречаются во многих частях мира, но особенно распространены в южной Азии и на Филиппинах
Слайд 51Основной тип мутаций в α-глобиновых генах (HBA1 и HBA2) — это протяженные

делеции, которые могут захватывать один или оба гена, а также находиться в гомозиготном или компаунд-гетерозиготном состояниях.
В результате в популяциях может наблюдаться полиморфизм по варьирующему от 4 до 0 числу копий
α-глобиновых генов
Слайд 52При этом в разных популяциях найдены специфические мажорные делеции.
Среди них самыми

частыми в южной Азии, на Филиппинах и Средиземноморье являются соответственно делеции, получившие название SEA, FIL, MED, а также некоторые другие (alpha3.7, alpha4.2)
Слайд 53Делеция одной копии любого из двух генов, как правило, не имеет клинических

проявлений. Делеция двух копий
α-глобиновых генов приводит к развитию микроцитоза
Слайд 54Классическая картина хронической гемолитической анемии, сопровождающаяся образованием новых типов гемоглобина, например, гемоглобина

HbH, состоящего из 4 β-цепей, наблюдается при делеции трех копий α-глобиновых генов.
Подобные делеционные формы идентифицируются у 83% больных
α-талассемией
Слайд 55В остальных случаях чаще всего наблюдается сочетание делеций двух копий генов с

гетерозиготными точковыми мутациями в одном из генов HBA1 или HBA2
Слайд 56Некоторые точковые мутации затрагивают район α-цепей, важный для осуществления их контактов с

β-цепями.
В этом случае образуется гемоглобин, состоящий из
2 γ- и 2 α-цепей
Слайд 57При делеции четырех копий α-глобиновых генов α-цепи полностью отсутствуют и образуется гемоглобин,

состоящий из 4 γ-цепей –
это состояние несовместимо с жизнью
Слайд 58β-талассемии – это группа клинически полиморфных аутосомно-рецессивных заболеваний, обусловленных мутациями в β-глобиновом

гене.
Заболевание часто встречается в Центральной Африке, Индии, странах Средиземноморья, Ближнего и Среднего Востока, в том числе, в Азербайджане, Узбекистане и Армении
Слайд 59Оказалось, что в тех же регионах мира распространен малярийный плазмодий, вызывающий тяжелое

протозойное заболевание – малярию.
Гетерозиготные носители мутаций в гене HBB обладают повышенной устойчивостью к малярии
Слайд 60Частота гетерозиготного носительства мутации в гене
β-глобина в этих популяциях достигает 5-8%.

Максимальная распространенность
β-талассемии зарегистрирована на Кипре (14%) и в
Сардинии (12%)
Слайд 61В зависимости от типа мутации и наличия β-глобиновых цепей выделяют β0- и

β+-талассемию. К β0-талассемии приводят мутации с преждевременной терминацией трансляции, при которых β-цепь полностью отсутствует
Слайд 62Примером тяжелой формы
β0-талассемии является
анемия Кули.
Болезнь проявляется в возрасте от

нескольких недель до 2 лет бледностью и иктеричностью,
иногда с медным оттенком кожи и слизистых вследствие гемолитической анемии, приступами лихорадки
Слайд 63При анализе крови выявляется тяжелая гипохромная анемия со снижением содержания гемоглобина и

уменьшением количества эритроцитов и изменением их формы – пойкилоцитозом.
Сопутствующими проявлениями заболевания являются задержка роста, гепатоспленомегалия, черепно-лицевой дизморфизм
Слайд 64Часто возникают осложнения в виде трофических язв, цирроза печени, мочекислого диатеза и

гемосидероза.
Причиной развития
β+-талассемии чаще всего являются регуляторные мутации, приводящие к снижению количества β-цепи и заменой её в зрелом гемоглобине
на γ-цепь
Слайд 65К редким вариантам β-талассемии относится персистирование фетального гемоглобина,
при котором не происходит

его замены на гемоглобин взрослого. Возникновение симптомов талассемии может наблюдаться при мутациях в регуляторном элементе β-глобиновых генов (LCR)
Слайд 66Одна из миссенс-мутаций (S) в гене HBB, сопровождающаяся заменой глютамина на валин

в 6 положении β-цепи, приводит к развитию
серповидноклеточной анемии.
SS-гомозиготы вместо нормального гемоглобина НbА имеют вариант НbS, который полимеризуется с образованием волокон или пучков
Слайд 67Это приводит к дефекту мембраны эритроцитов, обуславливающему их серповидную форму. Серповидные клетки

увеличивают вязкость крови и мешают ее циркуляции в мелких кровеносных сосудах
Слайд 68Такие эритроциты теряют пластичность, закупоривают капилляры и гемолизируются, вызывая развитие очагов ишемии

и инфаркты с выраженной гипоксией и дистрофией внутренних органов и тканей
Слайд 69Серповидноклеточная анемия является примером наследования с неполным доминированием. Гетерозиготные носители мутации (Ss)

в гене гемоглобина имеют промежуточную серповидную форму эритроцитов, которая обеспечивает им относительно нормальный фенотип
Слайд 70В обычных условиях у этих лиц анемия не выявляется, так как в

их крови содержится нормальный гемоглобин HbA, но при низком парциальном давлении кислорода, характерном, например, для высокогорья, патология прогрессирует
Слайд 72Не только гемоглобинопатии, но и многие другие наследственные дефекты могут привести к

развитию анемии.
Аутосомно-рецессивные или Х-сцепленные рецессивные формы неспецифической гемолитической анемии могут быть обусловлены наследственной недостаточностью многих эритроцитарных ферментов
Слайд 73Это – глюкозо-6-фосфатдегидрогеназа (G6PD), уридин-5'-монофосфат-гидролаза (UMPH1), пируваткиназа (PKLR), фосфоглицераткиназа (PGK1), глюкозофосфатизомераза (GPI),

аденилаткиназа (AK1)
Слайд 74Генетически гетерогенная группа Х-сцепленной и аутосомно-рецессивной анемии Фанкони характеризуется высокой геномной нестабильностью,

чувствительностью к агентам, вызывающим перекрестные сшивки между комплементарными нитями ДНК и предрасположенностью к онкологическим заболеваниям
Слайд 75Анемия Фанкони, являясь одной из форм апластической анемии, клинически проявляется прогрессирующей панцитопенией

и нередко сопровождается аномалиями развития различных органов и тканей
Слайд 76Одним из наиболее ранних проявлений заболевания является функциональная недостаточность костного мозга, обусловленная

нарушением пролиферации и дифференцировки клеток костного мозга
Слайд 77В настоящее время идентифицированы 15 генов, мутации которых приводят к анемии Фанкони.

Продукты этих генов являются белками
репарационных комплексов, обеспечивающих поддержание геномной стабильности
Слайд 78Центральным из этих путей является
активация и транспорт
к месту повреждения ДНК

белков, кодируемых генами
FANCD2 и FANCI.
Вслед за этим происходит координация ядерных репарационных комплексов
Слайд 79Мутации в гене FANCD2 являются самой частой причиной анемии Фанкони.
Активация продукта

гена FANCD2 происходит при участии
лигазного комплекса, 8 белков которого кодируются генами, мутантными при других генетических типах этого заболевания (FANCA, FANCB, FANCC, FANCE, FANCF, FANCG, FANCL, FANCМ )
Слайд 80Репарация перекрестных сшивок ДНК
происходит при участии многих других белков, 5 из

которых кодируются генами, мутантными при остальных генетических типах анемии Фанкони — FANCD1, FANCJ, FANCN, FANCO, FANCP
Слайд 81Врожденная дизэритропоэтическая анемия — это гетерогенная группа заболеваний, обусловленных неэффективным эритропоэзом.
При

редком аутосомно-рецессивном типе I, наряду с макроцитарной мегалобластной анемией, дополнительно выявляются вторичный гемохроматоз, костные аномалии в форме акродизостоза и сколиоза, дисплазия ногтевых пластин
Слайд 82Причиной заболевания являются мутации в гене коданина-1 (CDAN1).
Коданин-1 – это высоко

консервативный белок, необходимый для выживания клеток и их прохождения по клеточному циклу
Слайд 83При наиболее частом II типе заболевания, характеризующимся нормоцитарными, би- или многоядерными эритроцитами

с двойными цитоплазматическими мембранами, выявляемыми при электронной микроскопии, у больных обнаруживаются мутации в гене SEC23B.
Продукт этого гена участвует в дифференцировке и цитокинезе клеток эритроидного ряда
Слайд 84Редкий тип III умеренной дизэритропоэтической анемии, который называется также доброкачественным эритроретикулезом, наследуется

по аутосомно-доминантному типу и характеризуется многоядерным эритробластозом — «гигантобластозом», при котором количество ядер достигает 10-12. Обнаружено сцепление этой формы заболевания с локусом 15q21
Слайд 85Аутосомно-доминантная врожденная дизэритропоэтическая анемия
IV типа, обусловленная мутациями в гене транскрипционного активатора

(KLF1), по своим клиническим характеристикам отличается от предыдущих форм
Слайд 86Сидеробластическая анемия характеризуется присутствием в крови эритроидных сидеробластов. Ведущими клиническими проявлениями являются:

гипохромная анемия, присутствие двух типов эритроцитов (микроцитов и нормоцитов), наличие в костном мозге кольцевых сидеробластов, особенно на поздних стадиях формирования эритроидных предшественников
Слайд 87Характерны системная перегрузка железом в результате хронического неэффективного эритропоэза и часто положительный

гематологический ответ (ретикулоцитарный криз) на терапевтические дозы витамина В6 и пиридоксальфосфата.
Возраст начала заболевания может варьировать в очень широких пределах от внутриутробного периода до глубокой старости
Слайд 88Наследственные формы заболевания включают в себя два типа — Х-сцепленную рецессивную, пиридоксин(витамин

В6)-зависимую, обусловленную мутациями в гене ALAS2 и аутосомно-рецессивную пиридоксин-рефрактерную анемию, обусловленную мутациями в гене SLC25A38
Слайд 89Продуктом гена ALAS2 является эритроид-специфический фермент – дельта-аминолевулинатсинтетаза, катализирующая первый шаг в

биосинтезе гема
Слайд 90У больных с аутосомно-рецессивной формой заболевания также снижен уровень дельта-аминолевулинатсинтетазы 2
в

результате недостаточности одного из митохондриальных транспортеров, кодируемых геном SLC25A38
Слайд 91В12-дефицитная, или мегалобластная пернициозная (злокачественная) анемия обусловлена дефицитом витамина В12, который связан

с его недостаточным поступлением в организм с пищей
Слайд 92Редкие моногенные формы В12-дефицитной пернициозной анемии связаны с нарушением усвоения витамина В12

в организме
Слайд 93Поступающий с пищей витамин В12 образует комплекс с внутренним желудочным фактором, который

затем взаимодействует со специфическим рецептором. Образование этого комплекса и его взаимодействие с рецептором необходимо для всасывания витамина В12
Слайд 94Среди наследственных типов мегалобластной анемии наиболее известным является
синдром Имерслунд-Гресбека, характеризующийся одновременным

поражением у детей чаще всего в возрасте 1-4 лет пищеварительной и нервной системы, дефектами кожных покровов. В 90% случаев болезнь сопровождается протеинурией.
Слайд 95Два генетических типа заболевания – финский и норвежский – обусловлены мутациями в

генах CUBN и AMN.
Продукты этих генов участвуют в образовании рецептора для комплекса витамина В12 с внутренним желудочным фактором.
В возрасте 20 лет симптомы заболевания нередко исчезают самостоятельно
Слайд 96Более редкий генетический тип пернициозной анемии с дефицитом витамина В12 обусловлен наследственной

недостаточностью внутреннего желудочного фактора,
кодируемого геном GIF.
При наличии гиперхромной мегалобластной анемии тяжелой степени и мегалобластном типе кроветворения наблюдается фуникулярный миелоз, глоссит и поражения других органов и систем
Слайд 97Наследственная В12-дефицитная мегалобластная анемия, сочетающаяся с сахарным диабетом и нейросенсорной тугоухостью, является

одним из проявлений синдрома дисфункции тиаминового (витамина В1) метаболизма,
обусловленного мутациями в гене тиаминового транспортера SLC19A2
Слайд 98Аутосомно-рецессивная мегалобластная анемия нередко сочетается с задержкой психического развития, генерализованными судорожными приступами,

развивающимися в младенческом возрасте, с последующим формированием абсанс-эпилепсии и трудностей в обучении
Слайд 99Этот генетический тип мегалобластной анемии обусловлен наследственной недостаточностью ключевого фермента
метаболизма фолатов

– дигидрофолатредуктазы, кодируемой геном DHFR. Назначение фолиевой кислоты может в некоторых случаях улучшить состояние больного
Слайд 100Железодефицитная рефрактерная микроцитарная анемия без признаков нарушения метаболизма железа или кровотечений обусловлена

мутациями в гене TMPRSS6. Продуктом этого гена является трансмембранная сериновая протеаза, участвующая в расщеплении антимикробного пептида гепсидина — ключевого регулятора абсорбции железа и снижения его токсичности
Слайд 101Напомним, что мутации в гене гепсидина приводят к аутосомно-рецессивному ювенильному гемохроматозу типа

2B.
Прием препаратов железа при данной форме железодефицитной анемии неэффективен, так как они не всасываются в кишечнике
Слайд 102Гетерогенная группа аутосомно-доминантных младенческих форм анемии Блекфена-Даймонда, сопровождающихся врожденной эритроидной дисплазией, обусловлена

мутациями в генах различных рибосомных белков. В 30-40% случаев у больных наблюдаются черепно-лицевые аномалии и другие врожденные пороки развития, затрагивающие чаще всего верхние конечности
Слайд 103Характерным является хроническое течение анемии, однако у части больных, чаще в периоде

пубертата, отмечается спонтанная ремиссия.
Лечение анемии Блекфена-Даймонда заключается в назначении глюкокортикостероидов
Слайд 104В настоящее время идентифицированы 10 генов рибосомных белков, суммарно объясняющих более 50%

всех случаев анемии Блекфена-Даймонда.
Наиболее частой причиной этого заболевания являются гетерозиготные мутации в гене рибосомного белка S19 (RPS19)
Слайд 105Апластическая анемия — заболевание кроветворной системы, относящееся к миелодисплазиям и выражающееся в

резком угнетении или прекращении роста и созревания клеток всех ростков кроветворения в костном мозге (панмиелофтиз).
Это достаточно редкая и тяжелая патология, поражающая в год от 2 до 5 человек на миллион населения
Слайд 106Без лечения больные с тяжелыми формами апластической анемии погибают в течение нескольких

месяцев. При своевременном адекватном лечении прогноз заболевания относительно благоприятный
Слайд 107Согласно современным представлениям ключевым фактором в понимании патогенеза апластической анемии является положение

о главенствующей роли дефекта стволовой клетки крови, возникающего вследствие воздействия неизвестного пускового агента
Слайд 108Этот дефект близок по характеру или идентичен соматической мутации. Об этом свидетельствует

восстановление кроветворения у больных после трансплантации аллогенного костного мозга, содержащего нормальные стволовые клетки.
В 75% случаев заболевание носит идиопатический характер
Слайд 109В 15% случаев причиной аплазии является прием лекарственных препаратов или инфекционный процесс,

хотя наследственные причины подобной индивидуальной чувствительности до сих пор остаются неизвестными
Слайд 110В 5-10% случаев заболевание носит семейный характер или сочетается с другими соматическими

аномалиями.
К наследственным формам апластической анемии относится также и анемия Фанкони
Слайд 111В настоящее время идентифицированы гены, гетерозиготные мутации в которых повышают риск развития

апластической анемии.
Это гены гамма-интерферона (IFNG), нибрина — одного из ферментов репарации двунитевых разрывов ДНК (NBS1), перфорина-1 — пор-формирующего белка цитолитических гранул, участвующего в формировании мембранных пор (PRF1), и белка, предположительно участвующего в процессинге рРНК (SBDS)
Слайд 112Кроме того, укорочение теломер, обусловленное присутствием гетерозиготных мутаций в генах TERT и

TERC, также повышает риск развития апластической анемии в сочетании с фиброзом легких и печени
Слайд 114В основе развития Х-сцепленных рецессивных форм гемофилии А и гемофилии В лежат

наследственные дефекты двух факторов свертывания крови – VIII и IX –, обусловленные мутациями в генах F8C и F9 соответственно
Слайд 115При любой из этих форм наблюдаются нарушения свертывания крови, и самые незначительные

травмы без специальной гематологической помощи могут привести больного к
летальному исходу.
Частота гемофилии А составляет 1 : 5000 новорожденных мальчиков, гемофилия В встречается в 10 раз реже
Слайд 116Отметим, что у женщин – носительниц мутаций в одном из генов гемофилии

в отдельных случаях также наблюдается склонность к кровотечениям, что выражается в обильных месячных и длительных кровотечениях
во время родов.
В настоящее время возможна пренатальная диагностика
гемофилии А и В
Слайд 117Фактор VIII – это большой сывороточный гликопротеин, который функционирует в коагуляционном каскаде

как кофактор для активации фактора X. Протеолитически он активируется множеством коагуляционных ферментов, включая тромбин.
В неактивном состоянии фактор VIII тесно ассоциирован с
фактором Виллебранда
Слайд 118Около 10% всех идентифицированных мутаций в гене F8С – делеции одного или

нескольких смежных нуклеотидов. Остальные мутации точковые –
миссенс- или нонсенс-типа.
В 45% случаев у больных с тяжелыми формами гемофилии А обнаруживаются протяженные инверсии, которые затрагивают большую часть гена F8С от 5'-нетранслируемой области до 22 интрона включительно
Слайд 119Подобные инверсии полностью инактивируют ген F8С.
Их возникновение связано с особенностями молекулярной

структуры гена F8С
Слайд 120Около 14% матерей больных мальчиков являются соматическими или гонадными мозаиками, и вероятность

повторного рождения больного ребенка у них также повышена
Слайд 121Фактор IX в плазме крови находится в виде гетеродимера, состоящего из двух

полипептидных цепей (легкой и тяжелой), ковалентно связанных между собой дисульфидным мостиком
Слайд 122Он циркулирует в виде неактивной формы до тех пор, пока не произойдет

протеолитическое высвобождение активирующего его пептида, после чего фактор IX принимает конформацию активной сериновой протеазы
Слайд 123Его роль в свертывании крови связана с активацией фактора X посредством взаимодействия

с ионами кальция, фосфолипидами мембраны и фактором VIII
Слайд 124Для генов F8 и F9 характерна высокая частота возникновения мутаций
(4х10–6 за

поколение), причем мутации значительно чаще возникают в мужских половых клетках, чем женских.
Считается, что вероятность получения больным ребенком возникшей de novo мутации от отца в 11 раз выше, чем от матери
Слайд 125При этом с возрастом вероятность возникновения новых мутаций в гене F9 у

отца повышается.
По разным оценкам считается, что в спорадических случаях вероятность гетерозиготного носительства мутации у матери составляет лишь 80%.
В 40% случаев при тяжелых формах гемофилии В у больных обнаруживаются делеции в гене F9 различной протяженности
Слайд 126Точковые мутации в промоторной области гена связаны с более легкими формами заболевания,

такими, например, как Лейденская гемофилия, при которой у больных к возрасту половой зрелости наступает улучшение многих клинических показателей, в частности, исчезает геморрагический синдром
Слайд 128Болезнь Виллебранда —
это частое наследственное заболевание крови, проявляющееся спонтанными кровотечениями. Распространенность

болезни Виллебранда – 1 случай на 800 - 1000 человек
Слайд 129Основными клиническими проявлениями заболевания являются обильные носовые и десневые кровотечения, кровотечения из

внутренних органов с образованием гематом, меноррагии, длительные кровотечения после хирургических вмешательств и травм
Слайд 130В основе патогенеза лежат нарушения агрегации тромбоцитов, возникающие вследствие недостаточности
фактора Виллебранда

(ФВ)
— большого мультимерного белка, играющего ключевую роль в адгезии тромбоцитов к коллагену и их агрегации, а также служащего переносчиком для фактора VIII свертывания крови
Слайд 131Болезнь Виллебранда делится на 3 основных типа.
При первом доброкачественном типе, который

диагностируется в 60-80% случаев, наблюдается умеренный дефицит ФВ с сохранением его функциональной активности.
При этом уровень фактора VIII свертывания крови снижен до 5-30% по сравнению с нормой
Слайд 132Второй тип заболевания, характеризующийся структурными нарушениями ФВ, выявляется у
10-30% больных.
В

этом случае у больных может быть нарушена функция ФВ, связанная с агрегацией тромбоцитов, или теряется его способность связывать фактор VIII
Слайд 133Самый тяжелый третий тип заболевания обусловлен значительной количественной недостаточностью ФВ (менее 1%

нормы) или его полным отсутствием.
В этом случае у больных наблюдаются интенсивные рецидивирующие геморрагии, сопровождающиеся выраженной анемизацией.
Этот редкий тип заболевания встречается с частотой 1 случай на миллион населения и составляет не более 1-5% среди всех больных
Слайд 134Наследуется болезнь Виллебранда по аутосомно-доминантному типу с неполной пенетрантностью.
Все клинические типы

болезни Виллебранда обусловлены гетерозиготными мутациями в гене VWF, спектр которых достаточно разнообразен
Слайд 135Большинство составляют миссенс-мутации, наиболее частой из которых является R1205H.
На проявление мутаций

могут оказывать влияние многие факторы, такие как тиреоидные гормоны, эстрогены, разные виды стресса, возраст
Слайд 136Однако наибольшее модифицирующее влияние оказывает присутствие нулевой группы крови по системе АВ0.

Это объясняется тем, что глюкозилтрансфераза, отсутствующая у носителей 0 группы крови, участвует в процессинге ФВ, повышая его устойчивость ко многим эндогенным и экзогенным факторам
Слайд 137Лечение при болезни Виллебранда определяется типом заболевания и выраженностью геморрагического синдрома.
Так,

при первом типе болезни показан десмопрессин – синтетический аналог вазопрессина, который оказывает вазопрессорное, антидиуретическое действие и стимулирует выработку фактора Виллебранда и VIII коагуляционного фактора
Слайд 138При тяжелых формах используют вирусинактивированные
(не содержащие вирусов
гепатита В и С)

концентраты,
включающие в себя фактор Виллебранда
(препарат "Вилате")
Слайд 140В настоящее время достигнут определенный прогресс в выявлении генетических факторов риска тромбофилии

– нарушений гемостаза, обуславливающих повышенную склонность к развитию тромбозов кровеносных сосудов различного калибра и локализации, а также тромбоэмболий и
инфарктов органов
Слайд 141При наследственной тромбофилии значительно повышен риск развития в течение жизни венозных тромбозов

и тромбоэмболии легочной артерии
Слайд 142К генетическим маркерам наследственной тромбофилии относят наследственные дефициты
белков С, S и

антитромбина,
а также мутации в генах факторов свертывания крови V и II, или протромбина (F5 и F2)
Слайд 143Протеины С и S, а также протромбин – синтезируемые в печени витамин

К-зависимые сывороточные гликопротеины, являются ключевыми компонентами
антикоагулянтной системы
Слайд 144Протеин С активируется на поверхности эндотелия сосудов при помощи
тромбин-тромбомодулинового комплекса.
Действуя

как сериновая протеаза, он расщепляет активированные формы факторов V и VIII
свертывания крови
Слайд 145Белок S является кофактором активированного белка С.
Фактор II свертывания крови конвертируется

в тромбин фактором Xa в присутствии фосфолипидов, кальция и фактора Va
Слайд 146Активированный тромбин конвертирует фибриноген в фибрин, стимулируя тем самым агрегацию тромбоцитов, и

в свою очередь активирует факторы V, VIII и XIII
Слайд 147Фактор V свертывания крови циркулирует в крови в неактивной форме.
Он активируется

тромбином и действует как кофактор при конверсии протромбина в тромбин.
Активированный фактор Va инактивируется активированным белком С
Слайд 148Главным ингибитором тромбина является антитромбин III, принадлежащий к суперсемейству ингибиторов сериновых протеиназ

(серпинов)
Слайд 149Гетерозиготные мутации в генах протеина С (PROC) и S (PROS1) приводят к

двум редким формам наследственной тромбофилии. Наследственная недостаточность антитромбина III, кодируемого геном AT3D, является генетическим фактором риска развития
венозных тромбозов
Слайд 150Однако мутации в генах
PROC, PROS1 и AT3D
являются редкой причиной наследственных

тромбофилий, так как их суммарные частоты в популяции не превышают 0.4% и достигают 2% среди пациентов с венозными тромбозами. Как правило, эти нарушения выявляются при анализе коагулограммы
Слайд 151Главной причиной наследственной тромбофилии является присутствие гомозиготных и гетерозиготных мутаций в генах

F2 и F5.
В гене F5 идентифицирована миссенс-мутация R506Q, затрагивающая сайт
расщепления фактора Va
активированным белком C
Слайд 152В результате фактор Va становится устойчивым к действию активированного белка С.
Замена

R506Q получила название Лейденской мутации, или Лейденского фактора V
Слайд 153Её гетерозиготное носительство повышает риск развития венозной тромбоэмболии в 5 раз, причем

в этом случае тромбоз чаще всего начинается с глубоких вен.
Частота гетерозигот по Лейденскому фактору V в различных популяциях мира колеблется в пределах от
2% до 7%
Слайд 154Некоторые внешние факторы могут резко увеличивать частоту тромбозов при наличии Лейденской мутации.

Это – хирургические вмешательства, прием пероральных контрацептивов, беременность, повреждения сосудов и вынужденная обездвиженность больного
Слайд 155У гомозигот по Лейденской мутации, которые встречаются в популяциях значительно реже, риск

тромбозов и тромбоэмболии составляет десятки процентов и может достигать 100% при действии провоцирующих факторов
Слайд 156В гене F5 описаны также и другие мутации, которые в гомозиготном или

компаунд-гетерозиготном состоянии приводят к недостаточности фактора V и увеличению риска венозных тромбозов. В некоторых случаях подобные мутации обнаруживаются у больных с одной из форм геморрагического диатеза – парагемофилией
Слайд 157Присутствие инактивирующих мутаций в гене F5 в компаунде с Лейденским фактором V

(псевдогомозиготность по Лейденскому фактору V) значительно увеличивает риск развития тромбозов
Слайд 158Спектр мутаций в гене F2 также хорошо изучен.
Мажорной является замена G20210A.

Носительство этой мутации увеличивает риск тромбозов в 3 раза, а при сочетании с Лейденским фактором V – до 80 раз, хотя такое сочетание двух неблагоприятных аллелей крайне редко встречается в популяции
Слайд 159Необходимо учитывать, что риск развития венозных тромбозов резко возрастает при сочетании наследственной

предрасположенности к тромбофилии с внешними модифицирующими факторами.
В настоящее время показаниями для генетического тестирования с целью исключения наследственной тромбофилии являются следующие:
Слайд 1601. наличие венозной тромбоэмболии в семейном анамнезе;
2. первый случай венозной тромбоэмболии

в возрасте до 50 лет;
3. рецидивирующая венозная тромбоэмболия;
4. прием пероральных контрацептивов или наличие гормонзаместительной терапии;
5. привычное невынашивание беременности
Слайд 161 Разработаны схемы ведения и лечения беременных женщин с наследственными факторами предрасположенности к

тромбофилии































































































































































 Экссудативное воспаление
Экссудативное воспаление Федеральный закон Об основах охраны здоровья граждан в РФ № 323-ФЗ
Федеральный закон Об основах охраны здоровья граждан в РФ № 323-ФЗ Туристический маршрут в музей-заповедник Прохоровское поле
Туристический маршрут в музей-заповедник Прохоровское поле Аномалии развития зубочелюстной системы
Аномалии развития зубочелюстной системы Дерматомикоз. Клинический случай
Дерматомикоз. Клинический случай Патологическая анатомия. Препараты
Патологическая анатомия. Препараты Клиническая картина различных форм эндометриоза
Клиническая картина различных форм эндометриоза Оздоровительный туризм
Оздоровительный туризм Гломерулонефриты
Гломерулонефриты Правильное питание в современном мире
Правильное питание в современном мире Опухоль. Канцерогенные факторы
Опухоль. Канцерогенные факторы Заболевания кожи и её придатков
Заболевания кожи и её придатков Статистика COVID-19 в зависимости от процента вакцинированных
Статистика COVID-19 в зависимости от процента вакцинированных Синдром обширного просветления легочного поля
Синдром обширного просветления легочного поля Концептуальный аппарат нейропсихологии
Концептуальный аппарат нейропсихологии Вакцинация - защита от болезней
Вакцинация - защита от болезней Остеомієліт щелеп: Етіологія, патогенез, класифікація, лікування
Остеомієліт щелеп: Етіологія, патогенез, класифікація, лікування Нарушение белкового обмена при патологии печени
Нарушение белкового обмена при патологии печени Геномика, нысандары, жіктелуі
Геномика, нысандары, жіктелуі Osteopatia apuntes dorsal
Osteopatia apuntes dorsal Патофизиология седины
Патофизиология седины Спектральные методы анализа магнитных энцефалограмм
Спектральные методы анализа магнитных энцефалограмм Новинки. Линия Crème N°2. Контекст Payot
Новинки. Линия Crème N°2. Контекст Payot Тема 8-9_Первая помощь при неотложных состояниях1
Тема 8-9_Первая помощь при неотложных состояниях1 Перспективы применения новых дезинфицирующих средств с целью профилактики ИСМП
Перспективы применения новых дезинфицирующих средств с целью профилактики ИСМП Лечебная физкультура при лечении дефектов осанки
Лечебная физкультура при лечении дефектов осанки Antibody Production
Antibody Production Синдромная патология
Синдромная патология