Слайд 2Химиотерапевтические препараты – это лекарственные вещества, используемые для подавления жизнедеятельности и уничтожения

микроорганизмов в тканях и средах больного, обладающие избирательным, этиотропным действием.
По направленности действия химиотерапевтические препараты делят на:
противопротозойные;
противогрибковые;
противовирусные;
антибактериальные.
Слайд 3По химическому строению выделяют несколько групп химиотерапевтических препаратов:
Сульфаниламидные препараты (сульфаниламиды). Они нарушают

процесс получения микробами необходимых для жизни и развития ростовых факторов – фолиевой кислоты и др. веществ. К этой группе относят стрептоцид, норсульфазол, сульфаметизол, сульфаметаксазол
Производные нитрофурана. Механизм действия состоит в блокировании нескольких ферментных систем микробной клетки. К ним относят фурацилин, фурагин, фуразолидон, нитрофуразон и др.
Хинолоны. Нарушают различные этапы синтеза ДНК микробной клетки. К ним относят налидиксовую кислоту, циноксацин, норфлоксацин, ципрофлоксацин.
Слайд 4Азолы – производные имидазола. Ингибируют биосинтез стероидов, что приводит к повреждению наружной

клеточной мембраны грибов и повышению ее проницаемости. К ним относят клотримазол, кетоконазол, флуконазол и др.
Диаминопиримидины. Нарушают метаболизм микробной клетки. К ним относят триметоприм, пириметамин.
Антибиотики – это группа соединений природного происхождения или их синтетических аналогов.
Слайд 5Антибиотики – это химиотерапевтические препараты из химических соединений биологического происхождения (природные), а

также их полусинтетические производные и синтетические аналоги, которые в низких концентрациях оказывают избирательное повреждающее или губительное действие на микроорганизмы и опухоли.
Требования, предъявляемые к антибактериальным препаратам:
Они должны растворяться в воде, поскольку только в таком виде могут быть доставлены во внутреннюю среду организма.
Препараты должны быть достаточно стабильны во внутренней среде организма, но не накапливаться в нем.
Антибактериальные препараты должны быть безвредны, минимальные побочные действия и отсутствовать тератогенные и мутагенные эффекты.
Слайд 6Классификация антибиотиков
В основу классификации антибиотиков положены разные принципы:
1. По способу получения (природные,

синтетические и полусинтетические).
2. По направленности действия (антибактериальные, противогрибковые, противоопухолевые).
3. По числу видов (широкоспекторные, узкого спектра действия).
4. По происхождению продуцентами большинства антибиотиков являются грибы (плесневые- пенициллин, стрептомицин, тетрациклин), бактерии (полимиксин, грамицидин), высшие растения (фитонциды чеснока и лука), ткани животных и рыб (лизоцим, интерферон).
5. По химическому строению: бета-лактамы, гликопептиды, аминогликозиды, тетрациклины, макролиды, линкозамиды, левомицетин, рифамицины, полипептиды, полиены, разные антибиотики.
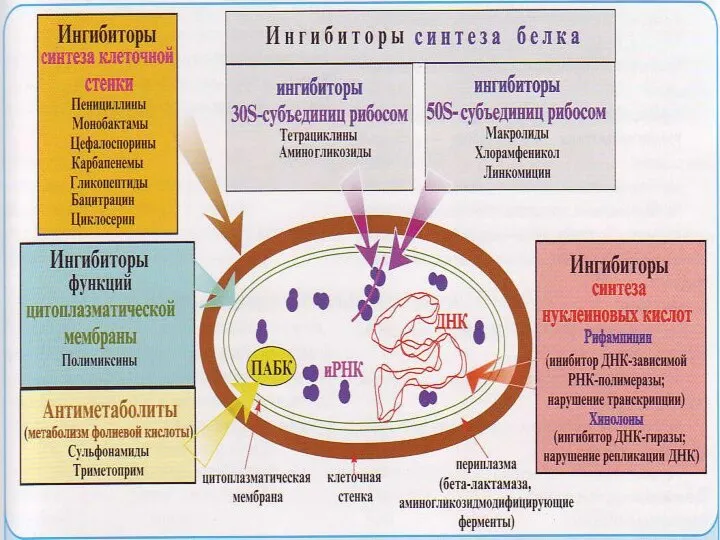
Слайд 14По химической структуре антибиотики сгруппированы в семейства (классы):
бета-лактамы (пенициллины, цефалоспорины. карбапенемы, монобактамы)
Гликопептиды
аминогликозиды
тетрациклины
макролиды

(и азалиды)
линкозамиды
левомицетин (хлорамфеникол)
рифамицины
полипептиды
полиены
разные антибиотики (фузидиевая кислота, фузафунжин и др.)
Слайд 15Бета-лактамы. Основу молекулы составляет бета-лактамное кольцо, при разрушении которого препараты теряют свою

активность; тип действия — бактерицидный. Антибиотики этой группы подразделяют на пенициллины, цефалоспорины, карбапенемы и монобактамы.
Слайд 16Пенициллины. Природный препарат— бензилпеницилин (пенициллин G) — активен против грам-положительных бактерий, однако

имеет много недостатков: быстро выводится из организма, разрушается в кислой среде желудка, инактивируется пенициллиназами — бактериальными ферментами, разрушающими бета-лактамное кольцо.
Слайд 17Полусинтетические пенициллины, полученные путем присоединения к основе природного пенициллина — 6-аминопенициллановой кислоте

— различных радикалов, имеют преимущества перед природным препаратом, в том числе широкий спектр действия:
• депo-препараты (бициллин), действует около 4 недель (создает депо в мышцах), применяется для лечения сифилиса, профилактики рецидивов ревматизма;
кислотоустойчивые (феноксиметилпенициллин), для перорального приема;
пенициллиназоустойчивые (метициллин, оксациллин), но у них довольно узкий спектр;
широкого спектра (ампициллин, амоксициллин);
антисинегнойные (карбоксипенициллины — карбенициллин, уреидопенициллины — пиперациллин, азлоциллин);
Слайд 18• комбинированные (амоксициллин + клавулановая кислота, ампициллин+сульбактам). В состав этих препаратов включены ингибиторы

ферментов — бета-лактамаз (клавулановая кислота и др.), которые тоже содержат в своей молекуле бета-лактамное кольцо; их противомикробная активность очень низка, но они легко связываются с этими ферментами, ингибируют их и таким образом защищают молекулу антибиотика от разрушения.
Слайд 19Цефалоспорины. Спектр действия широкий, но более активны в отношении грамотрицательных бактерий. По

последовательности внедрения различают 4 поколения (генерации) препаратов, которые отличаются по спектрам активности, устойчивости к бета-лактамазам и некоторым фармакологическим свойствам, поэтому препараты одного поколения не заменяют препараты другого поколения, а дополняют.
Слайд 201-е поколение (цефазолин, цефалотин и др.) — более активны в отношении грамположительных

бактерий, разрушаются бета-лактамазами;
2-е поколение (цефуроксим, цефаклор и др.) — более активны в отношении грамотрицательных бактерий, более устойчивы к бета-лактамазам;
3-е поколение (цефотаксим, цефтазидим и др.) — более активны в отношении грамотрицательных бактерий, высоко резистентны к действию бета-лактамаз;
4-е поколение (цефепим и др.) — действуют в основном на грамположительные, некоторые грамотрицательные бактерии и синегнойную палочку, резистентны к действию бета-лактамаз.
Слайд 21Карбапенемы (имипенем и др.) — из всех беталактамов имеют самый широкий спектр

действия и резистентны к бета-лактамазам.
Слайд 22Монобактамы (азтреонам и др.) — резистентны к бета-лактамазам. Спектр действия узкий (очень

активны против грамотрицательных бактерий, в том числе против синегнойной палочки).
Слайд 23ГЛИКОПЕПТИДЫ (ванкомицин и тейкопланин) — это крупные молекулы, которым трудно пройти через

поры грамотрицательных бактерий. Вследствие этого спектр действия ограничивается грамположительными бактериями. Их используют при резистентности или аллергии к бета-лактамам, при псевдомембранозном колите, вызываемом Clostridium difficile.
Слайд 24АМИНОГЛИКОЗИДЫ — соединения, в состав молекулы которых входят аминосахара. Первый препарат —

стрептомицин — был получен в 1943 г. Ваксманом как средство для лечения туберкулеза. Сейчас различают несколько поколений препаратов: (1) стрептомицин, канамицин и др., (2) гентамицин, (3) сизомицин, тобрамицин и др. Препараты бактерицидны, спектр действия — широкий (особенно активны против грамотрицательных бактерий, действуют на некоторых простейших).
Слайд 25ТЕТРАЦИКЛИНЫ — это семейство крупномолекулярных препаратов, имеющих в своем составе четыре цикличных

соединения. В настоящее время, в основном, применяют полусинтетики, например доксициклин. Тип действия — статический. Спектр действия — широкий (особенно часто используются для лечения инфекций, вызванных внутриклеточно расположенными микробами: риккетсиями, Хламидиями, Микоплазмами, бруцеллами, легионеллами).
Слайд 26МАКРОЛИДЫ (и азалиды) — это семейство больших макроциклических молекул. Эритромицин — наиболее

известный и широко используемый антибиотик. Более новые препараты: азитромицин, кларитромицин (их можно применять всего 1—2 раза в сутки). Спектр действия — широкий, включая внутриклеточные микроорганизмы, легионеллы, гемофильную палочку. Тип действия — статический (хотя, в зависимости от вида микроба, может быть и цидным).
Слайд 27ЛИНКОЗАМИДЫ (линкомицин и его хлорированный дериват — клиндамицин). Бактериостатики. Спектр их действия

похож на макролиды, клиндамицин особенно активен против анаэробов.
Слайд 28ЛЕВОМИЦЕТИН (ХЛОРАМФЕНИКОЛ) имеет в составе молекулы нитробензеновое «ядро», которое, к сожалению, делает

препарат токсичным не только в отношении бактерий, но для клеток организма человека. Статический тип действия. Спектр действия — широкий, включая внутриклеточных паразитов.
Слайд 29РИФАМИЦИНЫ (рифампицин). В основе препарата — крупная молекула со сложной структурой. Тип

действия — бактерицидный. Спектр действия — широкий (в том числе внутриклеточные паразиты; очень эффективны против микобактерий). Сейчас применяют в основном только для лечения туберкулеза.
Слайд 30ПОЛИПЕПТИДЫ (полимиксины). Спектр антимикробного действия — узкий (грамотрицательные бактерии), тип действия —

бактерицидный. Очень токсичны. Применение — наружное; в настоящее время не используются.
Слайд 31ПОЛИЕНЫ (амфотерицин В, нистатин и др.). Противогрибковые препараты, токсичность которых достаточно велика,

поэтому применяются чаще местно (нистатин), а при системных микозах препарат выбора — амфотерицин В.
Слайд 32Синтетические противомикробные химиопрепараты

Слайд 33СУЛЬФАНИЛАМИДЫ. Бактериостатики, спектр действия — широкий. Роль сульфаниламидов в лечении инфекций в

последнее время снизилась, так как существует много устойчивых штаммов, серьезны побочные эффекты и активность сульфаниламидов в целом ниже, чем у антибиотиков. Единственным препаратом этой группы, который продолжает достаточно широко использоваться в клинической практике, является ко-тримоксазол и его аналоги. Ко-тримоксазол (бактрим, бисептол) — комбинированный препарат, который состоит из сульфаметоксазола и триметоприма. Оба компонента действуют синергически, потенцируя действие друг друга. Действует бактерицидно. Триметоприм блокирует синтез фолиевой кислоты, но на уровне другого фермента. Применяют при инфекциях мочевого тракта, вызванных грамотрицательными бактериями.
Слайд 34ХИНОЛОНЫ. Первый препарат этого класса — налидиксовая кислота (1962). У нее ограниченный

спектр действия, к ней быстро развивается резистентность, применение нашла при лечении инфекций мочевыводящих путей, вызванных грамотрицательными бактериями. Преимущества фторхинолонов — разные способы введения, бактерицидное действие, хорошая переносимость, высокая активность в месте введения, хорошая проницаемость через гистогематический барьер, достаточно низкий развития резистентности. У фторхинолонов (ципрофлоксацин, норфлоксацин и др.) спектр — широкий, тип действия — цидный. Применяют при инфекциях, вызванных грамотрицательными бактериями (в том числе синегнойной палочкой), внутриклеточными паразитами, микобактериями.
Слайд 35НИТРОИМИДАЗОЛЫ (метронидазол, трихопол). Особенно активны против анаэробных бактерий, так как только эти

микробы способны активировать метронидозол путем восстановления. Тип действия — спектр — анаэробные бактерии и простейшие трихомонады, лямблии, дизентерийная амеба).
Слайд 36ИМИДАЗОЛЫ (клотримазол и др.). Противогрибковые препараты, действуют на уровне цитоплазматической мембраны.

Слайд 37НИТРОФУРАНЫ (фуразолидон и др.). Тип действия - цидный, спектр — широкий. Накапливаются

в моче в высоких концентрациях. Применяются как уросептики для лечения инфекций мочевыводящих путей.
Слайд 38Лекарственная устойчивость бактерий, пути ее преодоления. Методы определения чувствительности к антибиотикам

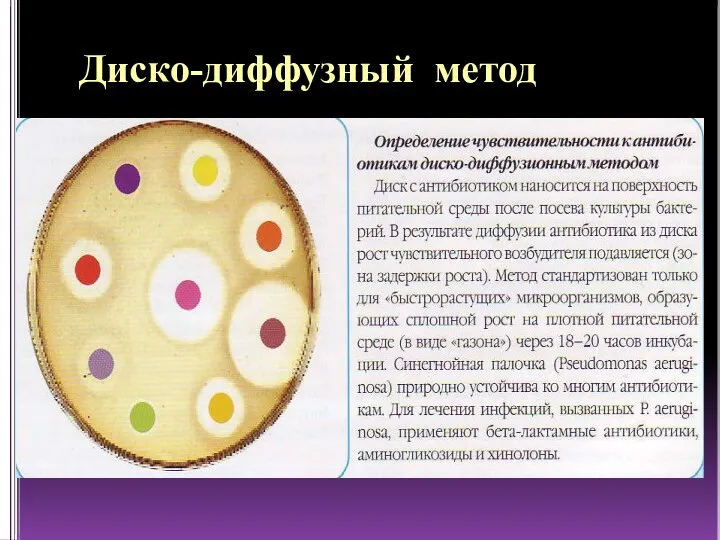
Слайд 39Чувствительность микроорганизмов к антибиотикам определяют диско-диффузным (метод диффузии в агар с применением

бумажных дисков с антибиотиками) и метод разведений антибиотиков в плотной или жидкой питательной среде. Выбор метода зависит от цели исследования и возможностей лаборатории.
Диско-диффузный метод следует рассматривать как качественный.
Методы разведения – более точные количественные способы исследования. Их применяют в особо важных практических случаях и научно-исследовательской работе.
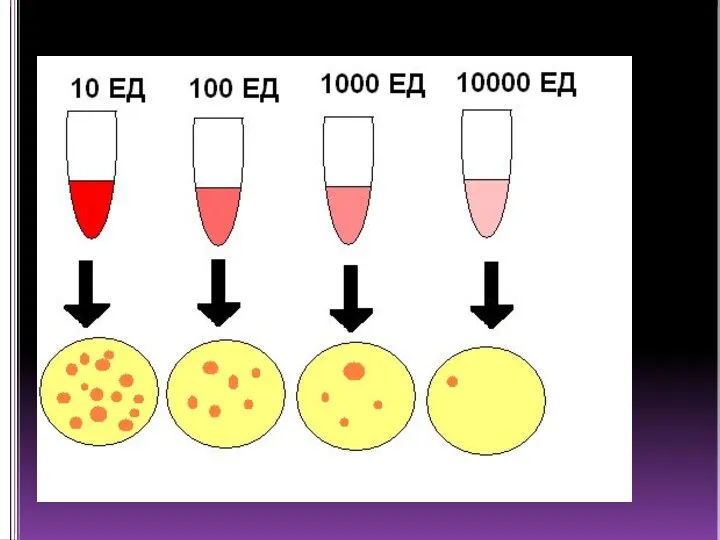
Слайд 41Метод серийных разведений
Для исследования используют мясопептонный бульон. Основные растворы антибиотиков приготавливают путем

взвешивания их порошка и растворения его в стерильной дистиллированной воде, чтобы получить определенную удобную концентрацию. Разведения антибиотиков готовят путем разбавления основного раствора антибиотика бульоном. Для этого используют 11 пробирок. В первую пробирку вносят 2 мл раствора антибиотика и переносят по 1 мл раствора антибиотика из первой пробирки в каждую последующую. Затем суточную бульонную культуру разводят до 105 – 106 микробных тел в 1 мл и вносят по 1 мл во все пробирки с разведениями антибиотика. Посевы инкубируют при 37ºС. Отмечают первую пробирку с задержкой роста микробов.
Слайд 43Ускоренные методы определения чувствительности
Ускоренное определение чувствительности микроорганизмов к антибиотикам осуществляется некоторыми зарубежными

автоматизированными системами микробиологических исследований. В кюветах панели содержатся дегидрированные субстраты или диски с антибиотиками. Каждый антибиотик в кювете представлен в одной концентрации, соответствующей критерию принадлежности бактерий к группе «чувствительных» к антибиотику. Одновременно тестируется 20 и более антибиотиков. После внесения взвеси испытуемых бактерий посевы инкубируют при 35-37ºС в течение 4 - 5 часов. Результаты регистрируют спектрофотометрически или кондуктометрически сразу при появлении размножения бактерий в контроле без антибиотиков.














































 Барьерная контрацепция (колпачки,диафрагмы, инпланоны)
Барьерная контрацепция (колпачки,диафрагмы, инпланоны) Средства индивидуальной защиты органов дыхания
Средства индивидуальной защиты органов дыхания Breast Massager
Breast Massager Дезинфекция медицинского оборудования
Дезинфекция медицинского оборудования Організація амбулаторної і стаціонарної допомоги міському і сільському населенню
Організація амбулаторної і стаціонарної допомоги міському і сільському населенню Wilhelm Conrad Röntgen (27.03.1845 – 10.02.1923)
Wilhelm Conrad Röntgen (27.03.1845 – 10.02.1923) Хирургический шов
Хирургический шов Онлайн курс Преображение. Привычки, влияющие на красоту и молодость: питание, водный баланс, сон
Онлайн курс Преображение. Привычки, влияющие на красоту и молодость: питание, водный баланс, сон Тест. Зачет 1-6
Тест. Зачет 1-6 Первая неотложная помощь при экстренных состояниях
Первая неотложная помощь при экстренных состояниях Оценки и опыт представителей науки, бизнеса и государственных организаций
Оценки и опыт представителей науки, бизнеса и государственных организаций Биохимический анализ крови
Биохимический анализ крови Термометрия. Виды термометров
Термометрия. Виды термометров Ветеринарная вирусология
Ветеринарная вирусология Осторожно гепатит!
Осторожно гепатит! Пациент с мигрирующей полиартралгией
Пациент с мигрирующей полиартралгией Повреждение ротаторной манжеты
Повреждение ротаторной манжеты Алгоритм лабораторной диагностики сифилиса
Алгоритм лабораторной диагностики сифилиса גישה למטופלת צעירה עם שלפוחית שתן רגיזה
גישה למטופלת צעירה עם שלפוחית שתן רגיזה Health problems. Accidents and injuries
Health problems. Accidents and injuries Факторы, определяющие состояние здоровья населения. (Лекция 3)
Факторы, определяющие состояние здоровья населения. (Лекция 3) Детская неврология
Детская неврология Гепатит А
Гепатит А Первая помощь при укусе змеи и насекомых
Первая помощь при укусе змеи и насекомых Подчелюстной лимфаденит
Подчелюстной лимфаденит Medcraft. Medznat online conference
Medcraft. Medznat online conference Острый коронарный синдром
Острый коронарный синдром Правила проведения сердечно-легочной реанимации
Правила проведения сердечно-легочной реанимации