Содержание
- 2. Вопросы: 1. О каком веществе идет речь? 2. Что вы можете сказать о его агрегатном состоянии?
- 3. НАЙДИТЕ СХОДСТВА В ПРЕДЛОЖЕННЫХ ФОРМУЛАХ K2O, MgO, Al2O3, SO3, SO2, N2O5, FeO, Fe2O3.
- 4. Ответ : Сложные вещества; Состоят из двух элементов; Один из которых кислород.
- 5. Кроссворд 1. Назовите самый распространенный химический элемент в земной коре. 2. Как называется вещество, которое ускоряет
- 6. ТЕМА УРОКА: ОКСИДЫ – СОЕДИНЕНИЯ ЭЛЕМЕНТОВ С КИСЛОРОДОМ
- 7. Выберите из предложенных формул формулы оксидов. Запишите их в тетради в столбик H2S, Na2O, Li2SO4, B2O3,
- 8. Схема: Название оксида = «Оксид» + название элемента в родительном падеже + (валентность элемента, если она
- 9. Проверяем: Na2O – оксид натрия B2O3 – оксид бора P2O3 – оксид фосфора (III) ZnO –
- 10. Найди ошибку в названии вещества CuO – оксид меди CaO – оксид кальция CO – оксид
- 11. Лабораторный опыт: 1. Рассмотрите выданные вам оксиды. Обратите внимание на: агрегатное состояние; цвет; запах. 2. Исследуйте
- 12. Выводы: 1. Оксиды могут быть твёрдыми, жидкими, газообразными веществами. 2. Могут быть бесцветными и окрашенными. 3.
- 13. Оксиды в природе SiO2 - кварцевый песок, кремнезём. Горный хрусталь Кварцевый песок Аметист Агат Яшма
- 14. Оксиды в природе: Al2O3 2SiO2 2H2O – белая глина, состоит из оксидов алюминия и кремния
- 15. Оксиды в природе: Fe2O3 – руда железная (красный железняк) Fe3O4 или FeO Fe2O3 – магнитный железняк
- 16. Оксиды в природе: CO2 – углекислый газ
- 17. Оксиды в природе: ? Самый распространенный на земле оксид, даже организм человека на 65 % состоит
- 18. Антуан Лоран Лавуазье Французский химик ( 1743 - 1794)
- 19. Составьте формулы оксидов и дайте им названия: Ca, C(IV), Al, Mg, N(III), Fe(II), Cu(I), S(IV). Если
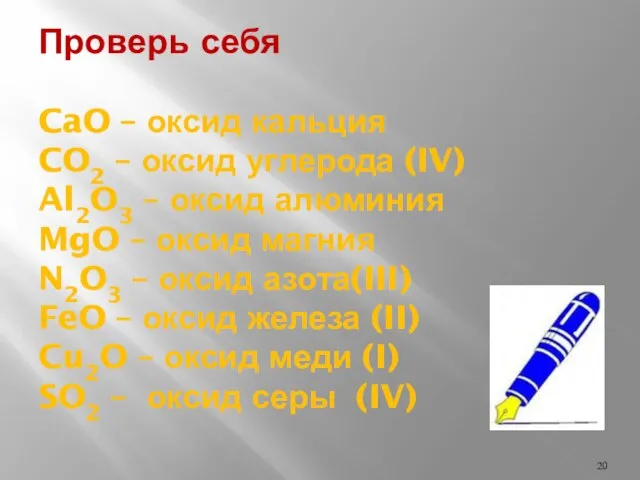
- 20. Проверь себя CaO – оксид кальция CO2 – оксид углерода (IV) Al2O3 – оксид алюминия MgO
- 21. Составьте уравнения реакций получение оксидов магния, алюминия, лития
- 22. Проверь себя 2Mg + O2 = 2 MgO 4 Al + 3O2 = 2 Al2O3 4
- 23. Дополни уравнения химических реакций Вариант I ? + O2→ P2 O5 C + O2 → ?
- 24. Проверь себя: Вариант I 4Р + 5O2→ 2P2 O5 C + O2 → СО2 2Fe +
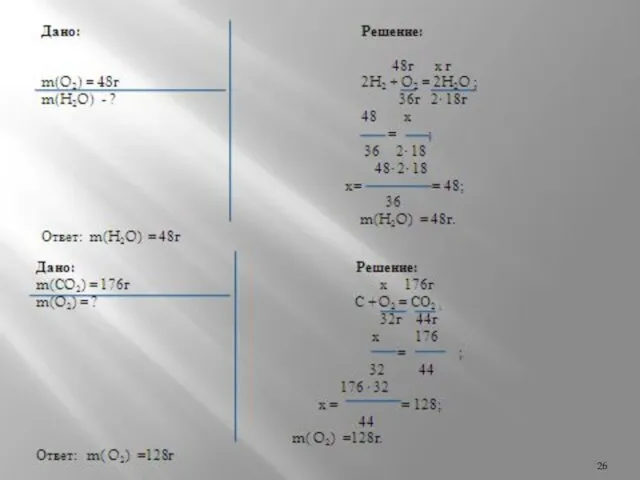
- 25. Реши задачу Вариант I Рассчитайте массу воды, которая образуется при взаимодействии водорода с кислородом, массой 48
- 27. ДОМАШНЕЕ ЗАДАНИЕ: § 23, стр. 104 номера 2, 4, 6, 8.
- 29. Скачать презентацию























 Урок русского языка Словарная работа. 2 класс. Автор Чиркова Т.Ф. МОУ СОШ Сп. «Село Софийск» 2008 г.
Урок русского языка Словарная работа. 2 класс. Автор Чиркова Т.Ф. МОУ СОШ Сп. «Село Софийск» 2008 г. Учимся готовить детей к ЕГЭ
Учимся готовить детей к ЕГЭ Презентация на тему Биография Тютчева
Презентация на тему Биография Тютчева Фонари на улицах и в парках
Фонари на улицах и в парках Культура Древнего Рима эпохи Октавиана Августа
Культура Древнего Рима эпохи Октавиана Августа  My future carees is a Lawyer
My future carees is a Lawyer Современные информационные технологии в образовании
Современные информационные технологии в образовании Мужской костюм
Мужской костюм КВАДРОЦИКЛЫ И КВАДРОЦИКЛЫ С ПОСАДКОЙ «БОК О БОК» CAN-AM 2013 г. в. Ванкувер/25-26 мая 2012 г.
КВАДРОЦИКЛЫ И КВАДРОЦИКЛЫ С ПОСАДКОЙ «БОК О БОК» CAN-AM 2013 г. в. Ванкувер/25-26 мая 2012 г. Алексей Константинович Толстой
Алексей Константинович Толстой Урок русского языка во 2 классе
Урок русского языка во 2 классе Обеспечение доступности и качества образования для всех учащихся
Обеспечение доступности и качества образования для всех учащихся Закон Архимеда
Закон Архимеда Проект: формирование издательским сообществом отраслевой организационно-правовой системы управления рынком продаж периодики
Проект: формирование издательским сообществом отраслевой организационно-правовой системы управления рынком продаж периодики Сталинградская битва
Сталинградская битва Дорожные знаки
Дорожные знаки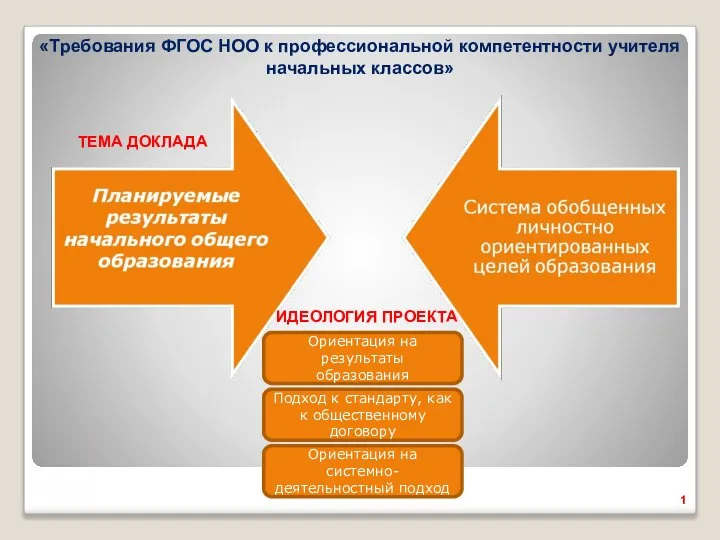 Планируемые результаты начального общего образования
Планируемые результаты начального общего образования Общение с клиентом
Общение с клиентом Презентация_компании_САМАРАСПЕКТР
Презентация_компании_САМАРАСПЕКТР О результатах служебной деятельности Сарапульского МРО ЛРР Управления за 1 квартал 2021 года
О результатах служебной деятельности Сарапульского МРО ЛРР Управления за 1 квартал 2021 года Сон. Значение сна как метода релаксации
Сон. Значение сна как метода релаксации Презентация на тему Изготовление розы из салфетки
Презентация на тему Изготовление розы из салфетки РОЛЬ СМИ В РАЗВИТИЯ ГРАЖДАНСКОГО ОБЩЕСТВА В КИРОВСКОЙ ОБЛАСТИ ЭКСПЕРТНОЕ ИССЛЕДОВАНИЕ(краткий обзор)
РОЛЬ СМИ В РАЗВИТИЯ ГРАЖДАНСКОГО ОБЩЕСТВА В КИРОВСКОЙ ОБЛАСТИ ЭКСПЕРТНОЕ ИССЛЕДОВАНИЕ(краткий обзор) Презентация на тему таблица умножения
Презентация на тему таблица умножения  Мониторинг власти
Мониторинг власти Проблемы безопасности литий-ионных аккумуляторов И.А. Профатилова, В.А. Тарнопольский Департамент развития, Группа компаний “Рус
Проблемы безопасности литий-ионных аккумуляторов И.А. Профатилова, В.А. Тарнопольский Департамент развития, Группа компаний “Рус Технология проведения тренировочных занятий по видам спорта в дистанционном формате
Технология проведения тренировочных занятий по видам спорта в дистанционном формате Раздел 9. Система оценки достижения планируемых результатов освоения ООП начального общего образования _____________________________ Оцениван
Раздел 9. Система оценки достижения планируемых результатов освоения ООП начального общего образования _____________________________ Оцениван