Содержание
- 2. Адсорбция – самопроизвольное изменение концентрации вещества на границе раздела фаз.
- 3. Медико-биологическое значение темы: 1. Усвоение питательных и лекарственных веществ 2. Перенос О2 и СО2 из лёгких
- 4. Основные понятия Сорбент – поглотитель Сорбтив (сорбат) – поглощаемое вещество Сорбция – процесс поглощения одного вещества
- 5. Поверхностное натяжение Поверхностное натяжение (σ) равно работе, которую нужно совершить для создания единицы поверхности [Дж/м2]. Поверхностное
- 6. Поверхностная активность Способность растворенного вещества изменять поверхностное натяжение – поверхностная активность (g) Мера поверхностной активности:
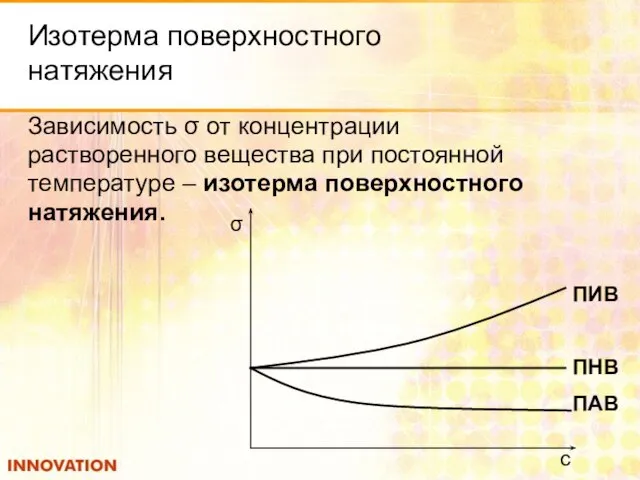
- 7. ПАВ, ПИВ, ПНВ Поверхностно-активные вещества (ПАВ): уменьшают σ растворителя. σ раствора О. ПАВ: спирты, органические кислоты,
- 8. Изотерма поверхностного натяжения Зависимость σ от концентрации растворенного вещества при постоянной температуре – изотерма поверхностного натяжения.
- 9. Строение молекулы ПАВ: Молекула ПАВ состоит из: неполярной гидрофобной углеводородной группы (“хвост”) полярной гидрофильной группы (“голова”):
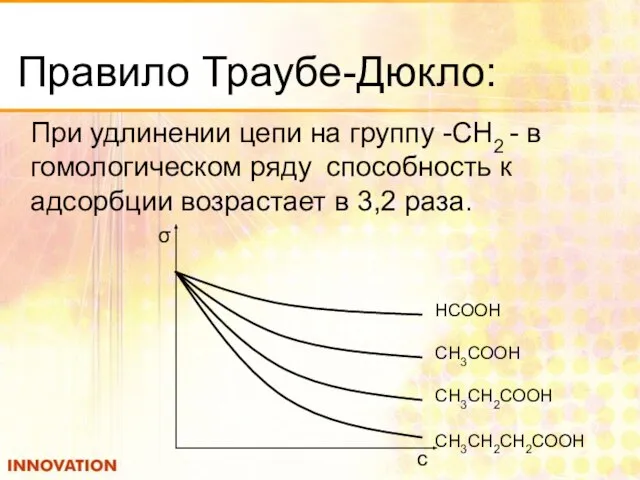
- 10. Правило Траубе-Дюкло: При удлинении цепи на группу -СН2 - в гомологическом ряду способность к адсорбции возрастает
- 11. Уравнение Гиббса >0 Г С вещества в поверхностном слое 0, т.е. ↑с ↓σ (ПАВ) С вещества
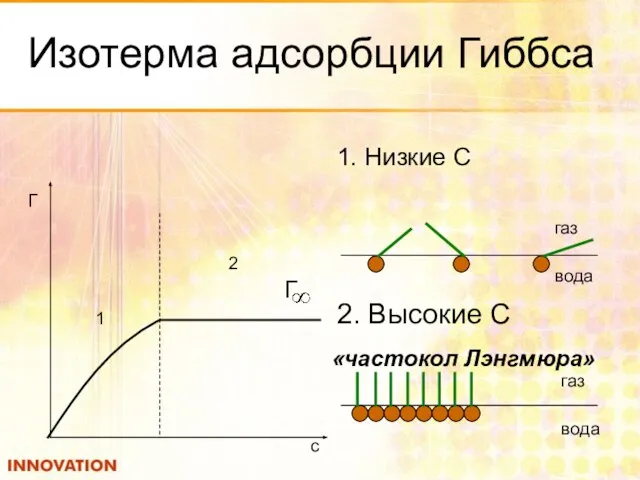
- 12. Изотерма адсорбции Гиббса 1. Низкие С 1 2 Г c газ вода 2. Высокие С газ
- 13. Адсорбция твердыми телами Величина адсорбции зависит от: Размера поверхности адсорбента чем > Sповерхности, тем > адсорбция.
- 14. Уравнение Фрейндлиха Г = x/m = КФ · Cn х – количество вещества адсорбтива (моль) m
- 15. Уравнение Ленгмюра Г = Г С для газов: Г = Г _Р_ К+С К+Р С –
- 16. Правило Панета-Фаянса Из раствора адсорбируются те ионы, которые входят в состав кристаллической решетки сорбента или образуют
- 17. Ионообменная адсорбция Ионообменная адсорбция – процесс, в котором адсорбент и раствор обмениваются между собой в эквивалентных
- 18. Хроматография Хроматография - динамический метод анализа, основанный на многократно повторяющихся процессах сорбции и десорбции.
- 19. ВЭЖХ Agilent Technologies
- 20. ВЭЖХ Милихром
- 21. ВЭЖХ HP
- 22. ВЭЖХ Люмекс
- 23. ВЭЖХ Чешский прибор
- 24. ГЖХ
- 25. ГЖХ “Agilent Technologies”
- 26. ГЖХ “Кристалл”
- 27. ГЖХ “Хромос”
- 28. ХМС НР
- 30. Скачать презентацию
























 Национальная принадлежность (5 класс)
Национальная принадлежность (5 класс) Культурные практики ребенка
Культурные практики ребенка Текстильные товары
Текстильные товары Изготовление объёмной обрывной аппликации из деталей непрямоугольной формы с использованием компьютера
Изготовление объёмной обрывной аппликации из деталей непрямоугольной формы с использованием компьютера Основные структурные компоненты системы социального образования
Основные структурные компоненты системы социального образования Деятельностный подход в обучении учащихся с ОВЗ музыке
Деятельностный подход в обучении учащихся с ОВЗ музыке Политическая система общества. Лекция 10
Политическая система общества. Лекция 10 Системный анализ в профессиональной деятельности 1 раздел
Системный анализ в профессиональной деятельности 1 раздел Татарский национальный костюм
Татарский национальный костюм Значения жестов в разных странах мира
Значения жестов в разных странах мира Паруса вдохновения Литературный альманах гимназии №1 г. Новогрудка 2012 г. Выпуск 1 Для выхода щелкните правой клавишей мышки
Паруса вдохновения Литературный альманах гимназии №1 г. Новогрудка 2012 г. Выпуск 1 Для выхода щелкните правой клавишей мышки Выступление Стрижкова А.Е. на родительском собрании лечебного факультета 29 октября 2011 года
Выступление Стрижкова А.Е. на родительском собрании лечебного факультета 29 октября 2011 года Мы даем тебе крылья!
Мы даем тебе крылья! КОМПЛЕКС СРЕДСТВ ЗАЩИТЫ ИНФОРМАЦИИ НА БАЗЕ РАЗРАБОТКИ ВОЛГОГРАДСКОГО ГОСУДАРСТВЕННОГО ТЕХНИЧЕСКОГО УНИВЕРСИТЕТА
КОМПЛЕКС СРЕДСТВ ЗАЩИТЫ ИНФОРМАЦИИ НА БАЗЕ РАЗРАБОТКИ ВОЛГОГРАДСКОГО ГОСУДАРСТВЕННОГО ТЕХНИЧЕСКОГО УНИВЕРСИТЕТА «Самые дорогие для нас слова: мама, Родина, мир, труд»
«Самые дорогие для нас слова: мама, Родина, мир, труд» Путешествие в прошлое и будущее вместе с Тур-Экс…
Путешествие в прошлое и будущее вместе с Тур-Экс… Словарные слова
Словарные слова Тюбетейка
Тюбетейка Организация Объединённых Наций по промышленному развитию (ЮНИДО)
Организация Объединённых Наций по промышленному развитию (ЮНИДО) Профильное обучение как фактор личностного развития учащегося
Профильное обучение как фактор личностного развития учащегося Вредные привычки. Их влияние на здоровье человека.
Вредные привычки. Их влияние на здоровье человека. Латинская Америка. Банановые республики
Латинская Америка. Банановые республики Свойства параллелепипеда
Свойства параллелепипеда «Аэроджип» Малый катер на воздушной подушке
«Аэроджип» Малый катер на воздушной подушке Математика(Школа 2100)4 класс
Математика(Школа 2100)4 класс Кинетическая Энергия
Кинетическая Энергия Светочи Земли Русской
Светочи Земли Русской Орфографические и синтаксические задачи
Орфографические и синтаксические задачи