Содержание
- 2. Результаты ЕГЭ 2010 Граница минимального балла -33 тестовых балла (12 первичных баллов) Уровни оценивания: неудовлетворительный –
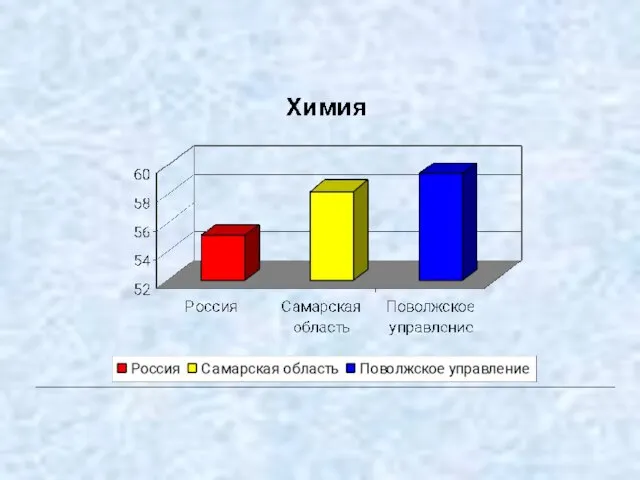
- 3. Самарская область Число учащихся - 1077 человек Средний балл -58,2 100 баллов – 8 учащихся 24
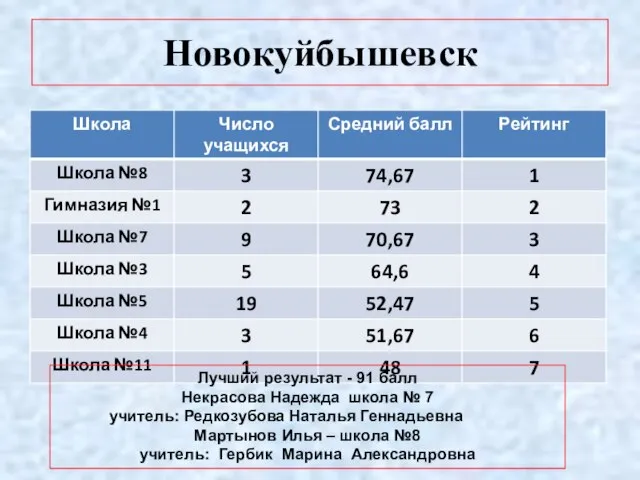
- 4. Новокуйбышевск Лучший результат - 91 балл Некрасова Надежда школа № 7 учитель: Редкозубова Наталья Геннадьевна Мартынов
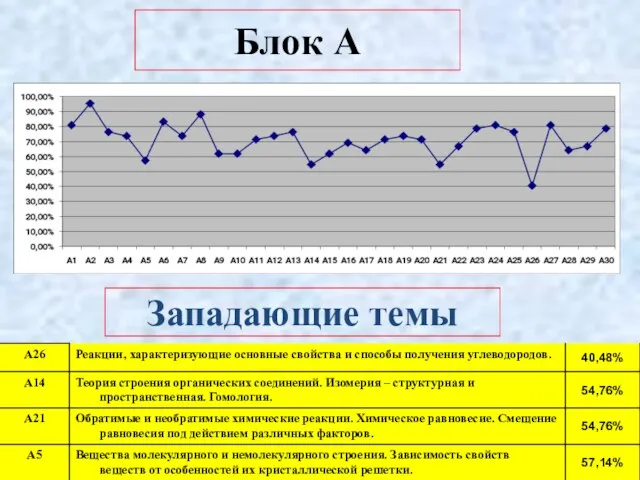
- 5. Блок А Западающие темы
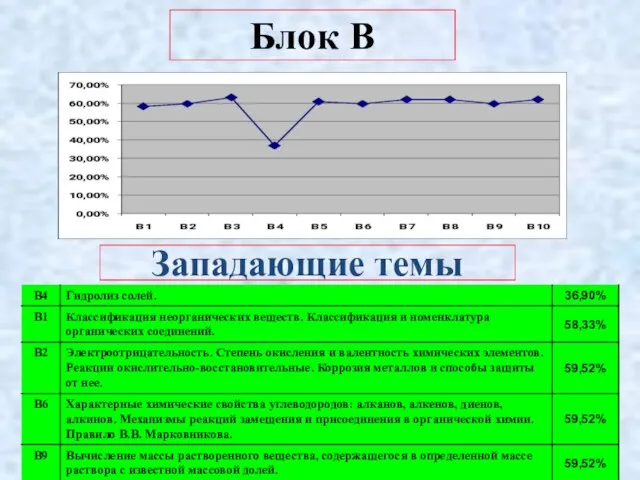
- 6. Блок В Западающие темы
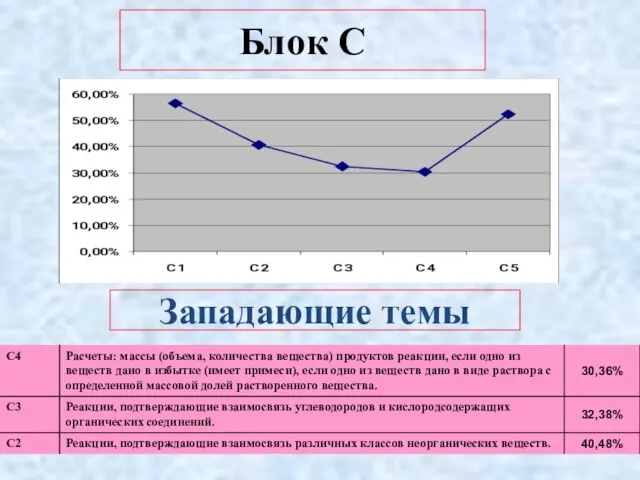
- 7. Блок С Западающие темы
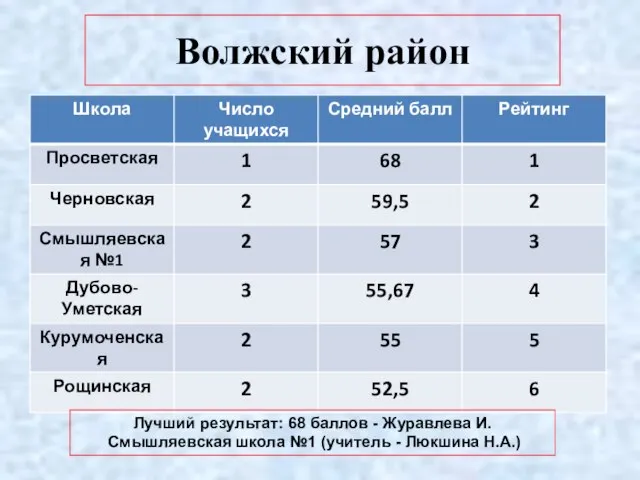
- 8. Волжский район Лучший результат: 68 баллов - Журавлева И. Смышляевская школа №1 (учитель - Люкшина Н.А.)
- 9. Блок А Западающие темы
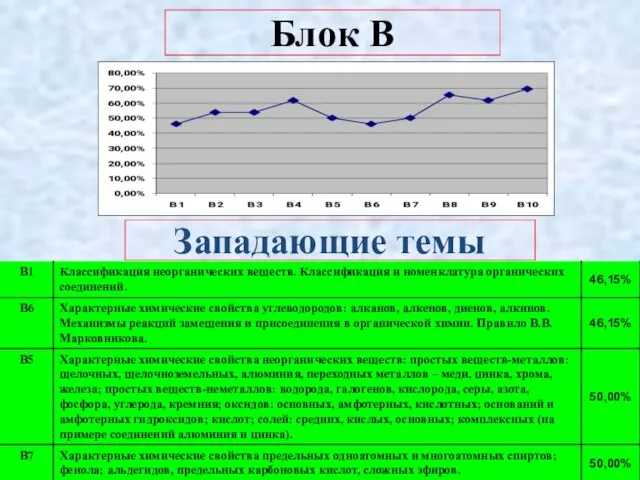
- 10. Блок В Западающие темы
- 11. Блок С Западающие темы
- 13. Западающие темы
- 14. Химическая связь (А 4) Ошибки: полярность связи; понятие о типах связи в органических веществах
- 15. Степень окисления (А 4, В 2) Ошибки: определение степени окисления в 4-х элементных соединениях; не учитывался
- 16. Кристаллические решетки (А 5) Ионную кристаллическую решетку имеет: 1)Хлор 2)хлорид цезия 3)хлорид фосфора (III) 4)оксид углерода
- 17. Свойства простых веществ и неорганических соединений (А 9) Ошибки: не используют ряд активности металлов; свойства амфотерных
- 18. Химические свойства неорганических веществ (А 12) Химическая реакция возможна между Zn и CuCl2 2) Fe и
- 19. Изомерия органических соединений (А 14) Изомером 2-метилпропанола-1 является 1)метилизопропиловый эфир 2) пропанол-1 3) 2-метилбутанол-1 4)пропандиол-1,2 Ошибки:
- 20. Химическое равновесие (А 21) Ошибки: незнание влияния концентрации реагирующих веществ на смещение равновесия
- 21. Общие химические свойства органических веществ (А 26) С бромной водой взаимодействует каждое из двух веществ: 1)этилен
- 22. Химические свойства органических веществ (А27) Альдегид получается при гидратации 1)этина 2) пропина 3) бутина-1 4) пентина-1
- 23. Свойства амфотерных гидроксидов (В 3) Ошибки: определение продуктов взаимодействия амфотерных гидроксидов со щелочами при сплавлении и
- 24. Гидролиз (В4) Ошибки: неправильное определение силы кислот и оснований как электролитов
- 25. Свойства угловодородов (В 6) Ошибки: не знают реакции альдегида со спиртами Ошибки: не знают отношение амина
- 26. Свойства кислородсодержащих органических веществ (В 7) В отличие от фенола метанол 1)взаимодействует с растворами щелочей 2)вступает
- 27. Свойства неорганических веществ (С 2) Даны вещества: йод, азотная кислота (конц.), сероводород и кислород. Написать 4
- 28. Комбинированная задача(С4) Ошибки: определение избытка вещества и расчет общей массы раствора с исключением выделившегося газа
- 30. Скачать презентацию




















 Международная торговля услугами
Международная торговля услугами  Техника бега на средние дистанции
Техника бега на средние дистанции
 Э́двард Мунк
Э́двард Мунк «Развитие ипотечного кредитования в регионах РФ, практика и особенности» Директор Департамента кредитных операций ЗАО «Банк Жил
«Развитие ипотечного кредитования в регионах РФ, практика и особенности» Директор Департамента кредитных операций ЗАО «Банк Жил Презентация на тему Стратегия Казахстан - 2050
Презентация на тему Стратегия Казахстан - 2050  «Жить – значит иметь проблемы, решать проблемы – значит растиинтеллектуально».Д.П. Гуплдфорд, психолог`
«Жить – значит иметь проблемы, решать проблемы – значит растиинтеллектуально».Д.П. Гуплдфорд, психолог` В гонках участвуют черепахи.
В гонках участвуют черепахи. Имя прилагательноеОчень занимательное.Его вопросы чей? Какой?Запомнит ученик любой.Оно обозначаетПризнаки предметов.И без сущ
Имя прилагательноеОчень занимательное.Его вопросы чей? Какой?Запомнит ученик любой.Оно обозначаетПризнаки предметов.И без сущ Живопись в формировании эстетического взгляда на жизнь
Живопись в формировании эстетического взгляда на жизнь Enjoy English
Enjoy English Что такое экономика?
Что такое экономика? Военно-промышленный завод Fighting robots
Военно-промышленный завод Fighting robots  Суперконденсаторы для гибридного и электро-транспорта Мурышев Андрей Евгеньевич Проектный директор Наноцентра «Дубна»
Суперконденсаторы для гибридного и электро-транспорта Мурышев Андрей Евгеньевич Проектный директор Наноцентра «Дубна» Использование информационных компьютерных технологий в специальном (коррекционном) образовании
Использование информационных компьютерных технологий в специальном (коррекционном) образовании 1 1 Контекстная реклама для Авто: Авто-дилеры, авто-бренды, авто-СМИ. Наумов Алексей, ЗАО «Бегун»
1 1 Контекстная реклама для Авто: Авто-дилеры, авто-бренды, авто-СМИ. Наумов Алексей, ЗАО «Бегун» Игра «Кто хочет стать историком»
Игра «Кто хочет стать историком» Макетирование и поиск идей для позиционирования бренда Саровский кирпичный завод
Макетирование и поиск идей для позиционирования бренда Саровский кирпичный завод День рождения нашей крошки
День рождения нашей крошки Инфраструктура в борьбе за внедрение ЭДОИЛИ «Кому нужны системы ЭДО»
Инфраструктура в борьбе за внедрение ЭДОИЛИ «Кому нужны системы ЭДО» Напольная ваза «Фантазия»
Напольная ваза «Фантазия» Презентация на тему Свежие плоды
Презентация на тему Свежие плоды ИСПАНИЯ
ИСПАНИЯ Институты и субинституты финансового права
Институты и субинституты финансового права Теория фильтров А. Керкгоффа и К. Дэвиса
Теория фильтров А. Керкгоффа и К. Дэвиса Буквы О и Е после шипящих и Ц в суффиксах и окончаниях имен существительных
Буквы О и Е после шипящих и Ц в суффиксах и окончаниях имен существительных Физическая культура в жизни человека и общества
Физическая культура в жизни человека и общества Образ Александра Невского в искусстве
Образ Александра Невского в искусстве