Содержание
- 2. Безопасность лекарств Лекарства могут предотвращать и лечить заболевания , они также могут смягчать страдания от заболеваний
- 3. Что такое Фармаконадзор (Pharmacovigilance)? Определение ВОЗ: Научная и иная деятельность, связанная с выявлением, оценкой, пониманием и
- 4. Pharmaco - Vigilance Pharmaco = лекарство Vigilare = наблюдать; надзирать; быть начеку
- 5. Какова цель фармаконадзора? Улучшить заботу о пациенте в отношении безопасности применения лекарств, и всех лекарственных и
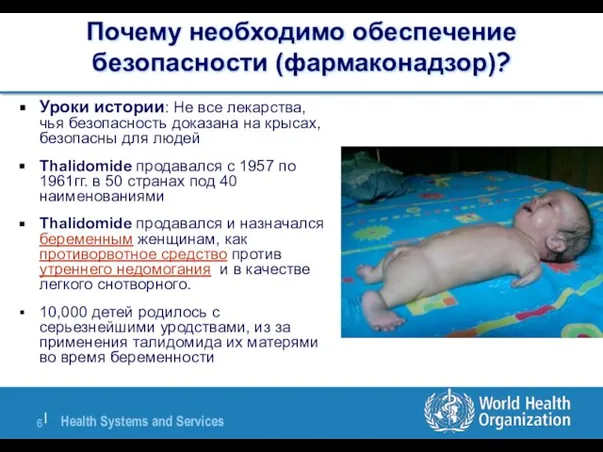
- 6. Почему необходимо обеспечение безопасности (фармаконадзор)? Уроки истории: Не все лекарства, чья безопасность доказана на крысах, безопасны
- 7. Почему необходим фармаконадзор? Озабоченность безопасностью пациентов – Недостаточные доказательства безопасности в результате клинических исследований Эксперименты на
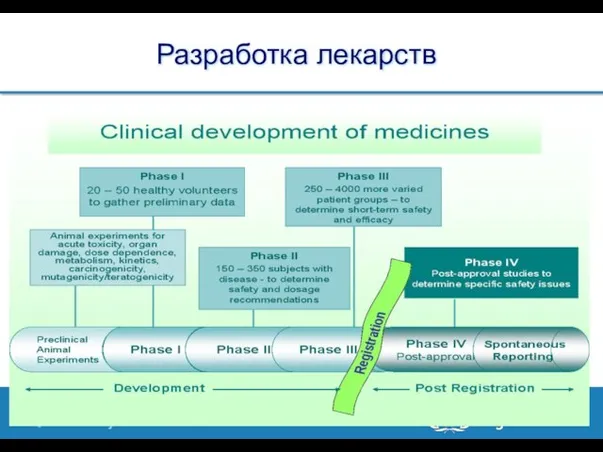
- 8. Разработка лекарств
- 9. Ограничения фаз 1 - 3 клинических исследований Ограниченный размер выборки: не более 5000, а чаще не
- 10. Примеры изъятия продуктов с рынка из соображений безопасности Лекарство Год Thalidomide 1965 Practolol 1975 Clioquinol 1970
- 11. Примеры из научной литературы Великобритания: США: Побочные действия лекарств были причиной каждой 4-6ой смерти в США
- 12. 125 пациентов 24 пациента испытывали побочные действия лекарств (19%) 59% были предотвращаемыми
- 13. 6.5% госпитализаций из за побочных эффектов лекарств Семь 800-кречных больниц заняты пациентами с побочными реакциями £446
- 14. Затраты связанные с предотвращаемыми проблемами, связанными с применением лекарств США Затраты на пациента в год $84-$128
- 15. Безопасность лекарств: разделенная ответственность Производители Регуляторы Работники здравоохранения Врачи Фармацевты медсестры Пациенты
- 16. Программа ВОЗ по международному мониторингу лекарств Thalidomide disaster consequence in 1960ies An international system for monitoring
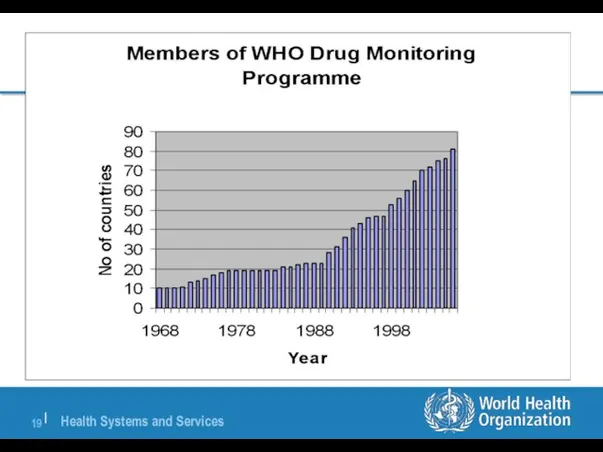
- 17. От первоначальных 10 до почти 100 стран членов участвуют в Программе ВОЗ по международному мониторингу лекарств
- 18. http://www.who-umc.org/DynPage.aspx
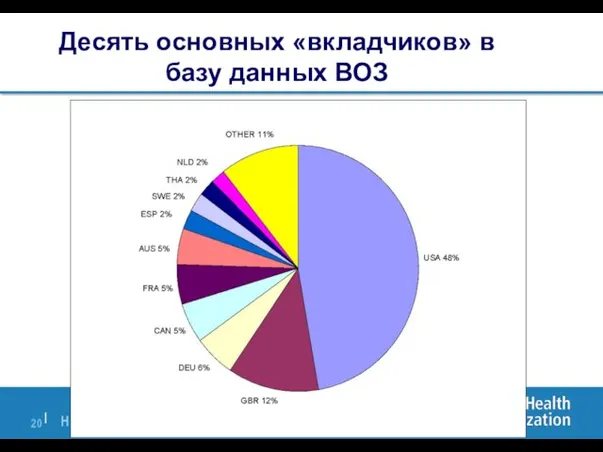
- 20. Десять основных «вкладчиков» в базу данных ВОЗ
- 21. Деятельность ВОЗ в области безопасности лекарств Политика и руководства Обмен информацией Экспертная поддержка стран Сотрудничество CIOMS
- 23. Обмен информацией WHO Pharmaceuticals Newsletter http://www.who.int/medicines/publications/newsletter/en/index.html WHO Drug Alerts WHO Drug Information http://www.who.int/druginformation/ WHO Restricted Pharmaceuticals
- 24. Экспертная поддержка стран Профессиональное руководство по различным аспектам фармаконадзора Специальные проекты Обучение по вопросам фармаконадзора Региональные
- 25. Безопасность лекарств- общая ответственность Спонтанную отчетность необходимо усилить: у многих стран есть потенциал (Бразилия, Китай и
- 27. Скачать презентацию



















 УРОКАлгебра 8 класс
УРОКАлгебра 8 класс Русский драматический театр
Русский драматический театр Аудитория Autonet.ru Москва, Март 2008
Аудитория Autonet.ru Москва, Март 2008 Искусство и костюм стиля МОДЕРН
Искусство и костюм стиля МОДЕРН Тема урока: Моделирование одежды. Профессия художника – модельера Цель урока: 1. Обобщить знания о приемах моделирования 2. Науч
Тема урока: Моделирование одежды. Профессия художника – модельера Цель урока: 1. Обобщить знания о приемах моделирования 2. Науч ПРАВОВАЯ ОТВЕТСТВЕННОСТЬ МОЛОДЕЖИ
ПРАВОВАЯ ОТВЕТСТВЕННОСТЬ МОЛОДЕЖИ Мастер - класс Вышивка крестом
Мастер - класс Вышивка крестом МАСЛЯНЫЕ РАДИАТОЫ NEOCLIMA 2011
МАСЛЯНЫЕ РАДИАТОЫ NEOCLIMA 2011 Презентация на тему Панда
Презентация на тему Панда Дэнас-вертебра. Принципиально новый способ стимуляции по типу бегущая волна
Дэнас-вертебра. Принципиально новый способ стимуляции по типу бегущая волна Темперамент и характер
Темперамент и характер Что и какие события могут по праву считаться всемирным наследием
Что и какие события могут по праву считаться всемирным наследием Грамматический чай
Грамматический чай primer_prezentatsii_PP_01_SV-97_2022
primer_prezentatsii_PP_01_SV-97_2022 Весна в картинах известных художников
Весна в картинах известных художников Психомоторное развитие детей. Семиотика нарушений психомоторного развития детей
Психомоторное развитие детей. Семиотика нарушений психомоторного развития детей Выбор одежды и поза ведущего во время тренинга
Выбор одежды и поза ведущего во время тренинга Классификация фотоаппаратов
Классификация фотоаппаратов В течение многих лет ученые, строители и производители искали универсальный строительный материал, имеющий необходимую прочность
В течение многих лет ученые, строители и производители искали универсальный строительный материал, имеющий необходимую прочность Презентация на тему Сельское хозяйство развитых и развивающихся стран (10 класс)
Презентация на тему Сельское хозяйство развитых и развивающихся стран (10 класс)  Модель построения предметно-развивающей среды в рамках проектной деятельности
Модель построения предметно-развивающей среды в рамках проектной деятельности Технология и аппаратура флотации. Применение флотации в производстве кормовых дрожжей
Технология и аппаратура флотации. Применение флотации в производстве кормовых дрожжей Анализ представленных субъектами Российской Федерации отчетов о достижении показателей результативности реализации субсидий
Анализ представленных субъектами Российской Федерации отчетов о достижении показателей результативности реализации субсидий Стартап. Поиск мечты
Стартап. Поиск мечты Презентация НИР (Шаблон) (2)
Презентация НИР (Шаблон) (2)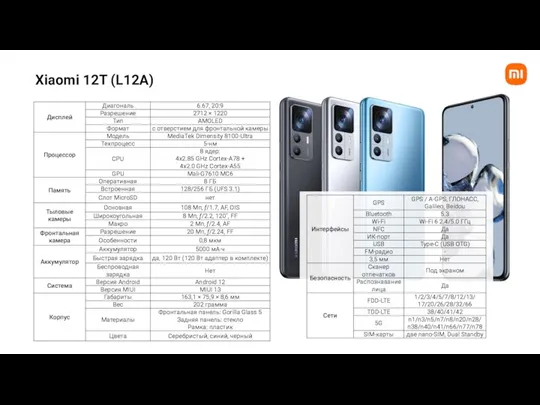 Xiaomi 12T (L12A) specs and KSP (1)[669]
Xiaomi 12T (L12A) specs and KSP (1)[669] Чего ты хочешь…^3^
Чего ты хочешь…^3^ К вопросу агентивности. Эволюция Ориентированного на Решение подхода
К вопросу агентивности. Эволюция Ориентированного на Решение подхода