Содержание
- 2. International Journal of Stroke Vol 4, October 2009, 406–412 CASTA: Методология
- 3. Цель исследования: Оценка безопасности и клинической эффективности 10-ти дневного курса терапии Церебролизином, вводимого на фоне базовой
- 4. Основные критерии эффективности Модифицированная шкала Ренкина (мшР) , индекс Бартел (ИБ), Шкала инсульта Национального Института Здоровья
- 5. Возраст от 18 до 85 лет Очаговый неврологический дефицит Клинический диагноз: острый полушарный ишемический инсульт Результаты
- 6. Данные КТ/МРТ в пользу острого или хронического внутримозгового кровоизлияния, САК, АВМ, мозговая аневризма или опухоли Признаки
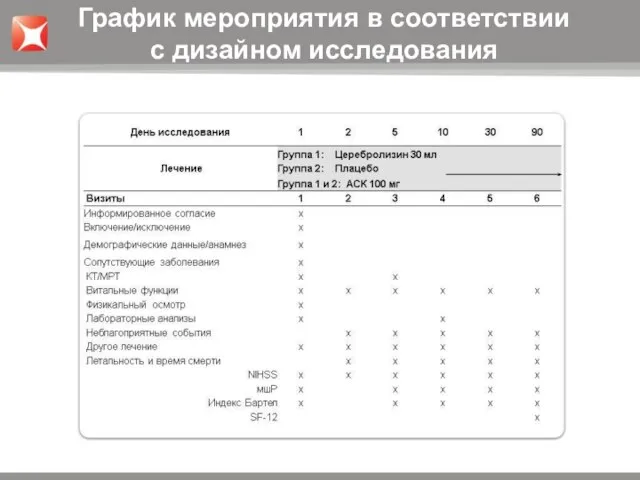
- 7. График мероприятия в соответствии с дизайном исследования
- 8. 52 центра в Азии CASTA: предварительные результаты Распределение пациентов в группах сравнения
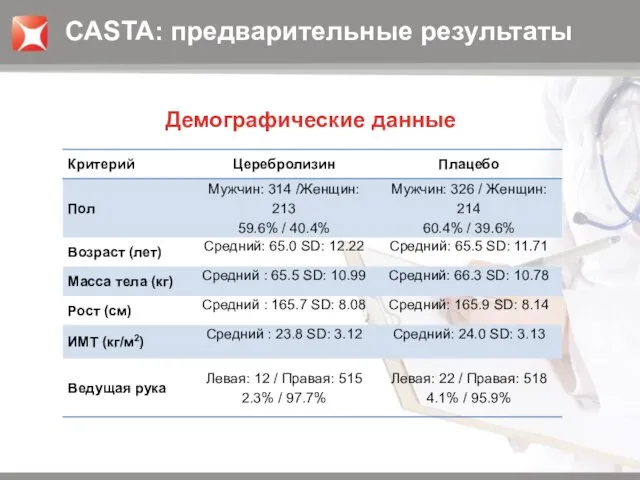
- 9. Демографические данные CASTA: предварительные результаты
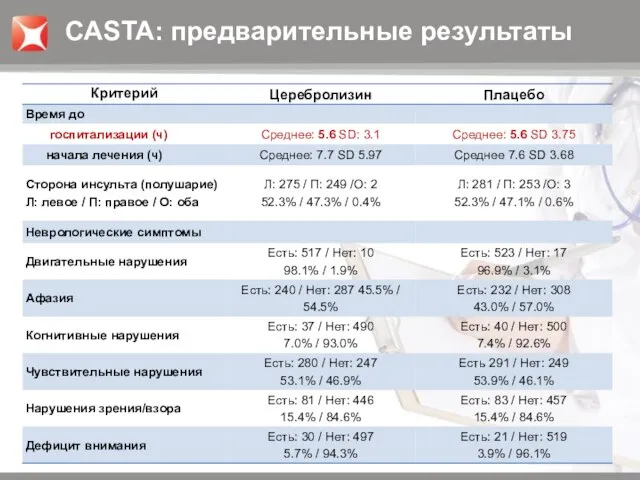
- 10. Тяжесть инсульта CASTA: предварительные результаты
- 11. CASTA: предварительные результаты
- 12. Основной и подтверждающий анализ проводился для трех основных критериев эффективности: модифицированная шкала Ренкина индекс Бартел NIHSS
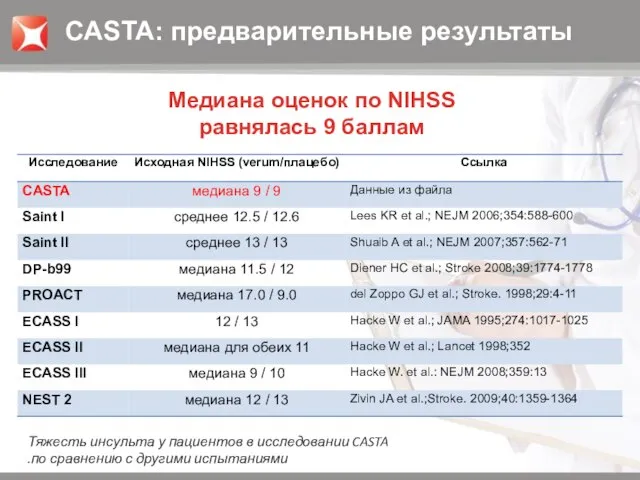
- 13. Медиана оценок по NIHSS равнялась 9 баллам Тяжесть инсульта у пациентов в исследовании CASTA по сравнению
- 14. Это хорошо известный факт, что пациенты с легким инсультом могут восстановиться, получая лишь стандартное лечение. Соответственно,
- 15. Чтобы установить, как тяжесть заболевания на момент поступления влияет на исход, был проведен анализ подгрупп. При
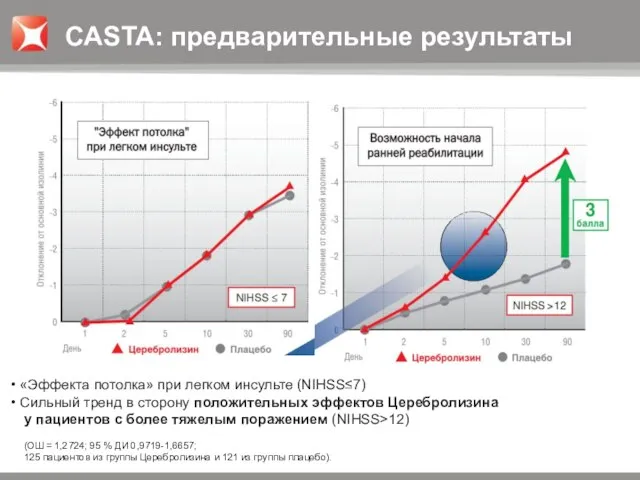
- 16. «Эффекта потолка» при легком инсульте (NIHSS≤7) Сильный тренд в сторону положительных эффектов Церебролизина у пациентов с
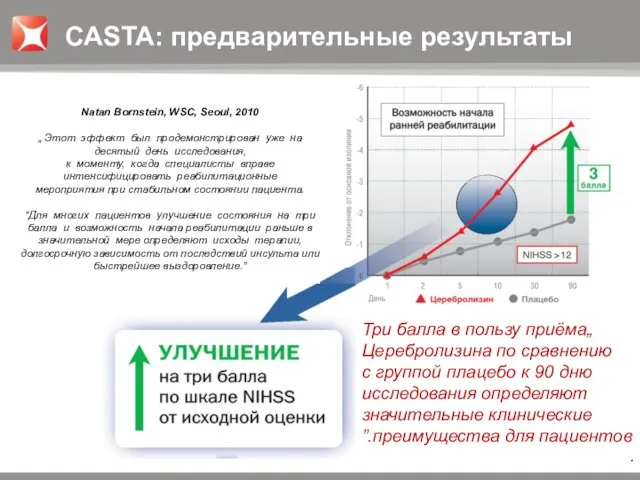
- 17. Natan Bornstein, WSC, Seoul, 2010 „ Этот эффект был продемонстрирован уже на десятый день исследования, к
- 18. Основная конечная точка не подтвердила наличия статистически значимых преимуществ лечения Церебролизином в данной популяции больных. У
- 19. Общее количество побочных эффектов, серьезные и жизнеугрожающие побочные эффекты, основные показатели состояния организма, лабораторные тесты (кровь,
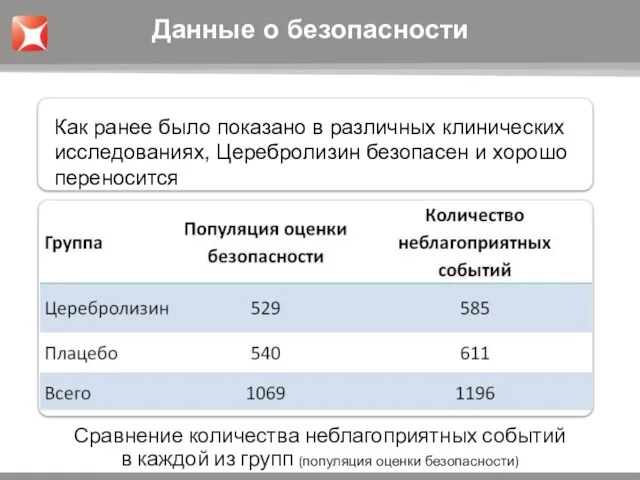
- 20. Сравнение количества неблагоприятных событий в каждой из групп (популяция оценки безопасности) Данные о безопасности Как ранее
- 21. “…Одним из наиболее важных преимуществ Церебролизина является его безопасность, что было продемонстрировано и в исследовании CASTA.”
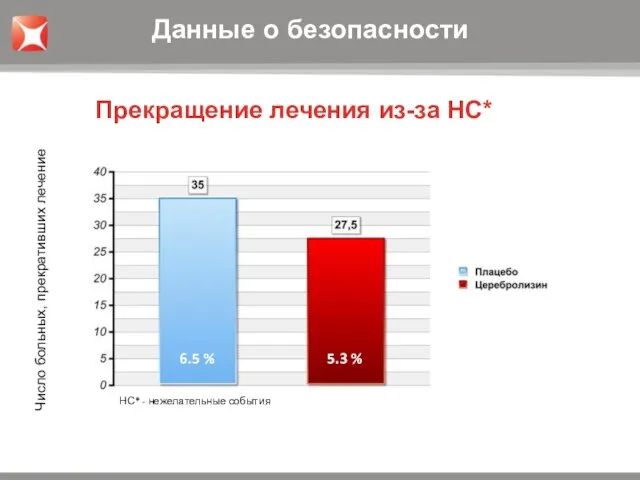
- 22. 5.3 % 6.5 % НС* - нежелательные события Прекращение лечения из-за НС* Число больных, прекративших лечение
- 23. 84 серьезных неблагоприятных события (serious adverse events – SAEs) Церебролизин – 46 SAEs Плацебо – 38
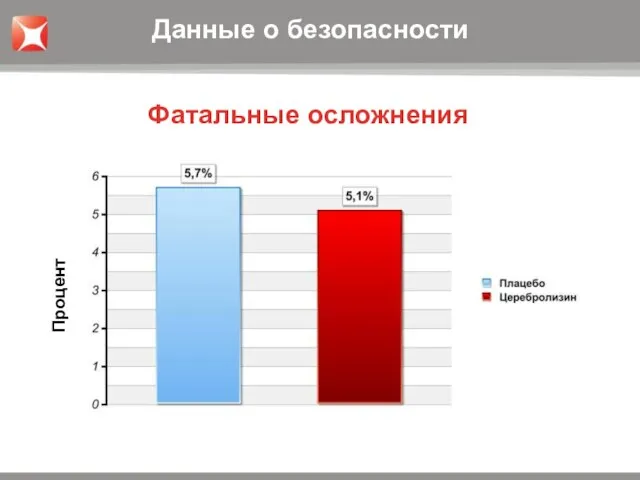
- 24. 5,7% 5,1% Процент Фатальные осложнения Данные о безопасности
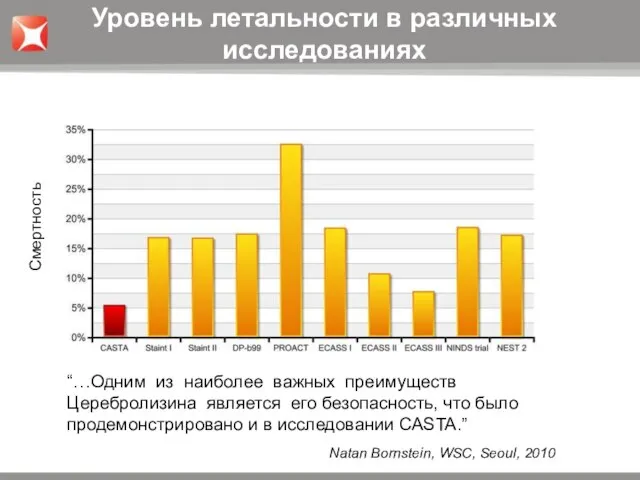
- 25. Общая летальность Вторичные критерии эффективности
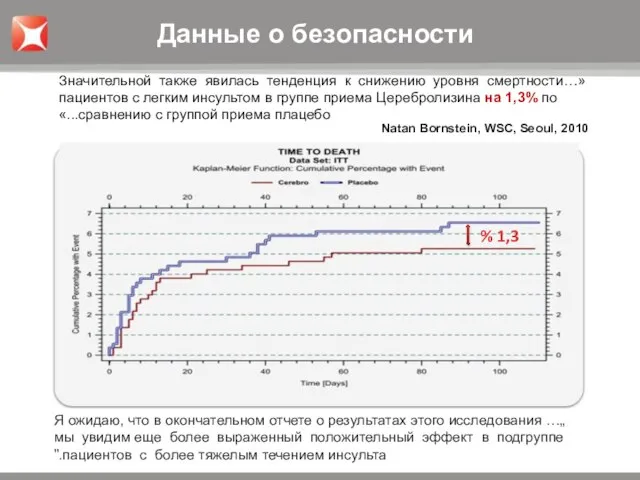
- 26. 1,3 % «…Значительной также явилась тенденция к снижению уровня смертности пациентов с легким инсультом в группе
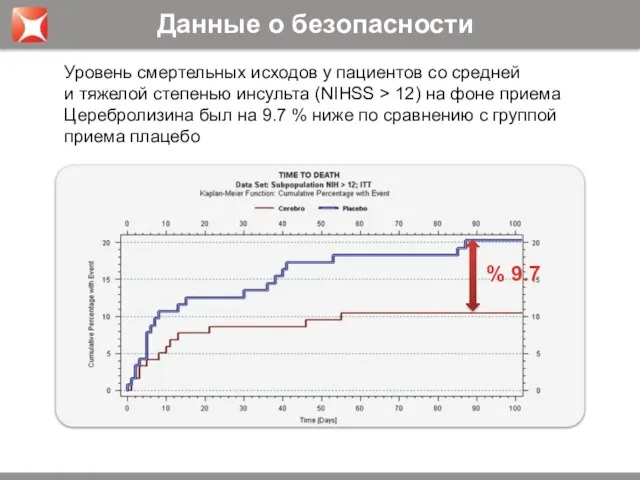
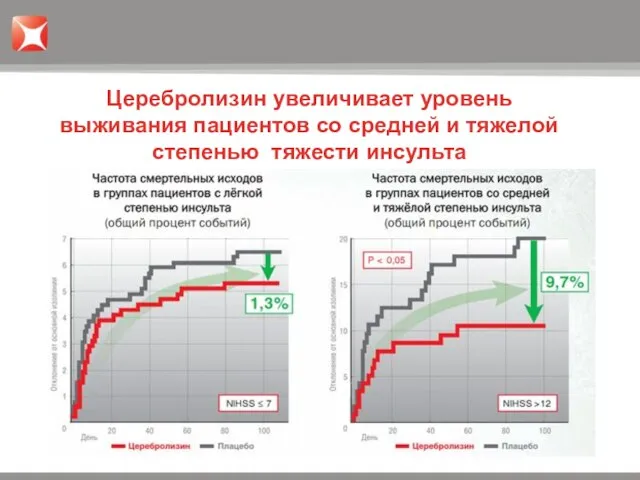
- 27. Уровень смертельных исходов у пациентов со средней и тяжелой степенью инсульта (NIHSS > 12) на фоне
- 28. Церебролизин увеличивает уровень выживания пациентов со средней и тяжелой степенью тяжести инсульта
- 29. Очень низкая летальность (5,4%) Церебролизин безопасен и хорошо переносится У пациентов с легкой степенью тяжести инсульта
- 31. Скачать презентацию















 Участник конкурса Студент года
Участник конкурса Студент года Cпециальное предложение для образовательных учреждений
Cпециальное предложение для образовательных учреждений  тема проекта:
тема проекта: Все действия с десятичными дробями
Все действия с десятичными дробями Relictum Lab. Крипто-бизнес
Relictum Lab. Крипто-бизнес Налогообложение в паевых инвестиционных фондах
Налогообложение в паевых инвестиционных фондах Презентация по английскому Money
Презентация по английскому Money  Новая пленка GMP с возможностью деламинации – TIME CAPSULE!
Новая пленка GMP с возможностью деламинации – TIME CAPSULE! В мире Калевалы
В мире Калевалы Мое хобби или минута славы
Мое хобби или минута славы Анализ типичных нарушений законодательства, выявленных в ходе проверок образовательных учреждений, расположенных на территории
Анализ типичных нарушений законодательства, выявленных в ходе проверок образовательных учреждений, расположенных на территории  МОТИВАЦИЯ БЕЗ ЗАТРАТ Приемы эффективногоруководства подчиненнымиВалерий Поляков
МОТИВАЦИЯ БЕЗ ЗАТРАТ Приемы эффективногоруководства подчиненнымиВалерий Поляков Причастие. Склонение, разряды, образование
Причастие. Склонение, разряды, образование С днём рождения Дианочка
С днём рождения Дианочка Тестирование сезонной корректировки с помощью Demetra+(на примере изменения запасов материальных оборотных средств в текущих ценах)
Тестирование сезонной корректировки с помощью Demetra+(на примере изменения запасов материальных оборотных средств в текущих ценах) Резьбовые соединения. Болтовое соединение
Резьбовые соединения. Болтовое соединение Курс лекций по теоретической механике
Курс лекций по теоретической механике В сердцах наших жить будут вечно Герои минувшей войны
В сердцах наших жить будут вечно Герои минувшей войны Моне и Мане
Моне и Мане Программы кредитования субъектов МСП ОАО АКБ «Связь-Банк»
Программы кредитования субъектов МСП ОАО АКБ «Связь-Банк» Regolith. Твоя высокая доходность на горизонте 3-5 лет
Regolith. Твоя высокая доходность на горизонте 3-5 лет Особенности политической культуры населения Санкт-Петербурга: межпоколенческие разломы
Особенности политической культуры населения Санкт-Петербурга: межпоколенческие разломы Вовлечение пользователяв социальную сеть
Вовлечение пользователяв социальную сеть Архітектура ПЛК Mitsubishi FX3U
Архітектура ПЛК Mitsubishi FX3U Стратегия СММ и ведение личных и коммерческих профилей
Стратегия СММ и ведение личных и коммерческих профилей Создание финансового плана
Создание финансового плана Алфавит
Алфавит Иоганн генрих песталоцци
Иоганн генрих песталоцци