Содержание
- 2. 1 2 3 4 Содержание Строение Zn Свойства Zn Свойства ZnO Свойства Zn(OH) 2
- 3. 30Zn 1s22s22p63s23p64s23d10 d-элемент IV-го периода второй группы побочной подгруппы Zn
- 4. +2 проявляет в соединениях постоянную степень окисления Степень окисления
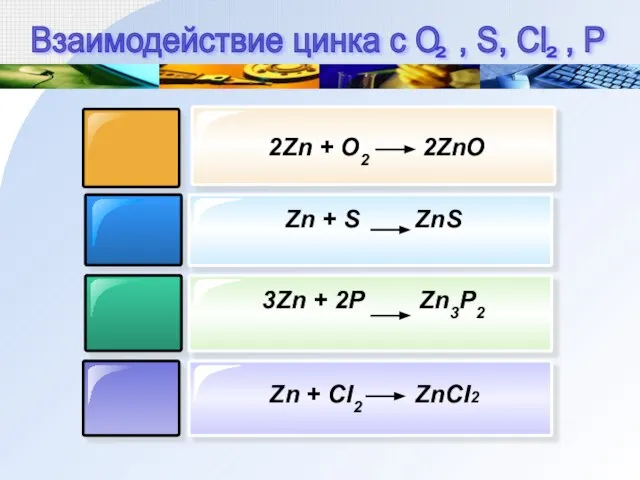
- 5. 2Zn + O2 2ZnO Zn + СI2 ZnCI2 Взаимодействие цинка с O , S, Cl ,
- 6. Zn + 2NaOH + 2H2O Na2 [Zn(OH)4] + H2 Zn + H3PO4 ZnHPO4 + H2 Zn
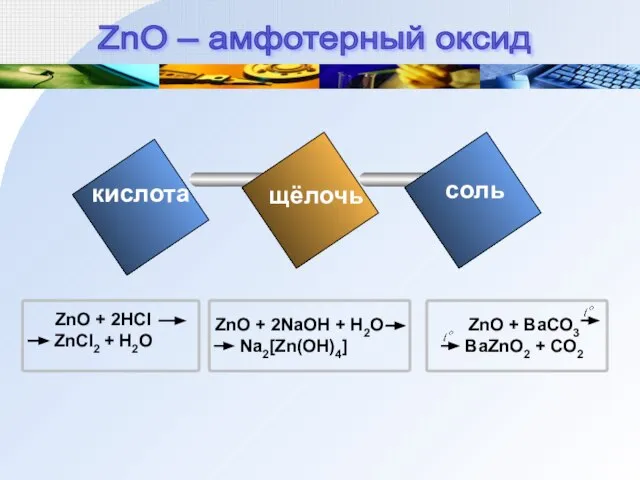
- 7. кислота щёлочь соль ZnO – амфотерный оксид
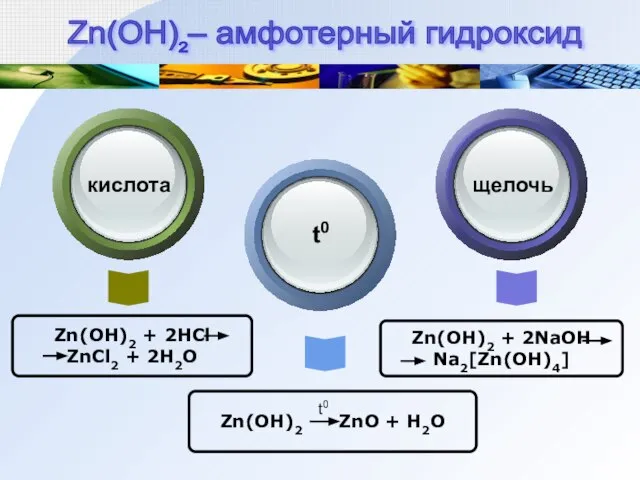
- 8. Zn(OH)2 + 2HCl ZnCl2 + 2H2O Zn(OH)2 ZnO + H2O Zn(OH)2 + 2NaOH Na2[Zn(OH)4] кислота Text
- 9. Zn Na2[Zn(OH)4] ZnSO4 ZnCl2 Zn(OH)2 ZnCl2 Осуществите превращения
- 10. Zn(OH)2 + 2HCl ZnCl2 + 2H2O ZnCl2 + Mg MgCl2 + Zn ZnSO4 + BaCl2 ZnCl2
- 12. Скачать презентацию



![Zn + 2NaOH + 2H2O Na2 [Zn(OH)4] + H2 Zn + H3PO4](/_ipx/f_webp&q_80&fit_contain&s_1440x1080/imagesDir/jpg/370798/slide-5.jpg)
![Zn Na2[Zn(OH)4] ZnSO4 ZnCl2 Zn(OH)2 ZnCl2 Осуществите превращения](/_ipx/f_webp&q_80&fit_contain&s_1440x1080/imagesDir/jpg/370798/slide-8.jpg)

 Вышивка. Образ птицы
Вышивка. Образ птицы Орфографическая диктовка
Орфографическая диктовка Для сх
Для сх Натюрморт
Натюрморт Права несовершеннолетних
Права несовершеннолетних СТОП вырубке ёлок!
СТОП вырубке ёлок! Русский мир
Русский мир Исследование развития речи детей старшего дошкольного возраста в игровой деятельности
Исследование развития речи детей старшего дошкольного возраста в игровой деятельности Предпрофильная подготовка и профильное обучение. Государственная (итоговая) аттестация выпускников
Предпрофильная подготовка и профильное обучение. Государственная (итоговая) аттестация выпускников Физиология мотивации
Физиология мотивации Маркетинговая стратегия
Маркетинговая стратегия СОЦИАЛЬНАЯ МОБИЛЬНОСТЬ
СОЦИАЛЬНАЯ МОБИЛЬНОСТЬ  Иконы православных праздников
Иконы православных праздников Олимпийские игры в Древней Греции
Олимпийские игры в Древней Греции Бумажная филигрань Бумагокручение Квиллинг
Бумажная филигрань Бумагокручение Квиллинг Бенчмаркинг, как инструмент управления организацией
Бенчмаркинг, как инструмент управления организацией Стандартизация. Общие положения стандартизации
Стандартизация. Общие положения стандартизации «Поспорили однажды корень, стебель, лист – кто из них важнее?»
«Поспорили однажды корень, стебель, лист – кто из них важнее?» В море коварном товаров и цен. Бизнес-корабль ведёт…
В море коварном товаров и цен. Бизнес-корабль ведёт… ИНФОРМАЦИЯ. ИНФОРМАТИКА.ИНФОРМАТИЗАЦИЯ.
ИНФОРМАЦИЯ. ИНФОРМАТИКА.ИНФОРМАТИЗАЦИЯ. Служу Отечеству
Служу Отечеству Продукты для «1С:Предприятия»
Продукты для «1С:Предприятия» Dadaisms mērķis. Veidot izpratni par modernisma virzienu dadaismu
Dadaisms mērķis. Veidot izpratni par modernisma virzienu dadaismu Урок -путешествие
Урок -путешествие Прогнозирование и анализ временных рядов
Прогнозирование и анализ временных рядов هدف از معامله کردن در بازار فارکس
هدف از معامله کردن در بازار فارکس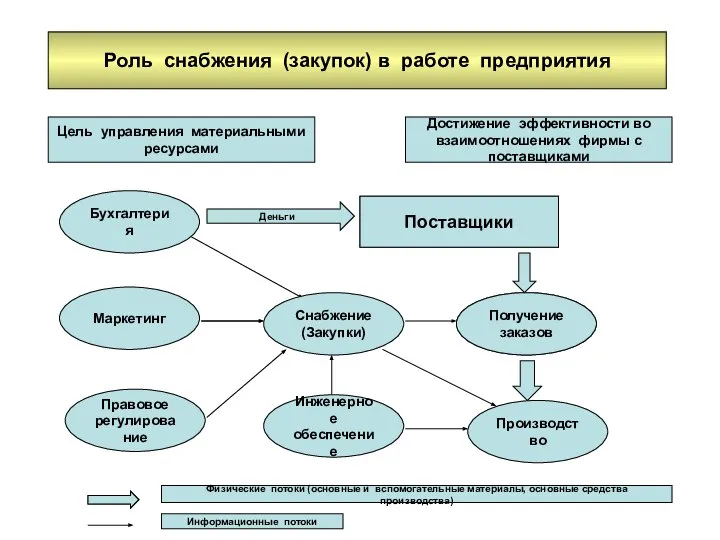 Роль снабжения, закупок в работе предприятия
Роль снабжения, закупок в работе предприятия Правописание о – е после шипящих и ц в окончаниях существительных 5 класс
Правописание о – е после шипящих и ц в окончаниях существительных 5 класс