Слайд 2 концентрация реагирующих веществ:
чем больше концентрация
реагирующих веществ, тем
больше скорость

химической реакции
Закон действующих масс (Н.И.Бекетов)
Скорость химической реакции прямо пропорциональна произведению концентраций реагирующих веществ
2А + 3В = 2С
v = k·CА2·СВ3 , k – константа скорости
Слайд 3Концентрация газообразных веществ

Слайд 4Скорость реакции зависит от концентрации только жидких и газообразных веществ

Слайд 6 температура
Чем выше температура, тем больше
кинетическая энергия частиц, следовательно, больше вероятность

их взаимодействия
Правило Вант-Гоффа (голландский химик):
При повышении температуры на каждые 10С скорость реакции возрастает в 2-4 раза
Слайд 7Некоторые химические реакции протекают с мгновенной скоростью (между кислотами и солями),
другие со

средней скоростью (между оксидами металлов, металлами и кислотами),
но есть реакции, протекающие очень медленно (гидролиз солей, коррозия металлов)
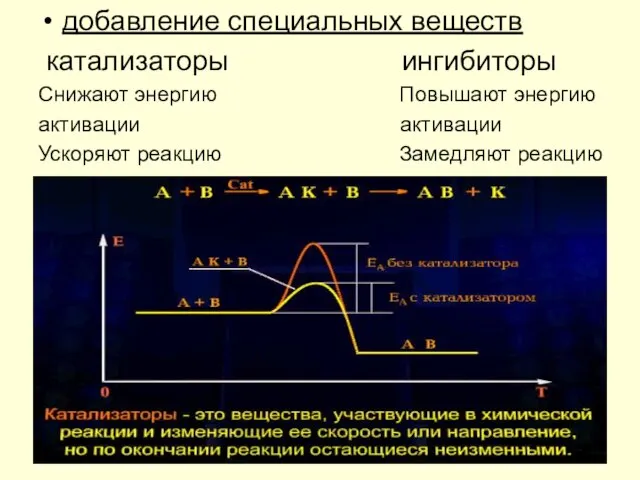
Слайд 9добавление специальных веществ
катализаторы ингибиторы
Снижают энергию Повышают энергию
активации активации
Ускоряют реакцию Замедляют реакцию
Слайд 11природа реагирующих веществ
Zn + 2HCl = ZnCl2 + H2↑
Pb + 2HCl

= PbCl2 + H2↑
Первая реакция протекает быстрее, т.к. цинк более активный металл и легче окисляется, чем свинец
Слайд 13площадь соприкосновения веществ:
Чем меньше размер поверхности
твердых веществ, тем больше площадь

соприкосновения реагирующих веществ,
тем больше скорость реакции
Увеличение площади поверхности соприкосновения достигается:
измельчением веществ;
растворением веществ;
подачей веществ противотоком.













 «MITSUBISHII HEAVY INDUSTRIES» Теперь в Казахстане.
«MITSUBISHII HEAVY INDUSTRIES» Теперь в Казахстане. Право на труд. Трудовые правоотношения
Право на труд. Трудовые правоотношения Управление технического учета и документирования
Управление технического учета и документирования Презентация
Презентация Власть и влияние
Власть и влияние Гражданские дела (первая инстанция) Урок 1.11. Регистрация решения по кассационной жалобе
Гражданские дела (первая инстанция) Урок 1.11. Регистрация решения по кассационной жалобе «Все, что служит системе образования, служит и будущему нашей страны» Н.А.Назарбаев
«Все, что служит системе образования, служит и будущему нашей страны» Н.А.Назарбаев Камиль Сен-Санс Карнавал животных
Камиль Сен-Санс Карнавал животных Отчет по площадке Июль 2012
Отчет по площадке Июль 2012 Транспорт
Транспорт Madame L’Automne
Madame L’Automne Занятие 1 презентация
Занятие 1 презентация Сельское хозяйство мира
Сельское хозяйство мира Храмы Древней Греции
Храмы Древней Греции Российские изобретения
Российские изобретения Я - сообщение
Я - сообщение Бурение скважин при доразведке золото-рудного месторождения Суздаль
Бурение скважин при доразведке золото-рудного месторождения Суздаль Презентация на тему Физиологические адаптации (9 класс)
Презентация на тему Физиологические адаптации (9 класс) Страна Вопросительных местоимений
Страна Вопросительных местоимений Система Пойнтер. Управление компьютером с помощью взгляда
Система Пойнтер. Управление компьютером с помощью взгляда МЕТОДИЧЕСКИЕ РЕКОМЕНДАЦИИ ПО РАЗРАБОТКЕ ОБРАЗОВАТЕЛЬНЫХ ПРОГРАММ ПОСЛЕВУЗОВСКОГО ПРОФЕССИОНАЛЬНОГО ОБРАЗОВАНИЯ (интернатура и
МЕТОДИЧЕСКИЕ РЕКОМЕНДАЦИИ ПО РАЗРАБОТКЕ ОБРАЗОВАТЕЛЬНЫХ ПРОГРАММ ПОСЛЕВУЗОВСКОГО ПРОФЕССИОНАЛЬНОГО ОБРАЗОВАНИЯ (интернатура и Презентация на тему Первый космонавт земли Юрий Алексеевич Гагарин
Презентация на тему Первый космонавт земли Юрий Алексеевич Гагарин  Кельнский собор
Кельнский собор «Герой нашего времени»
«Герой нашего времени» СМШ
СМШ Расти глобально, делать локально: международные компании в Казахстане
Расти глобально, делать локально: международные компании в Казахстане кп к уроку 3
кп к уроку 3 Презентация на тему Ф.Бэкон. Обоснование эмпиризма
Презентация на тему Ф.Бэкон. Обоснование эмпиризма