Содержание
- 2. План урока Фенолы Классификация фенолов Строение молекулы Физические свойства фенола Химические свойства фенола Получение Применение Чем
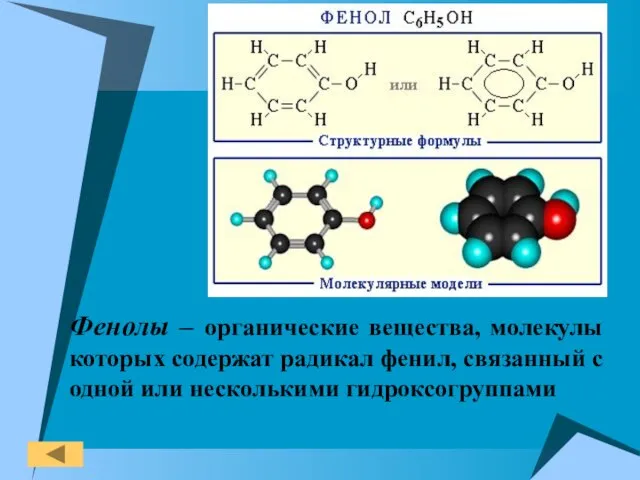
- 3. Фенолы – органические вещества, молекулы которых содержат радикал фенил, связанный с одной или несколькими гидроксогруппами
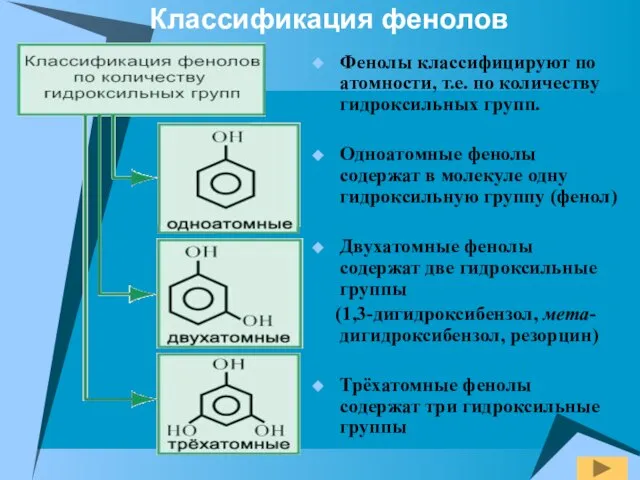
- 4. Фенолы классифицируют по атомности, т.е. по количеству гидроксильных групп. Одноатомные фенолы содержат в молекуле одну гидроксильную
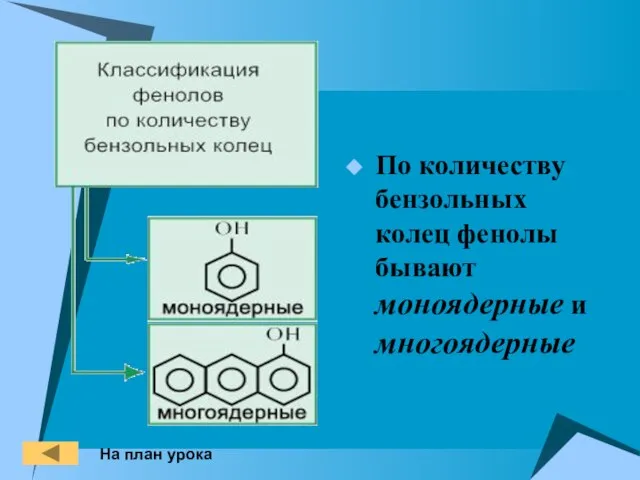
- 5. По количеству бензольных колец фенолы бывают моноядерные и многоядерные На план урока
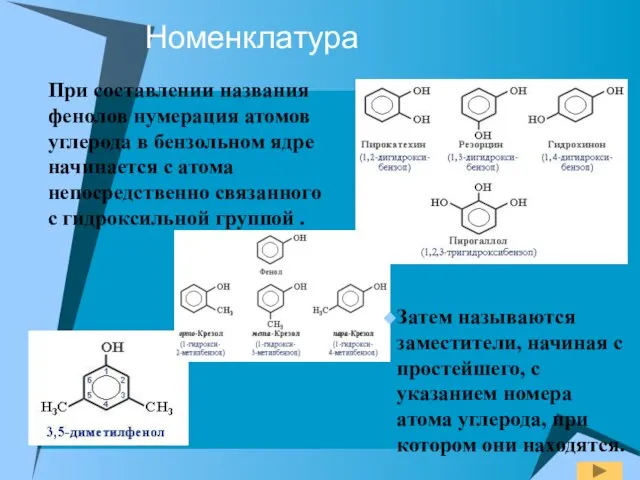
- 6. Номенклатура При составлении названия фенолов нумерация атомов углерода в бензольном ядре начинается с атома непосредственно связанного
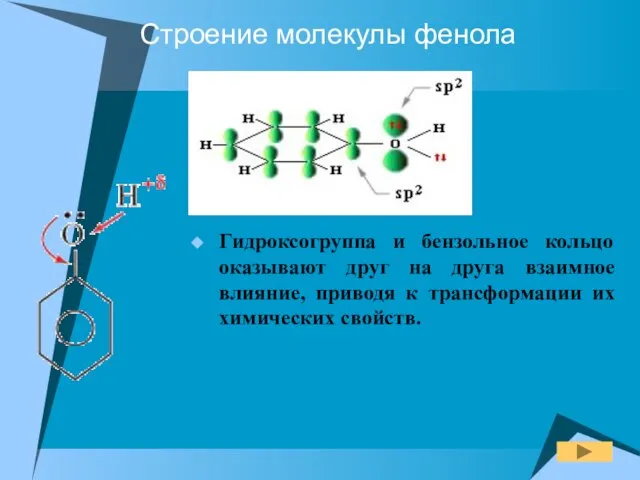
- 7. Строение молекулы фенола Гидроксогруппа и бензольное кольцо оказывают друг на друга взаимное влияние, приводя к трансформации
- 8. Физические свойства фенола Фенол - твёрдое бесцветное кристаллическое вещество. Вследствие частичного окисления на воздухе он бывает
- 9. на план урока
- 10. Химические свойства фенола Химические свойства фенола обусловлены наличием в его молекуле гидроксильной группы бензольного ядра
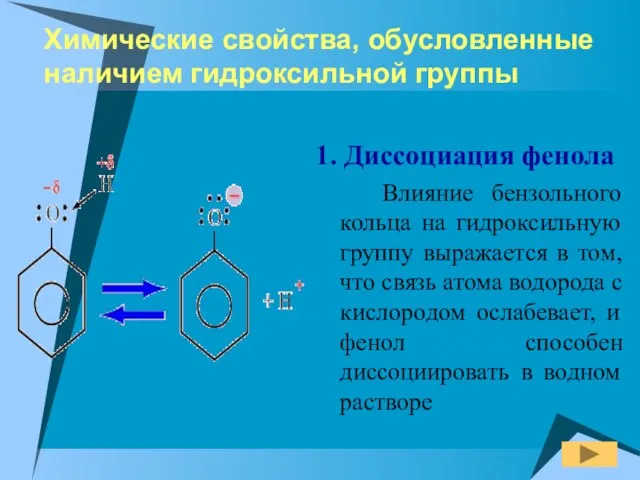
- 11. Химические свойства, обусловленные наличием гидроксильной группы 1. Диссоциация фенола Влияние бензольного кольца на гидроксильную группу выражается
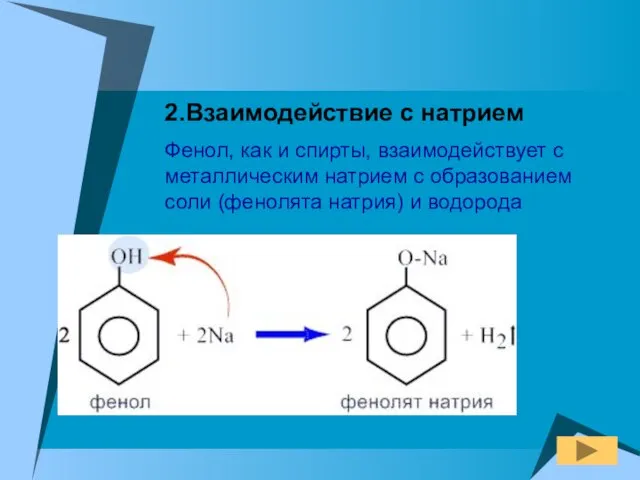
- 12. 2.Взаимодействие с натрием Фенол, как и спирты, взаимодействует с металлическим натрием с образованием соли (фенолята натрия)
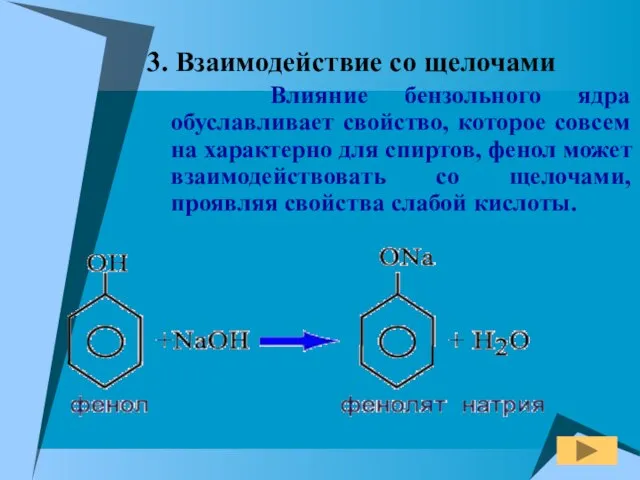
- 13. 3. Взаимодействие со щелочами Влияние бензольного ядра обуславливает свойство, которое совсем на характерно для спиртов, фенол
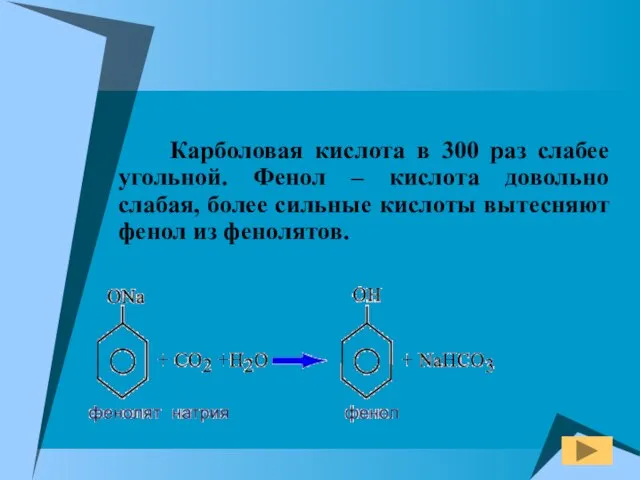
- 15. Карболовая кислота в 300 раз слабее угольной. Фенол – кислота довольно слабая, более сильные кислоты вытесняют
- 16. Химические свойства, обусловленные наличием бензольного ядра Отличия от ароматических углеводородов: 1. Реакции окисления Фенол окисляется кислородом
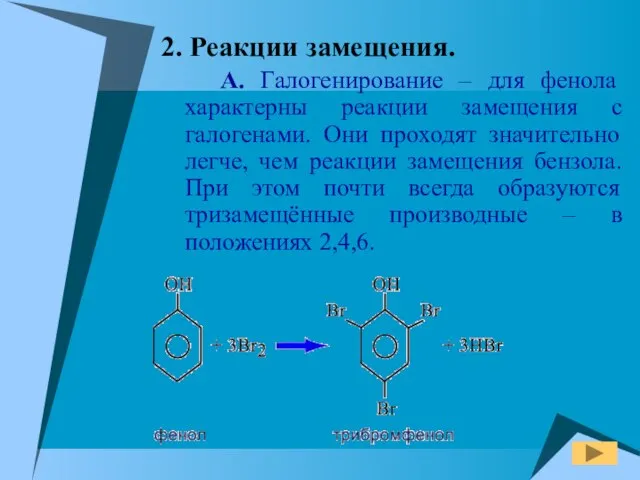
- 17. 2. Реакции замещения. А. Галогенирование – для фенола характерны реакции замещения с галогенами. Они проходят значительно
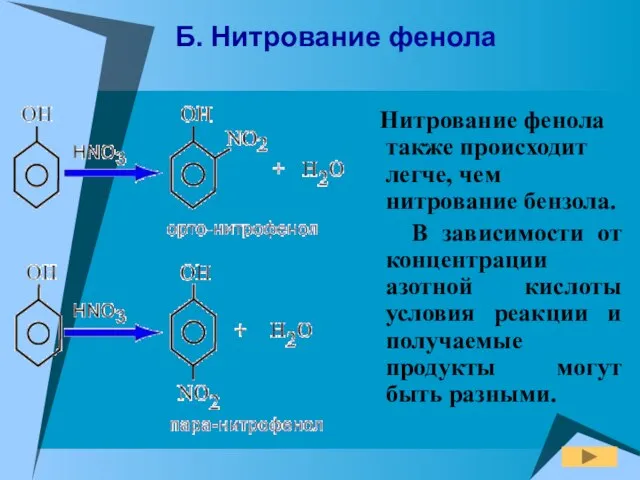
- 19. Б. Нитрование фенола Нитрование фенола также происходит легче, чем нитрование бензола. В зависимости от концентрации азотной
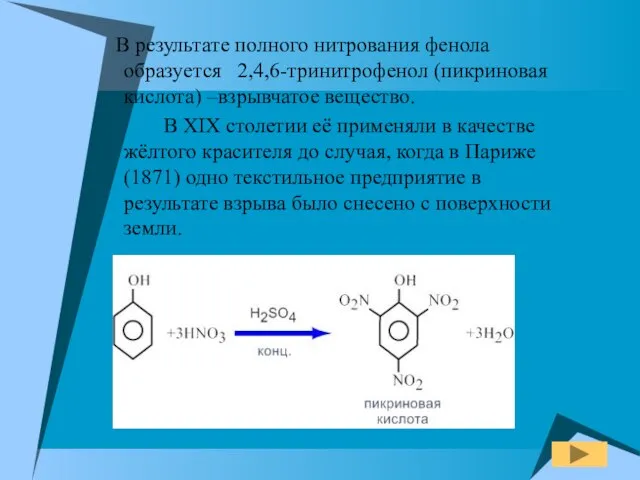
- 20. В результате полного нитрования фенола образуется 2,4,6-тринитрофенол (пикриновая кислота) –взрывчатое вещество. В XIX столетии её применяли
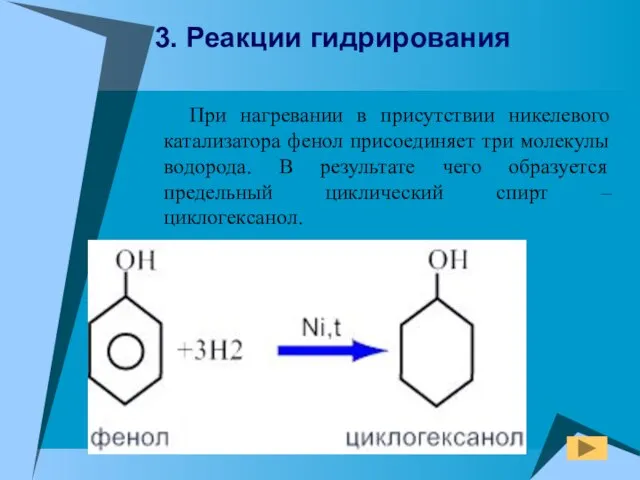
- 21. При нагревании в присутствии никелевого катализатора фенол присоединяет три молекулы водорода. В результате чего образуется предельный
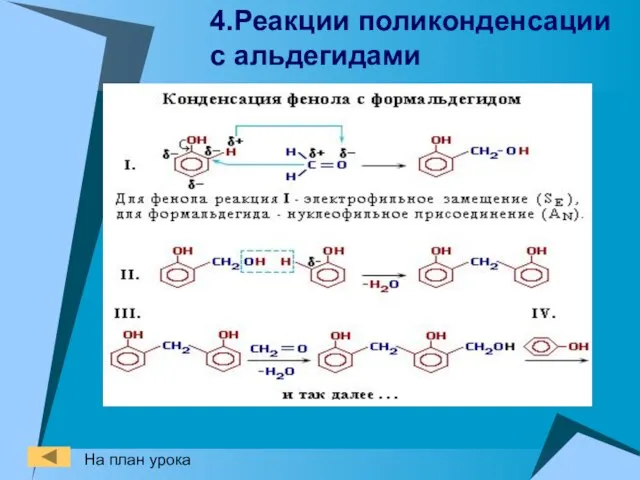
- 22. 4.Реакции поликонденсации с альдегидами На план урока
- 23. 5. Качественная реакция на фенол
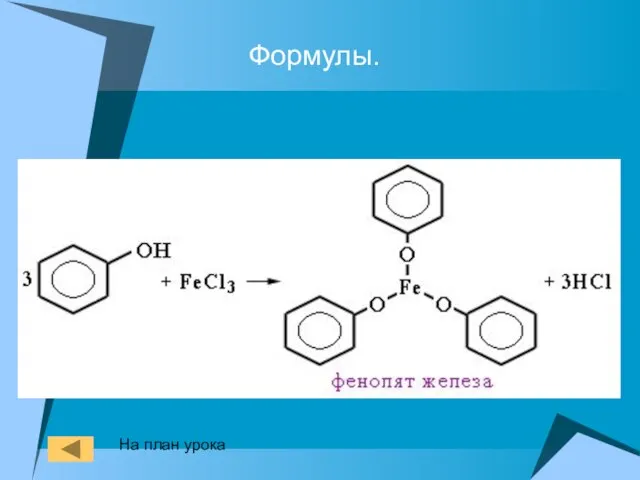
- 24. Формулы. На план урока
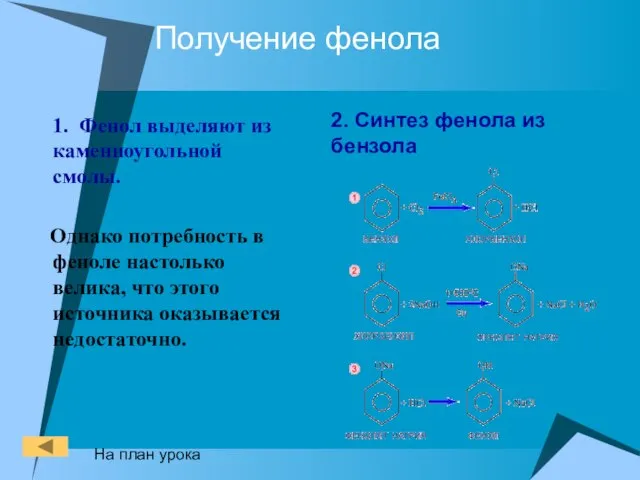
- 25. Получение фенола 1. Фенол выделяют из каменноугольной смолы. Однако потребность в феноле настолько велика, что этого
- 26. Применение фенола. Фенол применяют для производства фенолформальдегидных пластмасс, синтетического волокна капролактам, красителей, лекарств, взрывчатых веществ и
- 27. Чем опасен фенол. Практически сразу после получения фенола ученые установили, что это химическое вещество обладает не
- 28. Сфера применения фенолов достаточно широка, но большинство жителей нашей страны узнало о них из-за скандала, разразившегося
- 30. Скачать презентацию











 Презентация на тему Семейство Зонтичные
Презентация на тему Семейство Зонтичные  Типология и характеристика недвижимого имущества как объектов оценки. Коммерческая недвижимость(склады)
Типология и характеристика недвижимого имущества как объектов оценки. Коммерческая недвижимость(склады) Презентация на тему Отряд хищные
Презентация на тему Отряд хищные  Источники права в Турции
Источники права в Турции Бритвы Braun Учебное пособие
Бритвы Braun Учебное пособие Основные положения конструирования элементов железобетонных конструкций
Основные положения конструирования элементов железобетонных конструкций Презентация на тему Свойства функции (9 класс)
Презентация на тему Свойства функции (9 класс) Основные свойства простейших геометрических фигур
Основные свойства простейших геометрических фигур Игрушки древних славян. Погремушки
Игрушки древних славян. Погремушки Эволюция человека. Первые современные люди - неоантропы
Эволюция человека. Первые современные люди - неоантропы Политические режимы
Политические режимы Игра Для детей 4-5 лет
Игра Для детей 4-5 лет Шындыққа келмейтіндерді жариялаудың проблемалары
Шындыққа келмейтіндерді жариялаудың проблемалары Презентация на тему История Древнего мира 5 класс
Презентация на тему История Древнего мира 5 класс  Царство Божье… и ты
Царство Божье… и ты Тема: как компьютер влияет на наше зрение?
Тема: как компьютер влияет на наше зрение? Принципы административной ответственности
Принципы административной ответственности Что означают наши имена
Что означают наши имена Некоторые подходы к построению автоматизированной системы проведения комплексного анализа результатов обучающихся
Некоторые подходы к построению автоматизированной системы проведения комплексного анализа результатов обучающихся Хрящевые и костные рыбы
Хрящевые и костные рыбы Financial Markets
Financial Markets Круговорот воды в природе (3 класс)
Круговорот воды в природе (3 класс) Классный час «Дороги, которые мы выбираем»
Классный час «Дороги, которые мы выбираем» Реализация государственной научно-технической и инновационной политики
Реализация государственной научно-технической и инновационной политики Гипертоническая болезнь Артериальные гипертензии
Гипертоническая болезнь Артериальные гипертензии Мастер-класс Точка роста
Мастер-класс Точка роста Обучение грамоте (письмо) 1 класс Тема «Прописная буква Ф.» Пропись 4 к «Русской азбуке» В.В. Горецкого Москва «Просвещение» 20
Обучение грамоте (письмо) 1 класс Тема «Прописная буква Ф.» Пропись 4 к «Русской азбуке» В.В. Горецкого Москва «Просвещение» 20 «Лен. Льняное волокно. Сравнительная характеристика растительных волокон и тканей из них»
«Лен. Льняное волокно. Сравнительная характеристика растительных волокон и тканей из них»