Содержание
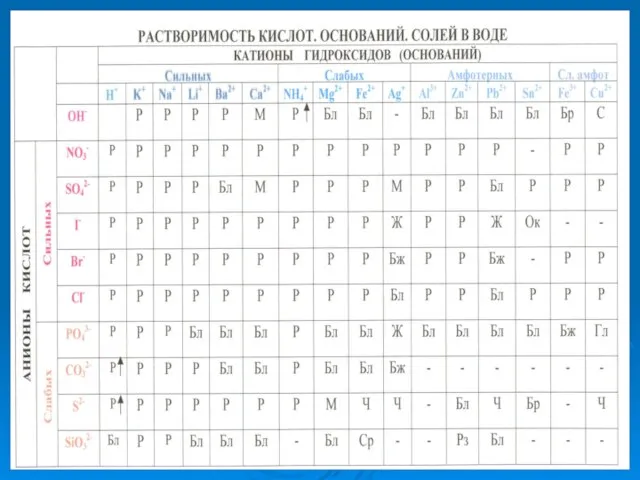
- 3. ОКРАСКА ЛАКМУСОВОЙ БУМАГИ В РАЗЛИЧНЫХ СРЕДАХ
- 4. Тема: Гидролиз солей Цель: изучить сущность гидролиза солей в водных растворах. Задачи : сформулировать определение понятия
- 5. «ГИДРОЛИЗ» - от греческого «гидро» - вода «лизис» - разложение
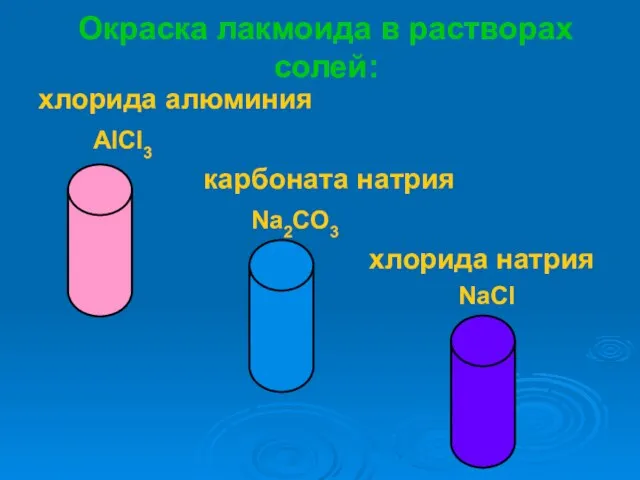
- 6. Окраска лакмоида в растворах солей: хлорида алюминия AlCl3 карбоната натрия Na2CO3 хлорида натрия NaCl
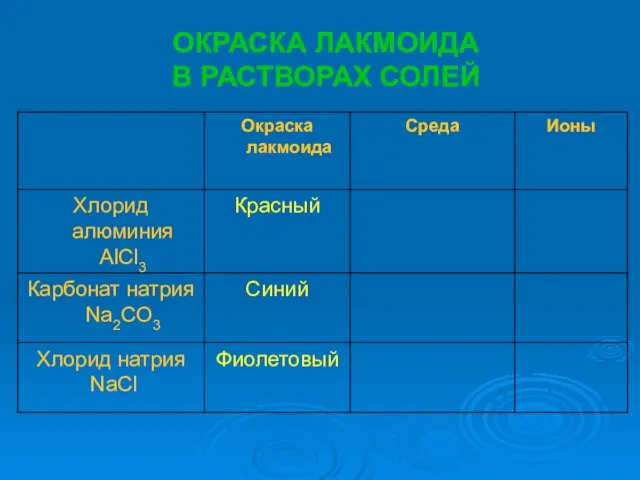
- 7. ОКРАСКА ЛАКМОИДА В РАСТВОРАХ СОЛЕЙ
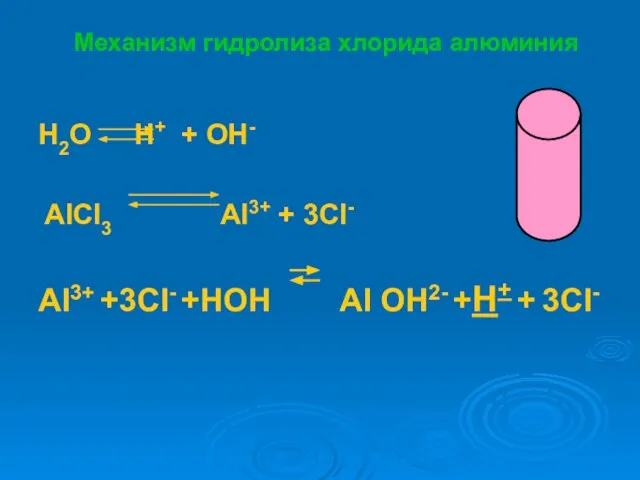
- 8. Механизм гидролиза хлорида алюминия H2O H+ + OH- AlCl3 Al3+ + 3Cl- Al3+ +3Cl- +HOH Al
- 9. Схема гидролиза хлорида алюминия AlCl3 Al(OH)3 HCl слабое основание сильная кислота [OH]- (что сильней того и
- 10. АЛГОРИТМ СОСТАВЛЕНИЯ УРАВНЕНИЙ РЕАКЦИЙ ГИДРОЛИЗА СОЛЕЙ Определить состав соли, то есть указать, каким по силе основанием
- 11. Al3+ + HOH AlOH2+ + H+ AlCl3 + H2O AlOHCl2 + HCl Одним из продуктов данной
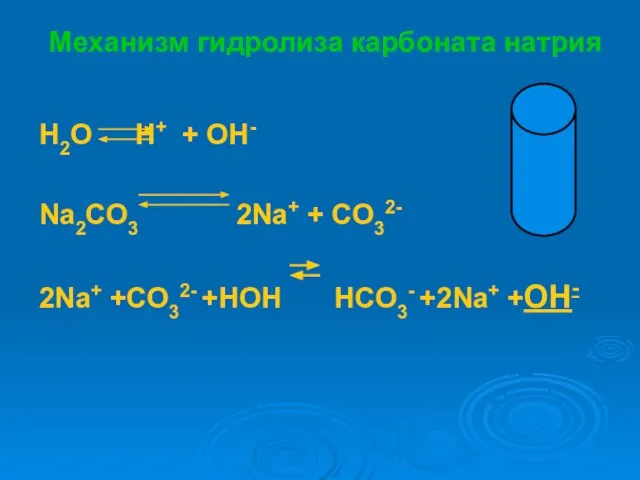
- 12. Механизм гидролиза карбоната натрия H2O H+ + OH- Na2CO3 2Na+ + CO32- 2Na+ +CO32- +HOH HCO3-
- 13. Схема гидролиза карбоната натрия Na2CO3 NaOH H2CO3 сильное основание слабая кислота [OH]- > [H]+ (что сильней
- 14. АЛГОРИТМ СОСТАВЛЕНИЯ УРАВНЕНИЙ РЕАКЦИЙ ГИДРОЛИЗА СОЛЕЙ Определить состав соли, то есть указать, каким по силе основанием
- 15. CO32- +HOH HCO3- +OH- Na2CO3 +H2O NaHCO3 +NaOH Одним из продуктов данной обменной реакции является кислая
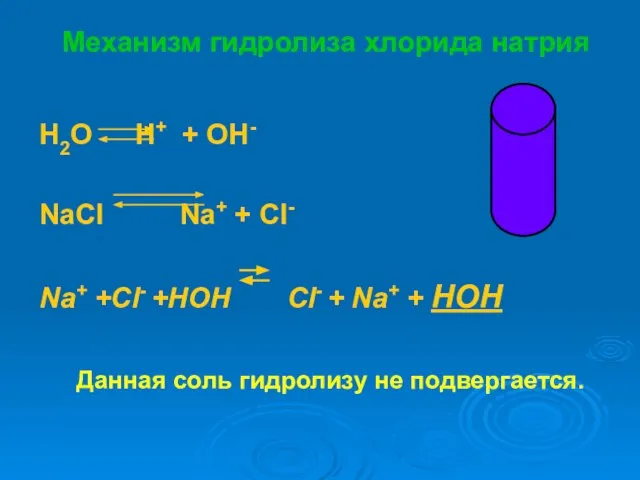
- 16. Механизм гидролиза хлорида натрия H2O H+ + OH- NaСl Na+ + Cl- Na+ +Cl- +HOH Cl-
- 17. Схема гидролиза карбоната натрия NaCl NaOH HCl сильное основание сильная кислота [OH]- = [H]+ Н е
- 18. NaCl + Н2О = Сформулируем вывод: Раствор соли, образованной__________________, имеет________________________реакцию, так как в растворе__________________________________.
- 19. Сформулируем определение понятия «гидролиз»: К какому типу мы отнесем данные реакции? Какие вещества в них участвуют?
- 20. ГИДРОЛИЗ – это реакция обмена между некоторыми солями и водой приводящая к образованию слабого электролита.
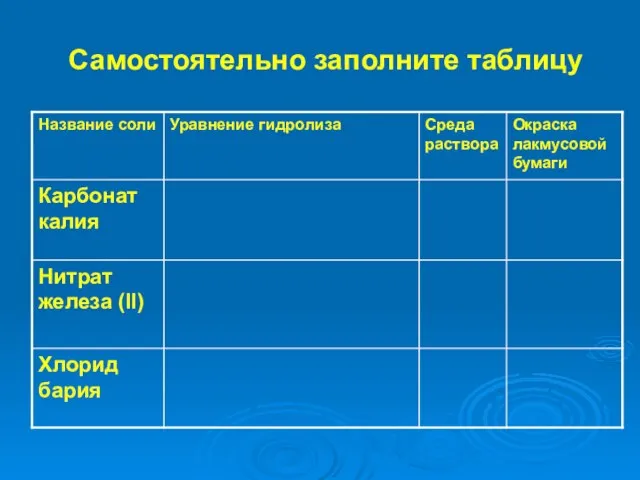
- 22. Самостоятельно заполните таблицу
- 23. Самостоятельно заполните таблицу
- 24. Роль гидролиза в природе Преобразование земной коры Обеспечение слабощелочной среды морской воды
- 25. Роль гидролиза в народном хозяйстве Порча производственного оборудования Выработка из непищевого сырья ценных продуктов (бумага, мыло,
- 26. Роль гидролиза в повседневной жизни человека Стирка Мытье посуды Умывание с мылом Процессы пищеварения
- 27. Ключ к оценке качества выполнения теста: Верные ответы: 1 вариант: 1а, 2б, 3а, S2- + HOH
- 28. Тема: Гидролиз солей Цель: изучить сущность гидролиза солей в водных растворах. Задачи : сформулировать определение понятия
- 30. Скачать презентацию



![Схема гидролиза хлорида алюминия AlCl3 Al(OH)3 HCl слабое основание сильная кислота [OH]-](/_ipx/f_webp&q_80&fit_contain&s_1440x1080/imagesDir/jpg/362173/slide-8.jpg)


![Схема гидролиза карбоната натрия Na2CO3 NaOH H2CO3 сильное основание слабая кислота [OH]-](/_ipx/f_webp&q_80&fit_contain&s_1440x1080/imagesDir/jpg/362173/slide-12.jpg)


![Схема гидролиза карбоната натрия NaCl NaOH HCl сильное основание сильная кислота [OH]-](/_ipx/f_webp&q_80&fit_contain&s_1440x1080/imagesDir/jpg/362173/slide-16.jpg)









 Архитектура итальянского Возрождения
Архитектура итальянского Возрождения Презентация на тему Маржинализм
Презентация на тему Маржинализм  Мини-музей "Югра"
Мини-музей "Югра"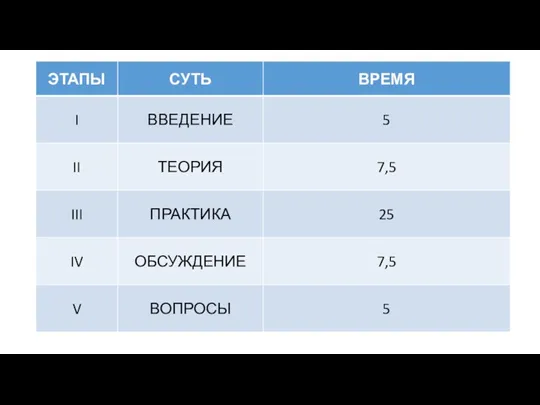 РОБОТ
РОБОТ Особенности литературного сообщества родного края: представители данного сообщества и их творчество
Особенности литературного сообщества родного края: представители данного сообщества и их творчество Отдел автоматизации предприятия
Отдел автоматизации предприятия Помилки, які можна зустріти на вулицях
Помилки, які можна зустріти на вулицях McDonald’s Corporation
McDonald’s Corporation Цель: формирование здорового образа жизни у подростков; формирование правильного представления о гигиенических условиях нормаль
Цель: формирование здорового образа жизни у подростков; формирование правильного представления о гигиенических условиях нормаль Взаимодействие аллельных генов
Взаимодействие аллельных генов Подарочные издания
Подарочные издания На озере
На озере Бизнес-информатика. Анализ ниши в Москве
Бизнес-информатика. Анализ ниши в Москве Профессии моих родителей (2 класс)
Профессии моих родителей (2 класс) 2.Чувашия. (1)
2.Чувашия. (1) Казанская икона
Казанская икона Процесс и базовые шаги установления регулируемых тарифов: обзор
Процесс и базовые шаги установления регулируемых тарифов: обзор Получите новых клиентов в 2 раза дешевле с помощью Антикризисного маркетинга! Создание продающих сайтов!
Получите новых клиентов в 2 раза дешевле с помощью Антикризисного маркетинга! Создание продающих сайтов! Подготовка к зачету. Беседы об искусстве
Подготовка к зачету. Беседы об искусстве Монгол хоол
Монгол хоол Презентация на тему Основные признаки животных организмов
Презентация на тему Основные признаки животных организмов Державин Гавриил Романович
Державин Гавриил Романович Работа электрического тока мощность электрического тока
Работа электрического тока мощность электрического тока Посудный бизнес. Июль 2021
Посудный бизнес. Июль 2021 Деление цветковых растений на однодольные и двудольные. Характерные признаки
Деление цветковых растений на однодольные и двудольные. Характерные признаки «Агропромышленное страхование-2010: Прогноз страховщика».
«Агропромышленное страхование-2010: Прогноз страховщика». Vitamins for children: pros and cons
Vitamins for children: pros and cons Ландшафты болот
Ландшафты болот