Содержание
- 2. Используемые в работе приборы
- 3. Закон Бойля-Мариотта (изотермический процесс) T=const PV=const Устанавливаем начальный объём 152 мл Жмём на поршень и устанавливаем
- 4. Объём воздуха 152 мл, давление воздуха равно атмосферному давлению
- 5. Уменьшаем объём – увеличивается давление. Даём воздуху остыть до прежней температуры, а давлению стабилизироваться.
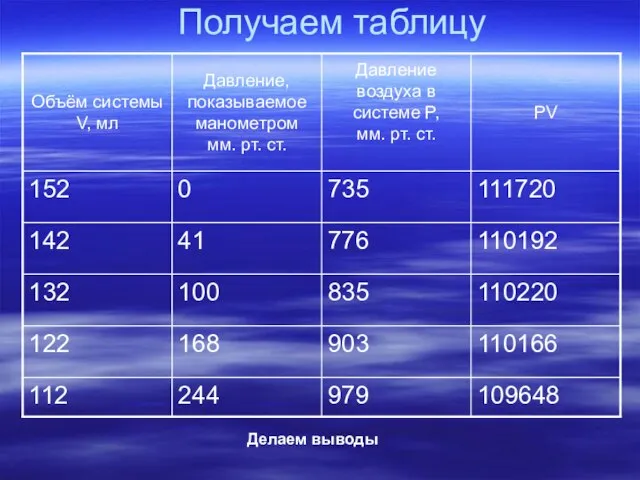
- 6. Получаем таблицу Делаем выводы
- 7. Закон Гей-Люссака(изобарный процесс) P = const V/T = const V = const * T
- 8. Увеличиваем температуру, давление тоже увеличивается
- 9. Чтобы давление сделать таким, каким оно и было надо увеличить объём с 52 до 54 мл
- 10. Продолжаем увеличивать температуру, давление от этого снова увеличивается
- 11. Чтобы вернуть прежнее давление, снова приходится увеличивать объём, теперь с 54 мл до 56 мл
- 12. Итоговая таблица измерений и вычислений
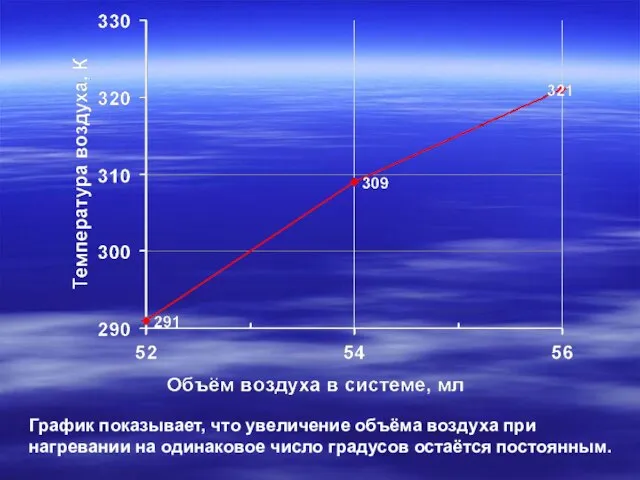
- 13. График показывает, что увеличение объёма воздуха при нагревании на одинаковое число градусов остаётся постоянным.
- 14. Вычислим коэффициент объёмного расширения воздуха при постоянном давлении Таким образом с повышением температуры на 1 градус
- 15. Закон Шарля (изохорный процесс) V = const P / T = const P = const *
- 16. Начальная температура воздуха 18 градусов. Давление воздуха в системе равно атмосферному. Манометр не показывает избыточного давления
- 17. Увеличили температуру, давление тоже увеличилось. Объём не меняется.
- 18. Продолжаем увеличивать температуру. Давление растёт.
- 20. Скачать презентацию















 Психология общения. Тема 2
Психология общения. Тема 2 Золотое сечение
Золотое сечение Основные производственные фонды
Основные производственные фонды Сон без стресса и тревоги
Сон без стресса и тревоги Компетентностный
Компетентностный Опыт внедрения системы Офис-кайдзен в ТЭЦ ОАО Иркутскэнерго
Опыт внедрения системы Офис-кайдзен в ТЭЦ ОАО Иркутскэнерго Адаптация спортсменов к выполнению специфических статических нагрузок
Адаптация спортсменов к выполнению специфических статических нагрузок Обеспечение карьерного роста в образовательном учреждении
Обеспечение карьерного роста в образовательном учреждении Бизнес план
Бизнес план Презентация на тему Лицейские друзья Пушкина
Презентация на тему Лицейские друзья Пушкина  Настольный теннис. Правила игры
Настольный теннис. Правила игры Презентация на тему Общественный строй Древней Руси (6 класс)
Презентация на тему Общественный строй Древней Руси (6 класс) Международный день грамотности
Международный день грамотности YTRON® ... все зависит от головки!
YTRON® ... все зависит от головки! Введение в алгебру логики
Введение в алгебру логики О Корабле
О Корабле Иллюзии зрения
Иллюзии зрения Мультивалютный сервис Alpha Cash
Мультивалютный сервис Alpha Cash Нормы трудового права. Тест
Нормы трудового права. Тест ИСТОРИЯ ОРУЖИЯ
ИСТОРИЯ ОРУЖИЯ Музеи изобразительного искусства
Музеи изобразительного искусства Баргузинский заповедник как составная часть природного наследия "озеро Байкал"
Баргузинский заповедник как составная часть природного наследия "озеро Байкал" Организация учебного процесса на 1 курсе ОЗО
Организация учебного процесса на 1 курсе ОЗО Content_Changes
Content_Changes Классицизм и барокко
Классицизм и барокко Полуектов Иван Фёдорович (29.08.1903 - 12.07.1944)
Полуектов Иван Фёдорович (29.08.1903 - 12.07.1944) Организация учета документов АФ РФ и других архивных документов в архиве
Организация учета документов АФ РФ и других архивных документов в архиве Кормление свиней. Составление кормовых смесей
Кормление свиней. Составление кормовых смесей