Содержание
- 2. Немного истории Понятие об атомах зародилось еще в Древней Греции. Теория была столь же проста сколь
- 3. Разные точки зрения Первое изложение этой теории относится примерно к 400 г. До н.э. и принадлежит
- 4. Если же деление нельзя продолжать бесконечно, рано поздно мы дойдём до мельчайшей частички, которую Демокрит назвал
- 5. Британский химик Роберт Бойль (1627 – 1691) выдвинул предположение, что материя состоит их неких первичных частиц,
- 6. Модели атомов «пудинг с изюмом» - предложил на грани ХIХ и ХХ веков английский ученый Дж.
- 7. В 1932 году английский физик Джеймс Чедвик (1891 – 1974) создал новую модель. Хоть она и
- 8. Соединение атомов Ковалентные соединения: при образовании ковалентных соединений атомы различных элементов делятся друг с другом своими
- 9. Такая разная материя Твердые тела, жидкости и газы – это различные агрегатные состояния вещества. Вещество не
- 10. Газообразное состояние вещества Газы не имеют собственной формы и объёма и, как правило, смешиваются друг с
- 11. Конденсированное состояние вещества К конденсированным системам относятся жидкости и твердые тела. В жидкостях и твердых телах
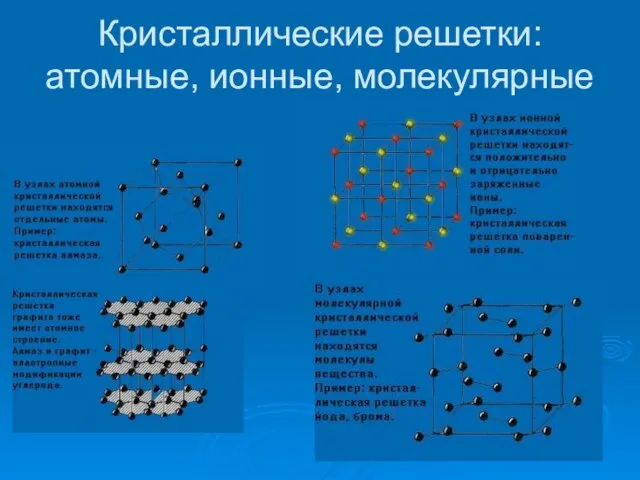
- 12. Кристаллические решетки: атомные, ионные, молекулярные
- 14. Скачать презентацию










 Архитектура итальянского Возрождения
Архитектура итальянского Возрождения Презентация на тему Маржинализм
Презентация на тему Маржинализм  Мини-музей "Югра"
Мини-музей "Югра" РОБОТ
РОБОТ Особенности литературного сообщества родного края: представители данного сообщества и их творчество
Особенности литературного сообщества родного края: представители данного сообщества и их творчество Отдел автоматизации предприятия
Отдел автоматизации предприятия Помилки, які можна зустріти на вулицях
Помилки, які можна зустріти на вулицях McDonald’s Corporation
McDonald’s Corporation Цель: формирование здорового образа жизни у подростков; формирование правильного представления о гигиенических условиях нормаль
Цель: формирование здорового образа жизни у подростков; формирование правильного представления о гигиенических условиях нормаль Взаимодействие аллельных генов
Взаимодействие аллельных генов Подарочные издания
Подарочные издания На озере
На озере Бизнес-информатика. Анализ ниши в Москве
Бизнес-информатика. Анализ ниши в Москве Профессии моих родителей (2 класс)
Профессии моих родителей (2 класс) 2.Чувашия. (1)
2.Чувашия. (1) Казанская икона
Казанская икона Процесс и базовые шаги установления регулируемых тарифов: обзор
Процесс и базовые шаги установления регулируемых тарифов: обзор Получите новых клиентов в 2 раза дешевле с помощью Антикризисного маркетинга! Создание продающих сайтов!
Получите новых клиентов в 2 раза дешевле с помощью Антикризисного маркетинга! Создание продающих сайтов! Подготовка к зачету. Беседы об искусстве
Подготовка к зачету. Беседы об искусстве Монгол хоол
Монгол хоол Презентация на тему Основные признаки животных организмов
Презентация на тему Основные признаки животных организмов Державин Гавриил Романович
Державин Гавриил Романович Работа электрического тока мощность электрического тока
Работа электрического тока мощность электрического тока Посудный бизнес. Июль 2021
Посудный бизнес. Июль 2021 Деление цветковых растений на однодольные и двудольные. Характерные признаки
Деление цветковых растений на однодольные и двудольные. Характерные признаки «Агропромышленное страхование-2010: Прогноз страховщика».
«Агропромышленное страхование-2010: Прогноз страховщика». Vitamins for children: pros and cons
Vitamins for children: pros and cons Ландшафты болот
Ландшафты болот