Содержание
- 2. Проблемно- исследовательский урок химии в 9-м классе Аммиак
- 3. План урока. 1. Актуализация знаний. 2. Значение связывания азота. 3. Строение молекулы аммиака. 4. Получение. 5.
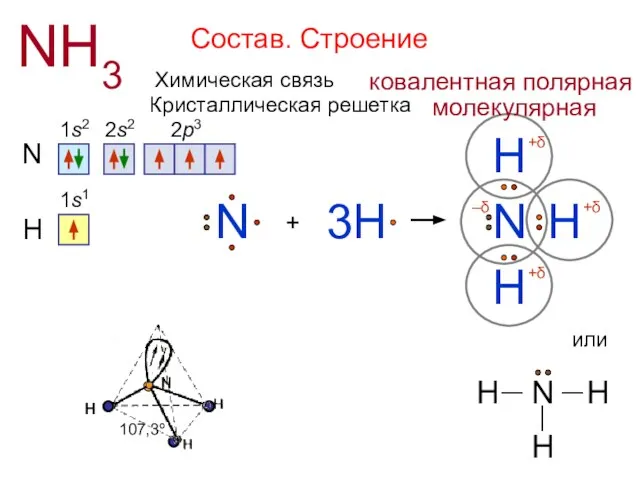
- 4. Состав. Строение NH3 N 1s2 2s2 2p3 + H N H H 3H H N 1s1
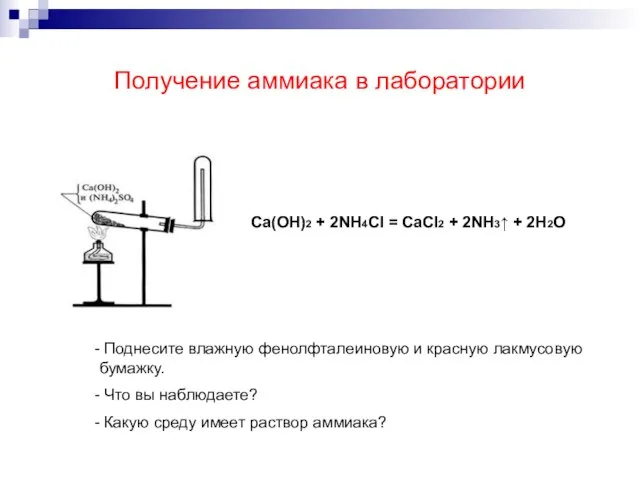
- 5. Получение аммиака в лаборатории Ca(OH)2 + 2NH4Cl = CaCl2 + 2NH3↑ + 2H2O Поднесите влажную фенолфталеиновую
- 6. Физические свойства При незначительном повышении давления или при охлаждении до – 33Сº аммиак сжижается, превращаясь в
- 7. Биологическое действие аммиака. + Средства I помощи при отравлении аммиаком: - Свежий воздух, Обильное промывание глаз
- 8. Химические свойства Является восстановителем. За счет чего аммиак может вступать в реакции присоединения?
- 9. Применение аммиака 1. Производство пластмасс и волокон 2. В составе моющих средств 4. В сельском хозяйстве
- 10. NH3 1 4 2 3 5 6 7
- 11. ПДК аммиака составляет 0,001 мг/л. Рассчитайте концентрацию аммиака после проведения лабораторного опыта.
- 13. Скачать презентацию








 Пример схемы для ЕАСД. Схемы размещения моторовагонных депо
Пример схемы для ЕАСД. Схемы размещения моторовагонных депо CTI приложения для офисных АТС Panasonic KX-TD/KX-TDA семейства BLITZ. Описание и функции
CTI приложения для офисных АТС Panasonic KX-TD/KX-TDA семейства BLITZ. Описание и функции Моя любимая группа
Моя любимая группа Поэтический образ Родины
Поэтический образ Родины Исследовательская работа на тему: «В старопольской кухне и за польским столом»
Исследовательская работа на тему: «В старопольской кухне и за польским столом» Презентация на тему Воспитательно-образовательная работа с детьми подготовительной к школе группы
Презентация на тему Воспитательно-образовательная работа с детьми подготовительной к школе группы Физические и
Физические и Что такое JavaScriptЧто такое JavaScriptC# C++ Java Delphi Eiffel Simula D Io Objective-C Object Pascal VB.NET Visual DataFlex Perl PowerBuilder Python. - презентация
Что такое JavaScriptЧто такое JavaScriptC# C++ Java Delphi Eiffel Simula D Io Objective-C Object Pascal VB.NET Visual DataFlex Perl PowerBuilder Python. - презентация 2_5328138068648009249
2_5328138068648009249 Прикладное искусство первой половины ХХ века
Прикладное искусство первой половины ХХ века Счастливы те люди. Кто учит Библию.
Счастливы те люди. Кто учит Библию. Структура активов и пассивов предприятия АПК
Структура активов и пассивов предприятия АПК Колобок
Колобок День народного единства
День народного единства Продвижение в торговых сетях. Активные методы продвижения.
Продвижение в торговых сетях. Активные методы продвижения. Презентация на тему Моя малая Родина (1 класс)
Презентация на тему Моя малая Родина (1 класс) КУРС ИНФОРМАЦИОННАЯ КУЛЬТУРА И/ИЛИ КОМПЬЮТЕР НА УРОКЕ БИОЛОГИИ
КУРС ИНФОРМАЦИОННАЯ КУЛЬТУРА И/ИЛИ КОМПЬЮТЕР НА УРОКЕ БИОЛОГИИ Белорусский костюм (1)
Белорусский костюм (1) Новая Букмекерская контора BINOM
Новая Букмекерская контора BINOM Собачка из кругов
Собачка из кругов Презентация на тему Функциональная схема компьютера
Презентация на тему Функциональная схема компьютера  Пересмотр ГОСТ 32600. Версия ООО НПК Герметика
Пересмотр ГОСТ 32600. Версия ООО НПК Герметика Произведения искусства Микеланджело
Произведения искусства Микеланджело Психология как профессия
Психология как профессия Avez-vous des tomates?
Avez-vous des tomates? Волшебный мир
Волшебный мир Рентгенография черепа
Рентгенография черепа Пробелы в области юридических и иных знаний у сотрудников таможенных органов
Пробелы в области юридических и иных знаний у сотрудников таможенных органов