Слайд 2№ 3 стр. 99
CaCl2
MgCO3
Zn(NO3)2
Al2(SO4)3
K2CO3
Na2SO4
Na2SiO3
AgCl
MgSO3
Al2S3
Слайд 3Кислотные оксиды – это оксиды, которым соответствуют кислоты.
Ангидрид – обезвоженная кислота
H2SO3

SO2 + H2O
H2CO3 CO2 + H2O
Слайд 4При взаимодействии кислотных оксидов (ангидридов) с водой образуются кислоты
N2O3 + H2O
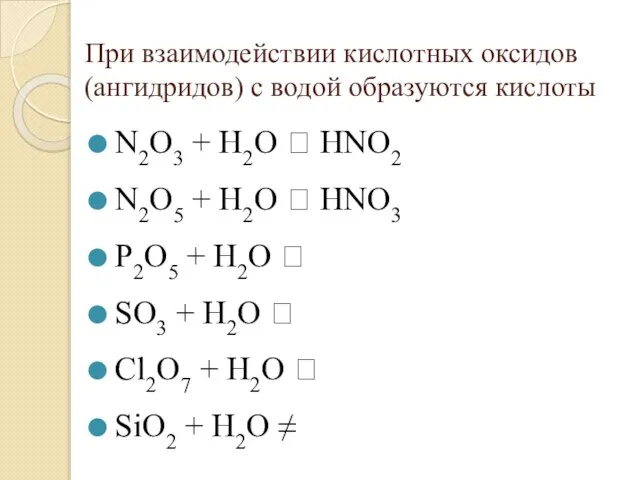
HNO2
N2O5 + H2O HNO3
P2O5 + H2O
SO3 + H2O
Cl2O7 + H2O
SiO2 + H2O ≠
Слайд 5При полной дегидратации гидроксидов всегда получаются оксиды:
H2SO4 = SO3 + H2O
2LiOH = Li2O + H2O
H2CO3 =CO2 + H2O
Ca(OH)2 = CaO
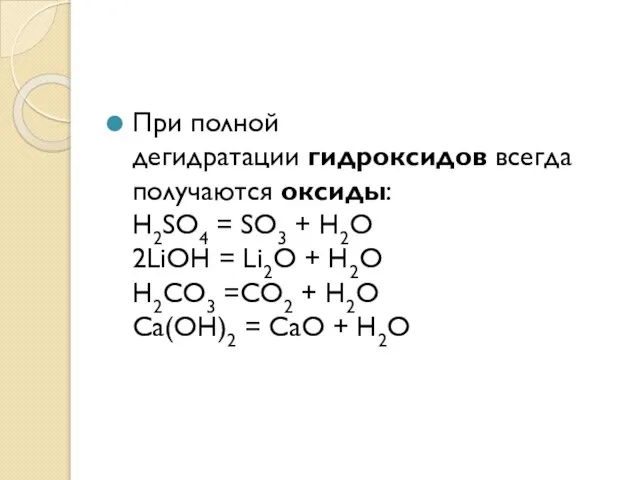
+ H2O
Слайд 6примеры
Оксид углерода(IV) CO2;
Оксид серы(IV) SO2;
Оксид серы(VI) SO3;
Оксид кремния(IV) SiO2;
Оксид хрома(VI) CrO3;
Оксид марганца(VII) Mn2O7;
Оксид азота (IV) NO2;
Оксид хлора (V)

Cl2O5,
Оксид хлора (III) Cl2O3
Оксид фосфора (V) P2O5
Оксид азота (V) N2O5
Оксид азота (III) N2O3
Оксид фосфора (v) P2O5
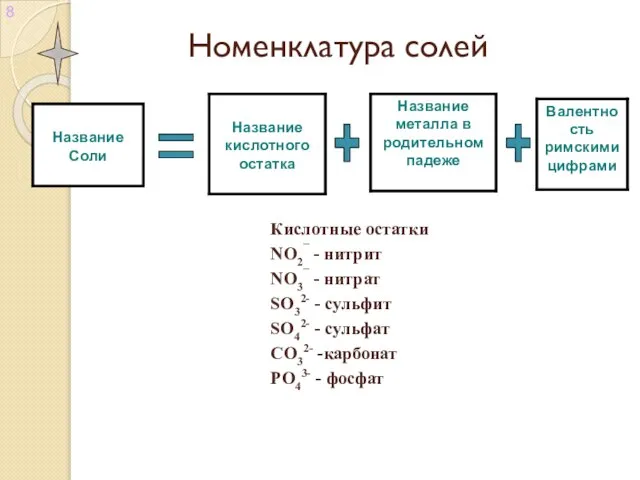
Слайд 9Составить формулу сульфата алюминия:
Al
2
SO
4
3
( )
III
II







 КОНКУРСНАЯ РАБОТА В НОМИНАЦИИ «ГЕНПЛАН» ПРОИЗВОДСТВЕНЫЙ ПРОЕКТ «Компрессорная станция «Приозерная» Стадия: Проектная докумен
КОНКУРСНАЯ РАБОТА В НОМИНАЦИИ «ГЕНПЛАН» ПРОИЗВОДСТВЕНЫЙ ПРОЕКТ «Компрессорная станция «Приозерная» Стадия: Проектная докумен 2 ФМ. 6-12 вебинары
2 ФМ. 6-12 вебинары «Слишком много на свете людей, которым никто не помог пробудиться.» А. Экзюпери
«Слишком много на свете людей, которым никто не помог пробудиться.» А. Экзюпери Разработка информационной системы для автоматизация бизнес-процессов ООО «Кузбасс - Эксперт»
Разработка информационной системы для автоматизация бизнес-процессов ООО «Кузбасс - Эксперт» Виды давления
Виды давления Шпонированные изделия
Шпонированные изделия Презентация на тему Взаимодействие людей в многонациональном обществе
Презентация на тему Взаимодействие людей в многонациональном обществе Презентация Microsoft PowerPoint
Презентация Microsoft PowerPoint Трудовое право
Трудовое право Влияние цвета на человека
Влияние цвета на человека Практическое применение технологий Business Intelligence при выработке научно-промышленной политики и управления имуществом г. Москвы
Практическое применение технологий Business Intelligence при выработке научно-промышленной политики и управления имуществом г. Москвы Изготовление образца ткацкого переплетения (Практическая работа№ 2)
Изготовление образца ткацкого переплетения (Практическая работа№ 2) Мое лето в Марбельи
Мое лето в Марбельи Поэты Кубани
Поэты Кубани Основные механизмы реализации пилотного проекта по развитию общего образования города Москвы.
Основные механизмы реализации пилотного проекта по развитию общего образования города Москвы. Образование в Великобритании
Образование в Великобритании Презентация на тему Красная книга Ставропольского края
Презентация на тему Красная книга Ставропольского края Операционный консалтинг
Операционный консалтинг Лекция 2
Лекция 2 Рестайлинг элемента в логотипе бочонка
Рестайлинг элемента в логотипе бочонка Инновационное развитие и информационно – коммуникационные технологии: новые механизмы и государственно – частное партнерство (
Инновационное развитие и информационно – коммуникационные технологии: новые механизмы и государственно – частное партнерство (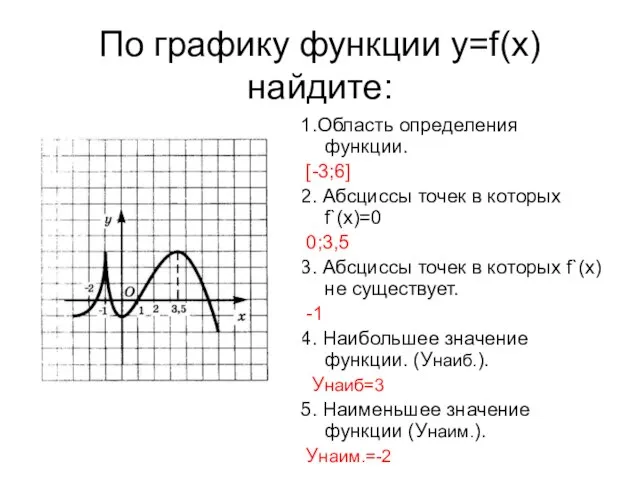 По графику функции у=f(x) найдите:
По графику функции у=f(x) найдите: Живая и неживая природа (2 класс)
Живая и неживая природа (2 класс) Презентация на тему Русские и татарские народные игры
Презентация на тему Русские и татарские народные игры Проведение мероприятий в г. Прага октябрь 2011 – февраль 2012. - презентация
Проведение мероприятий в г. Прага октябрь 2011 – февраль 2012. - презентация Интегрированный урок по математике и музыке.
Интегрированный урок по математике и музыке. Культура Московской Руси
Культура Московской Руси Большой этнографический диктант 2021 Народов много-страна одна
Большой этнографический диктант 2021 Народов много-страна одна