Содержание
- 2. Коллоидная химия Дисперсная система Дисперсная фаза (раздробленная часть дисперсной системы) Дисперсионная среда (непрерывная часть дисперсной системы)
- 3. Признаки объектов коллоидной химии
- 4. Поперечный размер частицы (а) – диаметр для сферических частиц (d) и длина ребра для кубических частиц
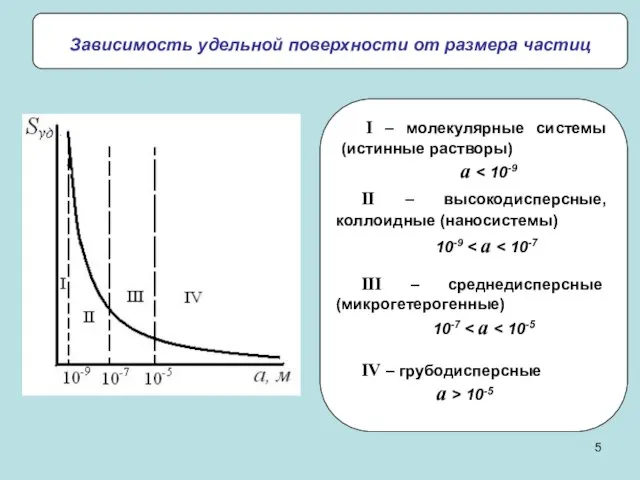
- 5. Зависимость удельной поверхности от размера частиц II – высокодисперсные, коллоидные (наносистемы) 10-9 III – среднедисперсные (микрогетерогенные)
- 6. Пример: Дисперсность частиц коллоидного золота 108 м-1. Принимая частицы золота в виде кубиков определить, какую поверхность
- 7. Особенности коллоидных систем 2. Термодинамическая неустойчивость 3. Невоспроизводимость (индивидуальность) 4. Способность к структурообразованию
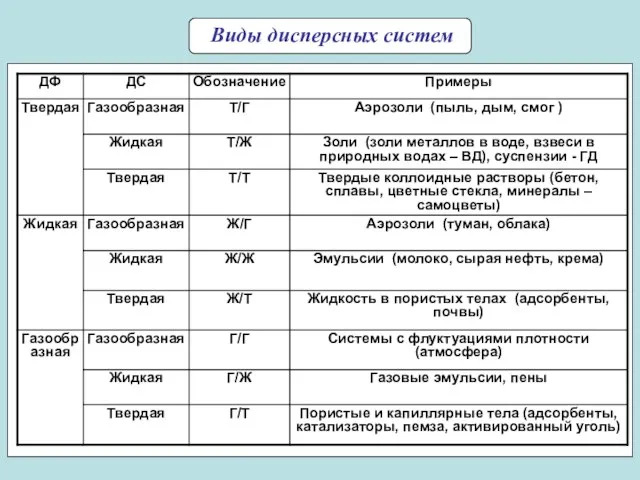
- 8. Виды дисперсных систем
- 9. Получение дисперсных систем измельчение крупных образцов вещества до частиц дисперсных размеров; химический состав и агрегатное состояние
- 10. Для облегчения диспергирования используют понизители твердости (электролиты, эмульсии, ПАВ и др.) Понизители твердости составляют 0,1 %
- 11. основаны на ассоциации молекул в агрегаты из истинных растворов; используют для получения высокодисперсных систем; не требуют
- 12. Стадии конденсации 2. Рост зародышей. 3. Формирование слоя стабилизатора (ДЭС).
- 13. Физические конденсационные методы
- 14. Химические конденсационные методы
- 16. 3. Реакции окисления Образование золя серы. 2H2Sр-р + O2 = 2S ↓+ 2H2O Строение мицеллы:
- 17. 4. Реакции гидролиза Получение золя гидроксида железа. FeCl3 + 3H2O = Fe(OH)3 ↓ + 3HCl Cтроение
- 18. Метод пептизации
- 19. Низкомолекулярные примеси (чужеродные электролиты) разрушают коллоидные системы. Диализ – отделение золей от низкомолекулярных примесей с помощью
- 20. Особенности коллоидных растворов Опалесценция (светорассеяние) наблюдается когда λ > d. Чем короче длина волны падающего света,
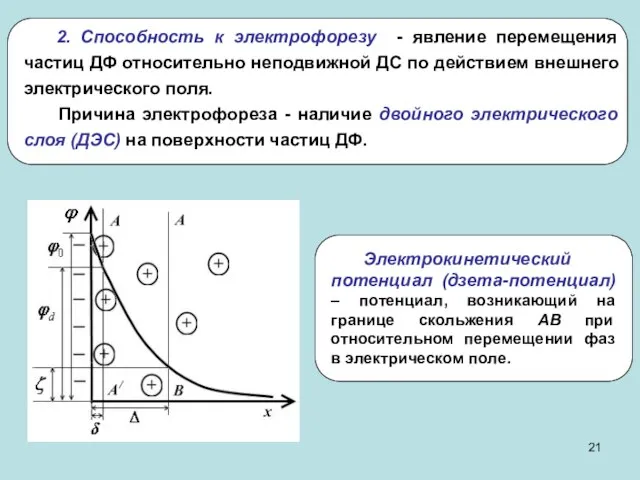
- 21. 2. Способность к электрофорезу - явление перемещения частиц ДФ относительно неподвижной ДС по действием внешнего электрического
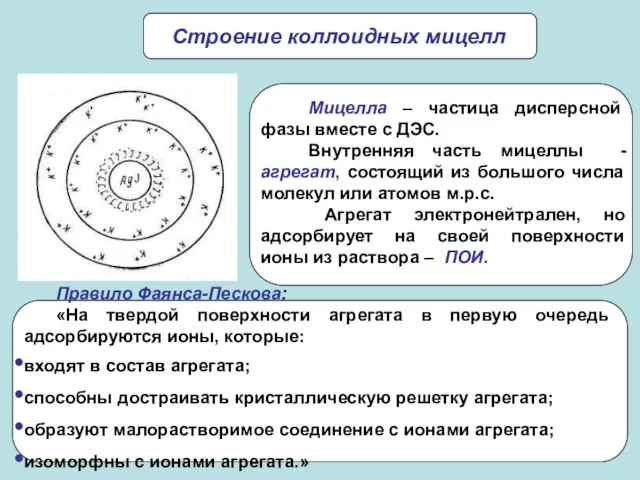
- 22. Строение коллоидных мицелл
- 24. Пример 1:
- 25. Устойчивость и коагуляция дисперсных систем
- 26. Коагуляция золей электролитами Все электролиты при определенной концентрации могут вызвать коагуляцию золя. Правило знака заряда: коагуляцию
- 27. Порог коагуляции (γ, Скр) – наименьшая концентрация электролита, достаточная для того, чтобы вызвать коагуляцию золя Коагулирующая
- 29. Скачать презентацию






















 Анализ бюджета телеканала
Анализ бюджета телеканала 1c
1c Дидактические системы и модели обучения, факторы и цели
Дидактические системы и модели обучения, факторы и цели Wellnessland. Скидки. Акции
Wellnessland. Скидки. Акции Инструменты и приспособления, применяемые при выполнении ручных работ
Инструменты и приспособления, применяемые при выполнении ручных работ Демонстрация возможностей ПО сайта закупок и продаж ОАО АНК «Башнефть» (http://zakupki.bashneft.ru)
Демонстрация возможностей ПО сайта закупок и продаж ОАО АНК «Башнефть» (http://zakupki.bashneft.ru) Что такое география и как мы будем ее изучать
Что такое география и как мы будем ее изучать День приятных неожиданностей
День приятных неожиданностей Презентация на тему Основные положения МКТ
Презентация на тему Основные положения МКТ Оценка трудозатрат на тестирование в проектах сопровождения (Два стандартных вопроса в Luxoft) Александр Александров, Luxoft www.luxoft.com
Оценка трудозатрат на тестирование в проектах сопровождения (Два стандартных вопроса в Luxoft) Александр Александров, Luxoft www.luxoft.com Эксклюзивная служба распространения «Царская почта» - единственная зарегистрированная курьерская служба по закрытым поселкам Ру
Эксклюзивная служба распространения «Царская почта» - единственная зарегистрированная курьерская служба по закрытым поселкам Ру Символы и церемонии олимпийских игр
Символы и церемонии олимпийских игр Памятники животным
Памятники животным Причины многообразия религий. Введение
Причины многообразия религий. Введение Проект “ОЦІНКА ПОТЕНЦІАЛУ ЯКІСНИХ ПРОДУКТІВ ХАРЧУВАННЯ З ПРИВ’ЯЗКОЮ ДО МІСЦЯ ПОХОДЖЕННЯ ТА ПОПИТУ НА НИХ В УКРАЇНІ”
Проект “ОЦІНКА ПОТЕНЦІАЛУ ЯКІСНИХ ПРОДУКТІВ ХАРЧУВАННЯ З ПРИВ’ЯЗКОЮ ДО МІСЦЯ ПОХОДЖЕННЯ ТА ПОПИТУ НА НИХ В УКРАЇНІ”
 Мастер-класс
Мастер-класс в Стрежевом 5 лет
в Стрежевом 5 лет Obschaya_prezentatsia_po_stroitelnym_materialam
Obschaya_prezentatsia_po_stroitelnym_materialam Мороженое – сладкая радость
Мороженое – сладкая радость Детство поэта Н.А. Некрасова
Детство поэта Н.А. Некрасова Файловая система
Файловая система Презентация на тему Диагностика предметной обученности
Презентация на тему Диагностика предметной обученности Какими качествами должен обладать психолог-консультант
Какими качествами должен обладать психолог-консультант Александр II
Александр II Налоги зарубежных стран
Налоги зарубежных стран ¿Qué hora es?
¿Qué hora es? Работа над магистерской диссертацией (выпускной квалификационной работой ). Часть I
Работа над магистерской диссертацией (выпускной квалификационной работой ). Часть I