Слайд 2Кислоты
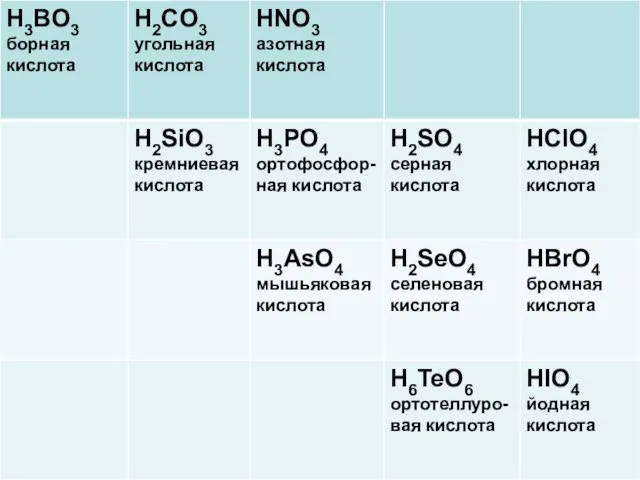
Высшим оксидам неметаллов соответствуют следующие кислоты

Слайд 3Высшим оксидам неметаллов соответствуют следующие кислоты
Слайд 4Кислоты
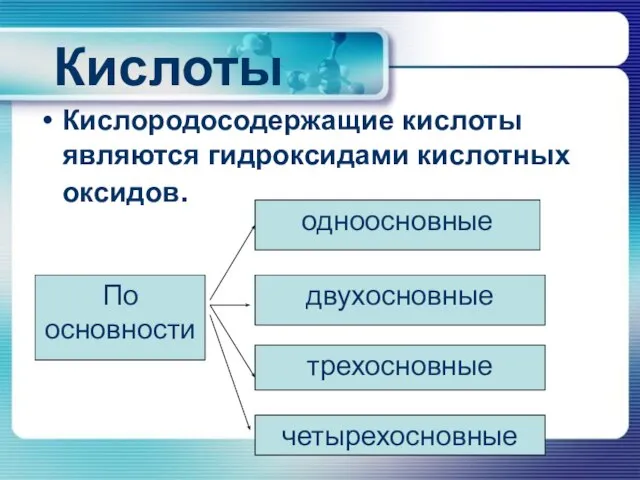
Кислородосодержащие кислоты являются гидроксидами кислотных оксидов.
По основности
одноосновные
двухосновные
трехосновные
четырехосновные
Слайд 5Кислоты
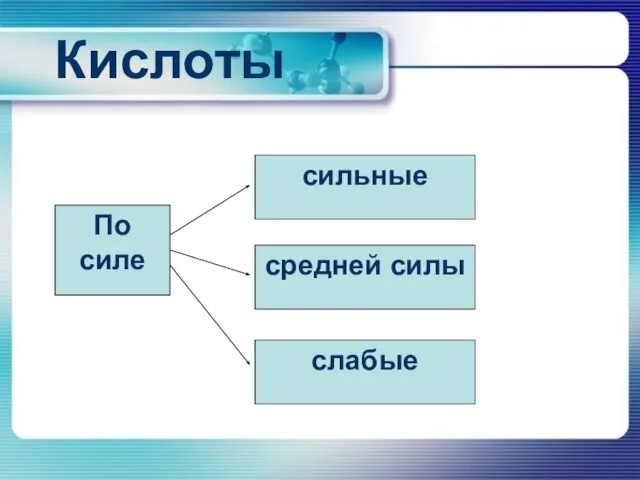
По силе
сильные
средней силы
слабые
Слайд 6Кислоты
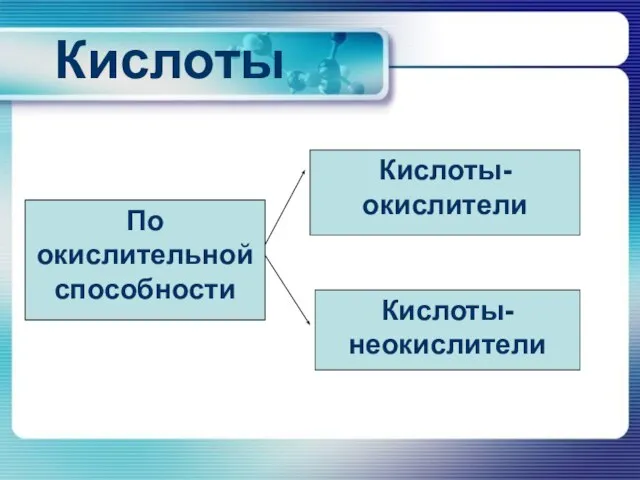
По окислительной способности
Кислоты-окислители
Кислоты-неокислители
Слайд 7Кислоты
По летучести
летучие
нелетучие
Слайд 8Кислоты
По устойчивости (прочности)
устойчивые
неустойчивые
Слайд 9Кислоты
Физические свойства
По агрегатному состоянию:
большинство кислот жидкости
некоторые растворы газов в воде (H2CO3,

H2SO3)
некоторые твердые вещества (H3PO4, H3BO3, HIO4)
Слайд 10Кислоты
Почти все кислоты хорошо растворимы в воде кроме H2SiO3
При растворении в воде

метакислоты переходят в ортокислоты
HPO3 + H2O =
Слайд 11Кислоты
Общие химические свойства кислот:
Попробуйте вспомнить и перечислите все химические свойства. Приведите пример

на каждое свойство (молекулярные и ионные уравнения).
Слайд 12Кислоты
Кислоты-неокислители взаимодействуют с металлами стоящими в ряду напряжений до водорода и образуется

водород и соль металла с низшей С.О.
Слайд 13Кислоты
Кислоты-окислители (H2SO4, HNO3) в водном растворе вступают в реакции практически со всеми

металлами (кр.Au, Pt ). В качестве окислителя выступает анион кислотного остатка. В результате этих реакций образуются соль металла в высшей С.О., вода и продукт восстановления кислоты.
Слайд 14Кислоты
Почти все кислоты разлагаются при нагревании.
Если при разложении не происходит ОВР, то

продуктами разложения являются вода и кислотный оксид(или кислота с меньшим содержанием H2O)
Слайд 15Кислоты
Если разложение ОВР, то продукты разнообразны:
4HNO3 = 4NO2 + O2 + 2H2O
3HNO2

= HNO3 + 2NO + H2O
3HClO = 2HCl + HClO3
4H3PO3 = 3H3PO4 + PH3
Слайд 16Кислоты
С неметаллами реагируют только кислоты обладающими сильными окислительными свойствами.
При их взаимодействии

неметалл окисляется до соответствующей кислоты(или ее ангидрида), а кислота восстанавливается до газообразного оксида.
H2SO4 (конц)- SO2 HNO3(конц)- NO2
HNO3(разб)- NO
Слайд 17Кислоты
S + HNO3 (разб) =
S + HNO3 (конц) =
C + HNO3 (конц)

=
S + H2SO4 (конц) =
P + HNO3 (конц) =
P + HNO3 (разб) =
Слайд 18Кислоты
Кислоты-окислители могут реагировать с безкислородными кислотами, обладающими восстановительными свойствами
H2SO4 (конц) + 2HBr

= Br2 + SO2 + 2H2O
H2SO4 (конц) + 8HI = 4I2 + H2S + 4H2O
H2SO4 (конц) + H2S = S + SO2 + 2H2O
8HNO3 (конц) + H2S = H2SO4 + 8NO2 + H2O

















 Общий анализ сложившейся правоприменительной практики арбитражных судов в условиях COVID-19
Общий анализ сложившейся правоприменительной практики арбитражных судов в условиях COVID-19 «Свободная цена»: решение для независимых музыкантов и НКО
«Свободная цена»: решение для независимых музыкантов и НКО Образование болот
Образование болот Прием переписного персонала
Прием переписного персонала Инфекционные болезни 4
Инфекционные болезни 4 Геометрические фигуры 4 класс
Геометрические фигуры 4 класс Профессиональные функции и умения старшего воспитателя ДОУ
Профессиональные функции и умения старшего воспитателя ДОУ История причёсок
История причёсок Информация по экологии
Информация по экологии Цицерон - философ Древнего Рима
Цицерон - философ Древнего Рима Unit 1 Speaking about seasons and weather
Unit 1 Speaking about seasons and weather “Привлечение общественности и поддержка гражданского общества в реализации Орхуской конвенции” EuropeAid/122449/C/SER/Multi
“Привлечение общественности и поддержка гражданского общества в реализации Орхуской конвенции” EuropeAid/122449/C/SER/Multi ЭЛЕКТРОННЫЙ ЖУРНАЛ ПЕДАГОГА
ЭЛЕКТРОННЫЙ ЖУРНАЛ ПЕДАГОГА Орфография. Морфемика. Словообразование
Орфография. Морфемика. Словообразование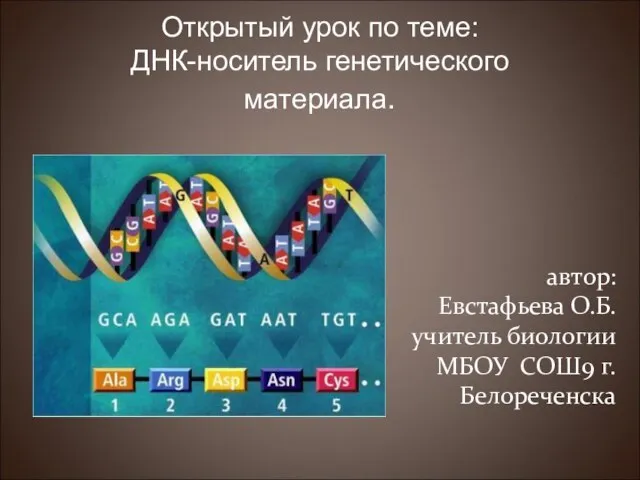 Открытый урок по теме: ДНК-носитель генетического материала.
Открытый урок по теме: ДНК-носитель генетического материала. КАФЕДРА УПРАВЛЕНИЯ И ЗАЩИТЫ В ЧРЕЗВЫЧАЙНЫХ СИТУАЦИЯХ
КАФЕДРА УПРАВЛЕНИЯ И ЗАЩИТЫ В ЧРЕЗВЫЧАЙНЫХ СИТУАЦИЯХ Свобода в деятельности человека
Свобода в деятельности человека Сенсорная характеристика как составляющая качества продуктов. Лекция 1
Сенсорная характеристика как составляющая качества продуктов. Лекция 1 Освободительная война в Нидерландах
Освободительная война в Нидерландах  пицца
пицца Софизмы.
Софизмы. Бактерии в жизни человека
Бактерии в жизни человека Программирование на языке Q Basic
Программирование на языке Q Basic Путешествие по Вселенным. Часть 1
Путешествие по Вселенным. Часть 1 Психологическая подготовка боксеров-юношей
Психологическая подготовка боксеров-юношей Как разрушить жизнь, когда вы молоды
Как разрушить жизнь, когда вы молоды Теологическая парадигма: И. Т. Посошков – аргументы в пользу правого суда
Теологическая парадигма: И. Т. Посошков – аргументы в пользу правого суда Презентация на тему Как вести себя в транспорте
Презентация на тему Как вести себя в транспорте