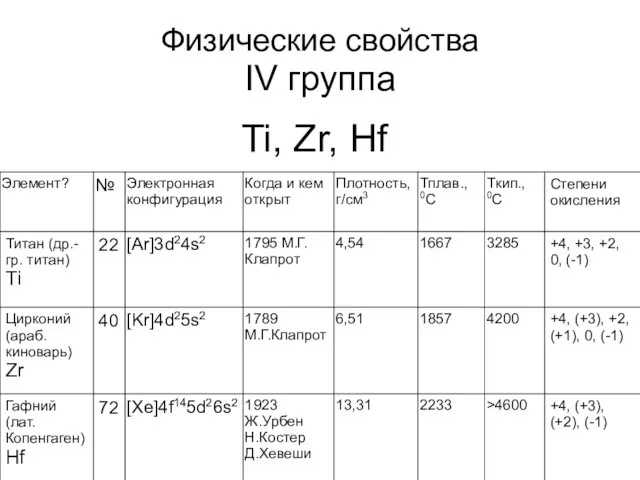
Слайд 2Физические свойства
IV группа
Ti, Zr, Hf
Слайд 3Нахождение в природе
Ti — в коре 0,63% по массе, основные минералы: рутил

TiO2, ильменит FeTiO3, перовскит CaTiO3 и еще более ста других.
Zr — в коре 0,016% по массе, основные минералы: циркон ZrSiO4, бадделеит ZrO2, всего более 30 минералов.
Hf — 3*10-4% по массе, собственных минералов не имеет, но часто сопутствует циркону в виде гафнона HfSiO4.
Слайд 4Получение в промышленности
Все элементы IV группы обычно получают восстановлением хлоридов или фторидов

МХ4 с помощью активных металлов (Mg, Ca, Na).
MCl4+2Mg → M+2MgCl2 (9000С)
MCl4+4Na → M+4NaCl (8000С)
Для более полной очистки используют, например, иодидное рафинирование (процесс Ван-Аркеля де Бура):
Ti+2I2 → TiI4↑ (2000С)
TiI4 → Ti +2I2 (14000С)
Слайд 5Химические свойства
Металлы инертны из-за пассивации, однако хорошо растворимы в плавиковой, щавелевой и

т.п. кислотах ввиду комплексообразования:
M+6HF → H2[MF6]+2H2↑
Металлы и оксиды при нагревании медленно растворяются в щелочах:
M+2NaOH+H2O → Na2MO3+2H2↑
Галогениды МХ4 — б/цв твердые в-ва, но TiCl4 — жидкость!
Также возможно получение оксосоединений типа TiOSO4 со сложным строением.
Слайд 6Химические свойства
Низшие степени окисления характерны только для титана, так при нагревании он

реагирует с разбавленными кислотами:
2Ti+6HCl → 2TiCl3+3H2↑
Аналогично с плавиковой кислотой,но в таких условиях происодит диспропорционирование:
2Ti+6HF → [TiF6]2-+Ti2++3H2O
Ti+6HF → H2[TiF6]+2H2O
Кроме того, для титана получены субоксиды состава Ti1-xO, Ti3O,Ti6O, имеющие кластерное строение.
Слайд 7Полисоединения элементов
IV группы
При гидролизе некоторых соединений(МХ4) возможно получить соединения состава MO2*xH2O,
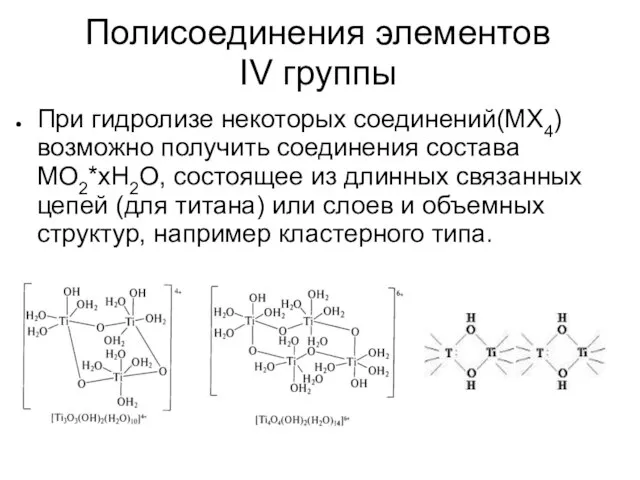
состоящее из длинных связанных цепей (для титана) или слоев и объемных структур, например кластерного типа.
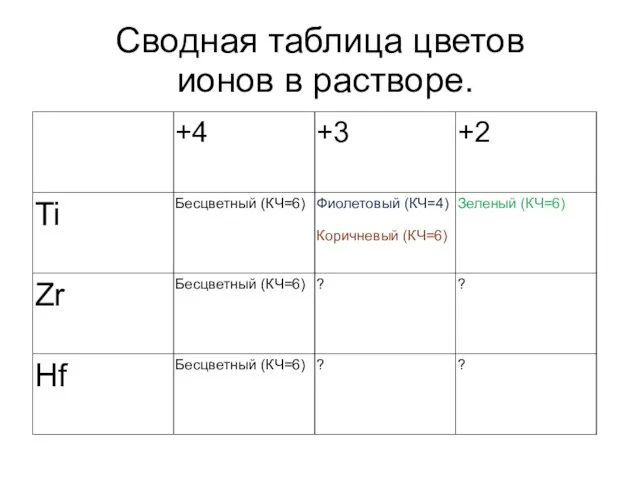
Слайд 8Сводная таблица цветов
ионов в растворе.
Слайд 9Применение
Ti — активно используется в металлургии (сверхлегкие и сверхпрочные сплавы, сплавы с

эффектом памяти), самоочищающиеся поверхности (TiO2).
Zr — добавка в некоторые сплавы, отражатель нейтронов.
Hf — поглотитель нейтронов в ядерных реакциях
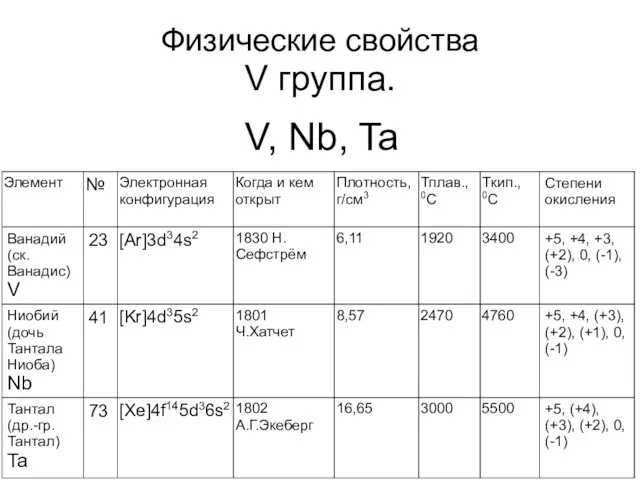
Слайд 10Физические свойства
V группа.
V, Nb, Ta
Слайд 11Нахождение в природе
V — в коре 0,014% по массе, основные минералы: патронит

VS4, ванадинит Pb5(VO4)3Cl и еще около 90 других.
Nb — в коре 0,002% по массе, основные минералы: ферроколумбит FeNb2O6 и пр.
Ta — 0,0017% по массе, основные минералы: ферротанталит FeTa2O6 и пр.
Тем не менее, данные элементы намного чаще встречаются в виде примесей в иных минералах.
Слайд 12Получение в промышленности
Ванадий чаще всего получают из шлака после обработки железных руд

в виде FeV2O4:
4FeV2O4+8NaCl+7O2 → 8NaVO3+2Fe2O3+4Cl2 (t)
2FeV2O4+9Cl2 → 4VOCl3+2FeCl3+2O2 (t)
Ниобий и тантал также получают из шлака, однако разделяют их фтороводородом:
4FeNb2O6+64HF+O2 →
→ 4H3[FeF6]+8H2[NbOF5]+18H2O
4FeTa2O6+80HF+O2 →
→ 4H3[FeF6]+8H2[TaF7]+26H2O
Слайд 13Химические свойства
Металлы также очень инертны, особенно Nb, Ta.
Ванадий растворяется только в конц.

кислотах, прочие же металлы — только в HF и его смесях:
V+6HNO3 → VO2NO3+5NO2↑+3H2O
2M+12HF → 2H[MF6]+5H2↑
Также они растворимы при сплавлении с конц. щелочами в присутствии окислителей :
4M+5O2+12KOH → 4K3MO4+6H2O
Слайд 14Формы ванадия в растворе
В зависимости от рН ванадий может принимать различные формы:

V+5 → VO2+ → HVO3 → VO3-
V+4 → VO2+ → H2VO3 → VO32-
сверх-кислая→кислая→нейтральная→щелочная
Кроме того, известен аналогичный оксокатион для V+3 → VO+.
Подобные оксокатионы проявляются и у Nb с Ta, но в чуть меньшей степени.
Слайд 15Полисоединения элементов
5-й группы
Анионы ванадиевых кислот при изменении рН образуют гигантские полисоединения
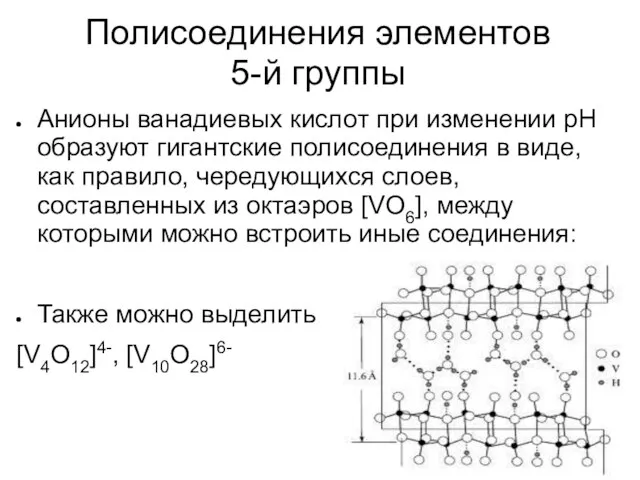
в виде, как правило, чередующихся слоев, составленных из октаэров [VO6], между которыми можно встроить иные соединения:
Также можно выделить
[V4O12]4-, [V10O28]6-
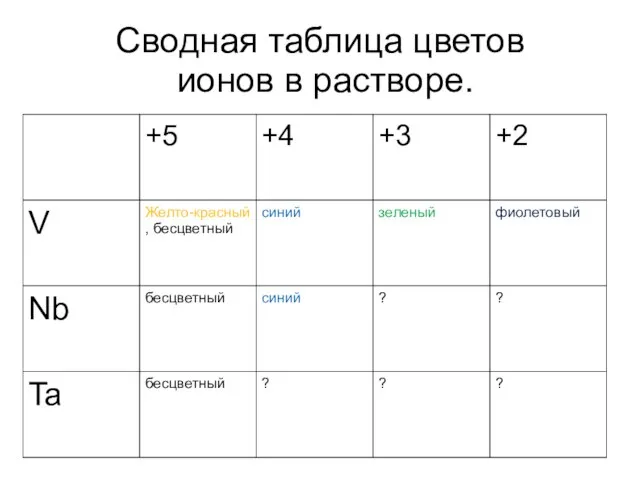
Слайд 16Сводная таблица цветов
ионов в растворе.
Слайд 17Применение
V, Nb и Ta часто используются как легирующие добавки к стали, а

также иногда в виде отдельных сплавов (феррованадий) и бронз.
Производные ванадия также активно используются в катализе, источниках тока и т. п.
Соединения ниобия (карбид) изпользуются как антикоррозийные покрытия для турбин самолетов и т. д.
Сверхпроводники
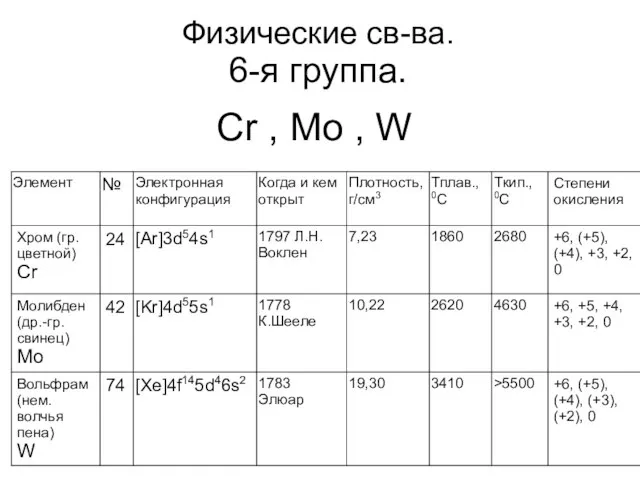
Слайд 18Физические св-ва.
6-я группа.
Cr , Mo , W
Слайд 19Нахождение в природе
Cr — в коре 0,035% по массе, основные минералы: хромит

FeCr2O4, крокоит PbCrO4 и пр.
Mo — в коре 3*10-4% по массе, основные минералы: молибденит MoS2, повеллит CaMoO4 и пр.
W — 0,0017% по массе, основные минералы: вольфрамит (Fe,Mn)WO4, шеелит CaWO4 и пр.
Слайд 20Получение в промышленности
Технический хром удобно получать из хромита:
4FeCr2O4+8Na2CO3+7O2 → → 8Na2CrO4+2Fe2O3+8CO2

(t)
K2Cr2O7+2C → Cr2O3+K2CO3+CO (t)
Вольфрам обогащают обычно флотацией, а после этого очищают т. н. щелочным методом:
2CaWO4+2Na2CO3+SiO2 → → 2Na2WO4+Ca2SiO4+2CO (t)
Слайд 21Химические свойства
Металлы пассивируются в конц. кислотах.
Хром хорошо растворяется в разб. кислотах:
Cr+2HCl

→ CrCl2+H2 (в отсутствии окислителей)
Не происходит растворения в щелочах.
Mo, W инертны по отношению к кислотам
Все металлы окисляются в щелочных расплавах:
M+3KNO3+2KOH → K2MO4+3KNO2+H2O
Слайд 22Полисоединения элементов
6-й группы
Все элементы 6-й группы образуют изополисоединения. М+6 чаще всего
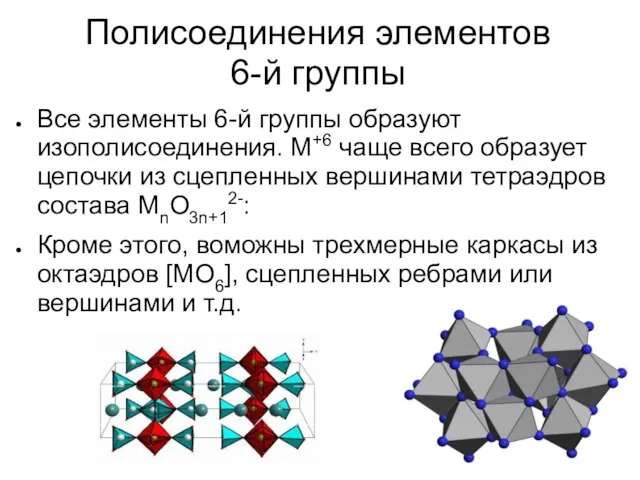
образует цепочки из сцепленных вершинами тетраэдров состава МnO3n+12-:
Кроме этого, воможны трехмерные каркасы из октаэдров [МO6], сцепленных ребрами или вершинами и т.д.
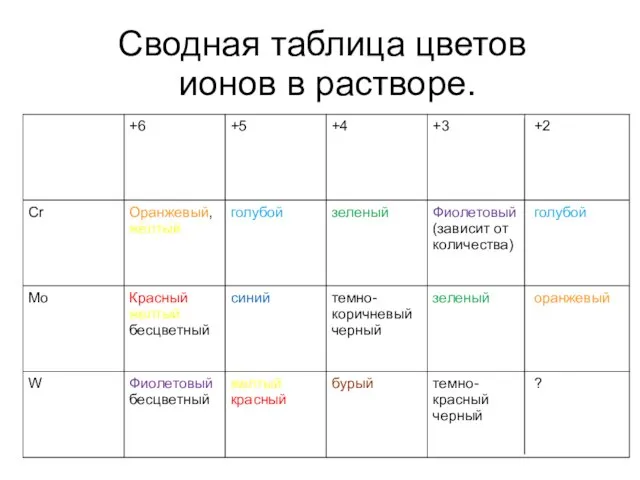
Слайд 23Сводная таблица цветов
ионов в растворе.
Слайд 24Применение
Cr — в металлургии: нержавеющие стали, декоративные покрытия; также зеркала, абразивы; в

хим.промышленности: пигменты, катализаторы и т.п.
Mo, W — часто используются как добавка к сталям для придания жаропрочностии твердости сплавам, соединения известны как катализаторы. Кроме этого используются в электронике и т.п.
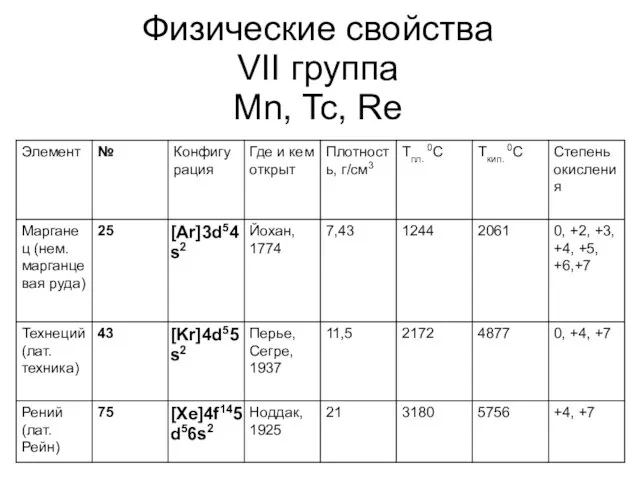
Слайд 25Физические свойства
VII группа
Mn, Tc, Re
Слайд 26Нахождение в природе
Mn – в коре 0,1% по массе, основные минералы: пиролюзит

MnO2
Tc – синтетический элемент
Re – в коре 7∙10-8% по массе, рассеянный элемент (примесь молибденита), основной минерал: CuReS4 – джезказганит.
Слайд 27Получение в промышленности
Mn – восстановление пиролюзита при нагревании: 4MnO2=2Mn2O3 + O2; Mn2O3

+ 2Al = 2Mn + Al2O3
Tc – получают из радиоактивных отходов промышленности
Re – обжиг минералов с последующим восстановлением: 4ReS2+15O2=2Re2O7+8SO2; Re2O7+7H2=2Re+7H2O
Слайд 28Химические свойства
В высших степенях окисления – сильные окислительные свойства, в низших –

практически не проявляют восстановительных
Марганец растворим в кислотах достаточно быстро, рений – гораздо медленнее
С щелочами марганец реагирует только в присутствии окислителей
Слайд 29Сводная таблица цветов ионов в растворе
Тут с таблицей будет неудобно, так как

рений и технеций в растворах являются бесцветными, а марганец проявляет самую различную окраску: +2 – бесцветный раствор (в твёрдом – очень слабо-розовый), +4 – бурый, +5 – синий (в сильнощелочных средах), +6 – зелёный, +7 – от розового до фиолетового (в зависимости от концентрации ионов)




























 Квиллинг-Необычные возможности обычной бумаги
Квиллинг-Необычные возможности обычной бумаги Презентация на тему Наш друг светофор
Презентация на тему Наш друг светофор г.Донецк
г.Донецк MAPLE
MAPLE Металлургия в Китае
Металлургия в Китае Фрезы для педикюра
Фрезы для педикюра Закон Ома для участка цепи
Закон Ома для участка цепи Герои Советского Союза Петуховского района к 65- летию Великой Победы
Герои Советского Союза Петуховского района к 65- летию Великой Победы Дидактическое пособие по формированию финансовой грамотности старших дошкольников Банковский терминал
Дидактическое пособие по формированию финансовой грамотности старших дошкольников Банковский терминал FOREIGN TRADE
FOREIGN TRADE  Применение компрессорно- конденсаторных блоков с плавным регулированием производительности компрессора в технологическом охлаж
Применение компрессорно- конденсаторных блоков с плавным регулированием производительности компрессора в технологическом охлаж МАРКЕТИНГОВА ЦІНОВА ПОЛІТИКА
МАРКЕТИНГОВА ЦІНОВА ПОЛІТИКА  Symbology of the Russian Federation
Symbology of the Russian Federation Роль системы развития персонала организации
Роль системы развития персонала организации Поиск творческого решения
Поиск творческого решения Применение специальных упражнений для восстановления зрения, исправления осанки и снижения веса9_urok_fizkultury
Применение специальных упражнений для восстановления зрения, исправления осанки и снижения веса9_urok_fizkultury База данных (БД) – основа информационных систем(ИС)
База данных (БД) – основа информационных систем(ИС) ГОСТ 102-75. Фанера березовая авиационная. Технические условия
ГОСТ 102-75. Фанера березовая авиационная. Технические условия Японская символика
Японская символика Надежность и долговечность автомобиля. Техническое обслуживание и ремонт машин
Надежность и долговечность автомобиля. Техническое обслуживание и ремонт машин Разработка масштабируемой системы диагностирования технологического оборудования
Разработка масштабируемой системы диагностирования технологического оборудования Урок истории России в 7 классе
Урок истории России в 7 классе Презентация на тему фразеологизмы
Презентация на тему фразеологизмы  Основные положения теории деятельности А. Н. Леонтьева
Основные положения теории деятельности А. Н. Леонтьева 13
13 Учитель математики МОУ СОШ 1 Тупикова Л. М.. «Мне приходится делить время между политикой и уравнениями. Однако уравнения, по-моему,
Учитель математики МОУ СОШ 1 Тупикова Л. М.. «Мне приходится делить время между политикой и уравнениями. Однако уравнения, по-моему,  Презентация на тему Молдавия
Презентация на тему Молдавия  Eyebrow tremor
Eyebrow tremor