Содержание
- 2. Жоспар: Кіріспе Негізгі бөлім Периодтық жүйесінің ашылу тарихы Периодтық жүйесінің құрылымы Химиялық элементтердің периодтық жүйесі маңызы
- 3. Кіріспе Химиялық элементтердің периодтық жүйесі — элементтердің әртүрлі қасиеттерінің атом ядросы зарядына тәуелділігін белгілейтін химиялық элементтердің
- 5. Жүйе атақты орыс химигі Д. И. Менделеевтің 1869 жылы ашқан периодтық заңының графикалық түрде бейнеленуі болып
- 6. Негізгі бөлім Алғашқы кестеде Менделеев әлі ашылмаған бірнеше элементтер бар екенін болжап, оларға кестеде тиісті орын
- 7. Сонымен қатар Менделеев марганецке (қазіргі технеций Тс және рений Re), теллурге (полоний Ро), йодқа (астат At),
- 8. Радиоактивтік ыдыраудың (1806), рентген сәулелерінің (1895) ашылуы, неміс физигі М.Планктің сәуле шығарудың кванттық теориясын (1900), ағылшын
- 9. Ағылшын физигі Г.Мозли еңбектерінің нәтижесінде Менделеев ұсынған әр элементтің рет нөмерінің оның ядро зарядымен тең болуы,
- 10. Қазіргі Э. п. ж.126 хим. элементті қамтиды, олардан трансуран элементтері (Z – 93 – 110) және
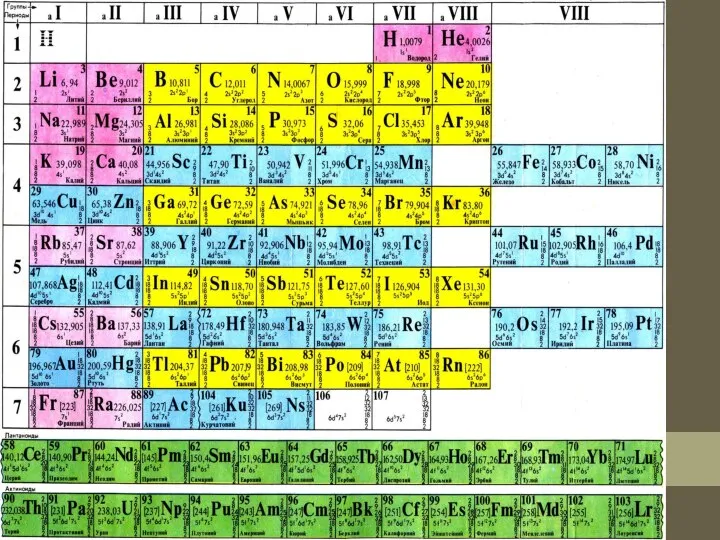
- 11. Периодтық жүйесінің құрылымы Қазіргі кездегі периодтық жүйеде барлық элементтер рет бойынша нөмірленген. Элементтердің нөмерін реттік немесе
- 12. Периодтар Период деп сілтілік металдан басталып инертті газбен аяқталатын элементтер тобын айтады.
- 13. Периодтар горизонталь қатардан тұрады. Периодтық жүйеде 7 период бар, олар рим сандарымен белгілеген, I, II және
- 14. Қатарлар Периодтарда араб сандарымен белгіленген 10 қатар кіреді. Үлкен периодтардың жұп қатарларында (төртінші, алтыншы, сегізінші және
- 15. Топтар Тігінен орналасқан элементтердің қатарын топтар деп атайды. Периодтық жүйеде сегіз топ бар, олардың нөмері рим
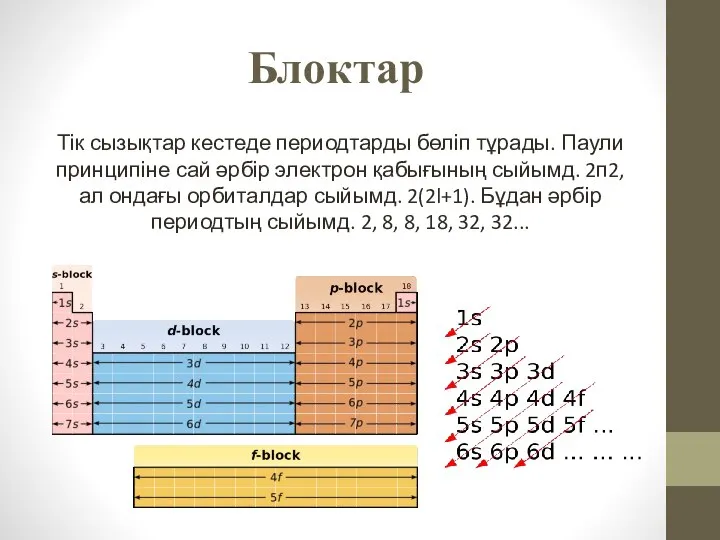
- 16. Блоктар Тік сызықтар кестеде периодтарды бөліп тұрады. Паули принципіне сай әрбір электрон қабығының сыйымд. 2п2, ал
- 17. Әр периодтың басы жаңа мәніне сай келетін s – элементтен басталады ( Қа-, ІҚа-топшалар), соңы р
- 18. Химиялық элементтердің периодтық жүйесі маңызы Химиялық элементтердің периодтық жүйесі – периодтық заңның графиктік бейнесі, олар өзара
- 19. Химиялық элементтердің периодтық жүйесі ашылған кезде көптеген элементтер белгісіз еді. Д. И. Менделеев аса үлкен болжампаздықпен
- 20. Галлий Ga 1875 ж., скандий Sc 1879 ж., германий (Ge) 1885 ж. ашылды. Д. И. Менделеев
- 21. Қорытынды Химиялық элементтердің периодтық жүйесі – периодтық заңның графиктік бейнесі, олар өзара тығыз байланысты, бірін-бірі толықтыра
- 23. Скачать презентацию


















 Не убивай!
Не убивай! My life
My life Radio
Radio  Презентация на тему Измерение физических величин
Презентация на тему Измерение физических величин Работа с мультимедийным оборудованием: проектор, интерактивная доска, веб-камера, аудио-оборудованиеПериферийное оборудование: п
Работа с мультимедийным оборудованием: проектор, интерактивная доска, веб-камера, аудио-оборудованиеПериферийное оборудование: п Имена прилагательные, близкие и противоположные по смыслу
Имена прилагательные, близкие и противоположные по смыслу Предмет астрономии. Астрономия в древности.
Предмет астрономии. Астрономия в древности. Структурные типы данных
Структурные типы данных ABBYY TestReader 5.2Новое в версии 5.2
ABBYY TestReader 5.2Новое в версии 5.2 Прощай, начальная школа! Здравствуй, 5 класс!
Прощай, начальная школа! Здравствуй, 5 класс! Психология рисунка
Психология рисунка «ДОКУМЕНТЫ НУЖНО НЕ ТОЛЬКО ХРАНИТЬ…»
«ДОКУМЕНТЫ НУЖНО НЕ ТОЛЬКО ХРАНИТЬ…» Подарок. Умей благодарить
Подарок. Умей благодарить Реализация региональных проектов информатизации здравоохранения
Реализация региональных проектов информатизации здравоохранения Mary Jane Ansel
Mary Jane Ansel 1С-Битрикс: Корпоративный портал
1С-Битрикс: Корпоративный портал Презентация на тему Романтизм в музыке
Презентация на тему Романтизм в музыке  RISC V – новая эра процессоров
RISC V – новая эра процессоров Психологические особенности взрослого человека в период поздней взрослости: когнитивные особенности, аффективная сфера
Психологические особенности взрослого человека в период поздней взрослости: когнитивные особенности, аффективная сфера ?????
????? Cоциология поведения экономических агентов на финансовых рынках: роль культуры и социальных институтов
Cоциология поведения экономических агентов на финансовых рынках: роль культуры и социальных институтов Стильная классика Title
Стильная классика Title Интерактивный урок
Интерактивный урок Презентация на тему Культ личности И.В.Сталина
Презентация на тему Культ личности И.В.Сталина  In our region people wear…
In our region people wear… Способы работы с цветом: Гуашь
Способы работы с цветом: Гуашь Юридическое агентство «ЮС КОГЕНС»
Юридическое агентство «ЮС КОГЕНС» Лекарственные растения. Команда Весёлые огородники
Лекарственные растения. Команда Весёлые огородники