Слайд 2Цель урока:
Дать учащимся первоначальные понятия о кислородсодержащих веществах. Познакомить с составом и

строением одноатомных спиртов, дать понятие о функциональной группе атомов и влиянии ее на физические свойства. Знать определение спиртов, общую формулу .Уметь записывать уравнения химических реакций , доказывающих свойства спиртов.
Слайд 3Ход урока.
Определение спиртов: спирты- это производные углеводородов, в молекулах которых один или

несколько атомов углерода замещены на гидроксильную группу ( - ОН).
Или: спиртами называются органические вещества, молекулы которых содержат одну или несколько функциональных групп соединенных с углеводородным радикалом.
Слайд 4Гомологический ряд предельных одноатомных спиртов .
а) СН3 ОН - метиловый -

метанол
С2 Н5 ОН - этиловый –этанол
С3 Н7 ОН -пропиловый -пропанол
С4 Н9 ОН – бутиловый –бутанол
С5 Н11 ОН - амиловый -пентанол
б) Общая формула
R- OH или СnН2n +1 ОН
Слайд 5КЛАССИФИКАЦИЯ СПИРТОВ
а)Спирты могут быть первичными, вторичными, третичными:
Если спирт содержит группу - ОН

связанную с первичным атомом углерода RCH2 OH он первичный
Вторичные RR` CHOH группа - ОН связана со вторичным атомом углерода
Третичные RR`R``COH группа атомов связана с третичным атомом углерода
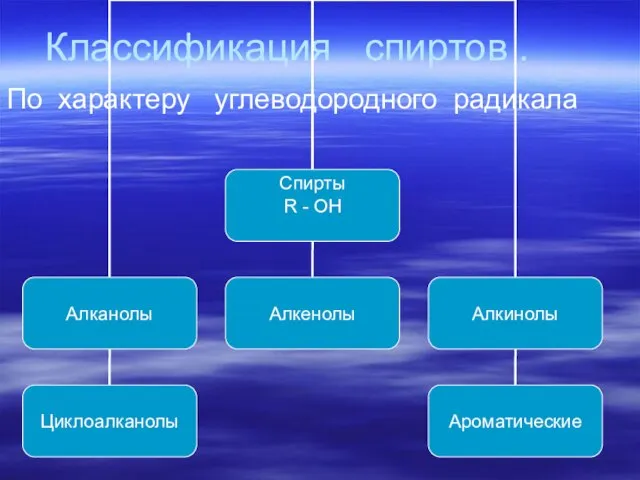
Слайд 6Классификация спиртов .
По характеру углеводородного радикала
Слайд 7По количеству гидроксильных групп спирты могут быть:
Одноатомными С2 Н5 ОН этанол
Двухатомные С

Н 2 -О Н 2,2 -этандиол
С Н 2 - О Н (этиленгликоль)
Трехатомные С Н 2 -ОН
С Н -ОН 1,2,3 - пропантриол
С Н 2 -ОН (глицерин)
Также спирты можно разделить на две группы по количеству углеродных атомов в углеродном радикале: низшие (С 1 - С 10 )
И высшие ( свыше С10 )
Слайд 8ИЗОМЕРИЯ
Для спиртов характерно несколько видов структурной изомерии: изомерия углеродного скелета ( изомерия

цепи ) ;изомерия положения группы -ОН, межклассовая изомерия .
СН3 –СН2- -СН2 –СН2 –ОН бутанол -1
СН3 -СН –СН2 –ОН 2 метил-пропанол -1
СН3
СН3 -СН –СН2 -СН3 бутанол- 2
ОН
Слайд 9Межклассовая изомерия
C4H10O
CH3-CH2-CH2-CH2-OH CH3-CH2-O-CH2-CH3
(бутанол – 1) (диэтиловый эфир)

Слайд 10Химические свойства спиртов
Реакции замещения
1. Замещение атома водорода в группе –ОН
2С2Н5ОН+2Na→2C2H5ONa+H2

(этанол) (этилат натрия)
2. Реакции этерификации
C2H5OH+HONO2→C2H5ONO2+H2O
(этилнитрат)
Слайд 11 O H2SO4 O
CH3OH+CH3-C CH3-C +H2O
( метанол) OH O-CH3
(метилацетат)
3. Замещение
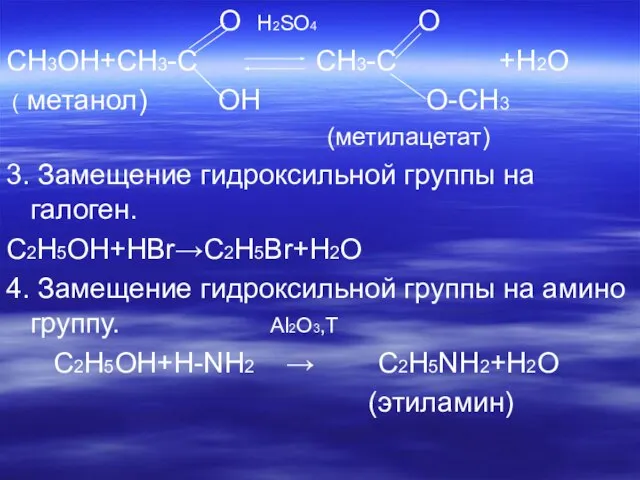
гидроксильной группы на галоген.
C2H5OH+HBr→C2H5Br+H2O
4. Замещение гидроксильной группы на амино группу. Al2O3,T
C2H5OH+H-NH2 → C2H5NH2+H2O
(этиламин)
Слайд 12Реакции отщепления (элиминирования)
Межмолекулярная дегидратация
140
С2Н5ОН+С2Н5ОН → С2Н5-О-С2Н5+Н2О
(диэтиловый эфир)
2. Внутримолекулярная дегидратация

180
СН3-СН2-СН-СН3 → СН3-СН=СН-СН3+Н2О
ОН
(бутанол-2) (бутен-2)
(правило Зайцева)
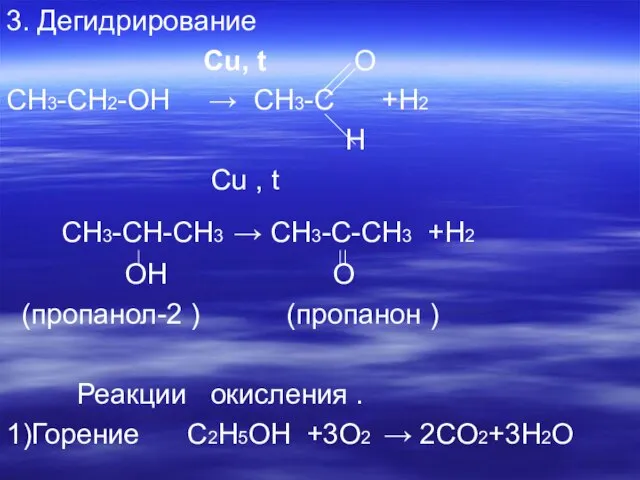
Слайд 133. Дегидрирование
Сu, t О
СН3-СН2-ОН → СН3-С +Н2
Н
Сu
, t
CH3-CH-CH3 → CH3-C-CH3 +H2
OH O
(пропанол-2 ) (пропанон )
Реакции окисления .
1)Горение C2H5OH +3O2 → 2CO2+3H2O
Слайд 14Не полное окисление .
О
С2H5OH + CuO CH3-C +H2O
(этанол) Н
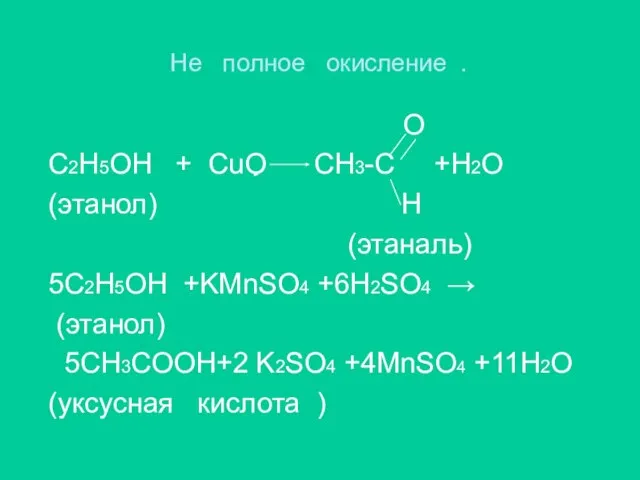
(этаналь)
5C2H5OH +KMnSO4 +6H2SO4 →
(этанол)
5CH3COOH+2 K2SO4 +4MnSO4 +11H2O
(уксусная кислота )
Слайд 15Способы получения алканолов.
Гидратация алкенов
СН2=СН2 +НОН → СН2-СН2-ОН
(этен) (этанол)

Щелочной гидролиз галогеналканов.
CH3CH2CH2Br + KOH → CH3CH2CH2OH +KBr
Гидрирование альдегидов и кетонов .
О
СН3СН2С + Н2 → СН3СН2СН2ОН
Н
(пропаналь) (пропанол-1)
Синтез из водяного газа
СО2 + 2Н2 → СН3ОН
Спиртовое брожение глюкозы
C6H12O6 → 2C2H5OH + 2CO2
Слайд 16Закрепление знаний, умений ,навыков .
Подготовить сообщения ,,Влияние алкоголя на организм человека ,,
















 Верный подход к выбору рекламной площадки. Поверил словам — проверь глазами или как я определяю целевую аудиторию
Верный подход к выбору рекламной площадки. Поверил словам — проверь глазами или как я определяю целевую аудиторию Система приема платежей под торговой маркой Апельсин
Система приема платежей под торговой маркой Апельсин Тепловые схемы. Расчет показателей тепловых схем электростанций
Тепловые схемы. Расчет показателей тепловых схем электростанций 20161207_egipet
20161207_egipet Презентация на тему 2 класс Математический диктант № 1
Презентация на тему 2 класс Математический диктант № 1  Презентация на тему Сложение и вычитание векторов
Презентация на тему Сложение и вычитание векторов  Правила построения жизнедеятельности без агрессии
Правила построения жизнедеятельности без агрессии Воспитание культурно-гигиенических навыков у детей младшего дошкольного возраста
Воспитание культурно-гигиенических навыков у детей младшего дошкольного возраста Кабан
Кабан Урок по рассказу Ивана Бунина «Холодная осень»
Урок по рассказу Ивана Бунина «Холодная осень» Цвета для рестайлинга
Цвета для рестайлинга Eco-fashion: 10 терминов экологичной моды
Eco-fashion: 10 терминов экологичной моды Конференция «Бизнес и этика»
Конференция «Бизнес и этика» «Кровь», 4класс
«Кровь», 4класс Гравюры на камне из Карелии. Гравёрная мастерская Контраст
Гравюры на камне из Карелии. Гравёрная мастерская Контраст Иллюстрированный словарь архитектурного стиля модерн
Иллюстрированный словарь архитектурного стиля модерн Из истории генетики.
Из истории генетики. Особенности создания мудбоарда при оформления интерьера
Особенности создания мудбоарда при оформления интерьера Презентация на тему Портфолио (Миляхова Оксана Вячеславовна)
Презентация на тему Портфолио (Миляхова Оксана Вячеславовна)  Сочинение по картине Т.Н. Яблонской «Утро»
Сочинение по картине Т.Н. Яблонской «Утро» Леди Баг и Супер Кот
Леди Баг и Супер Кот Здоровье и безопасность
Здоровье и безопасность Конституционное право РФ как наука и учебный курс
Конституционное право РФ как наука и учебный курс Криптовалюты: революция в электронных платежах
Криптовалюты: революция в электронных платежах Обобщение знаний о предлогах
Обобщение знаний о предлогах Деловые встречи
Деловые встречи Премиум тариф курса: Бизнес с Китаем. Роль посредника. Алгоритм выкупа через посредника и самостоятельный выкуп
Премиум тариф курса: Бизнес с Китаем. Роль посредника. Алгоритм выкупа через посредника и самостоятельный выкуп Знакомые ситуации Заказчик закрыт – отказывается сотрудничать Заказчик работает с другими и доволен Заказчик устраивает закупки
Знакомые ситуации Заказчик закрыт – отказывается сотрудничать Заказчик работает с другими и доволен Заказчик устраивает закупки